Hvordan gjorde John Dalton Ivent Atomic Theory?
1. Gamle græske rødder: Konceptet med atomer stammer tilbage til det gamle Grækenland med filosoffer som Democritus og Leucippus. De foreslog ideen om, at stof blev sammensat af udelelige partikler.
2. Daltons eksperimentelle observationer: Dalton var en omhyggelig eksperimentalist. Han studerede gassens opførsel, specifikt deres blandings- og reaktionsforhold. Han observerede, at kemiske reaktioner altid involverede specifikke proportioner af elementer (lov om bestemte proportioner), og at når elementer kombinerede i forskellige proportioner, dannede de forskellige forbindelser (lov om flere proportioner).
3. Postulering af atomteorien: Baseret på hans observationer foreslog Dalton følgende postulater i sin atomteori:
* Alle stof er sammensat af atomer, som er udelelige og uforglemmelige partikler.
* atomer af et givet element er identiske i størrelse, masse og andre egenskaber.
* atomer af forskellige elementer er forskellige i størrelse, masse og andre egenskaber.
* Kemiske reaktioner involverer kombination, adskillelse eller omarrangement af atomer.
* Forbindelser dannes, når atomer af forskellige elementer kombineres i faste forhold mellem hele nummeret.
4. Bygning på tidligere arbejde: Dalton bygget på andre videnskabers arbejde, herunder:
* Robert Boyle: Boyle's arbejde med gasser hjalp med at lægge grundlaget for Daltons forståelse af stoffets opførsel.
* Antoine Lavoisier: Lavoisiers arbejde med bevarelse af masse hjalp Dalton med at forstå, at kemiske reaktioner ikke blot var oprettelsen eller ødelæggelsen af stof, men snarere en omarrangering af eksisterende atomer.
5. Betydningen af Daltons teori: Daltons atomteori revolutionerede vores forståelse af kemi. Det gav en ramme for at forklare kemiske reaktioner og stoffernes egenskaber. Det banede også vejen for fremtidige opdagelser inden for atomstruktur.
nøglepunkter at huske:
* Daltons teori var ikke perfekt og er blevet raffineret over tid.
* Vi ved nu, at atomer kan deles i mindre partikler, og at atomer af det samme element kan have lidt forskellige masser (isotoper).
* På trods af sine begrænsninger forbliver Daltons atomteori en grundlæggende hjørnesten i moderne kemi.
 Varme artikler
Varme artikler
-
 Nu i 3D:Deep learning-teknikker hjælper med at visualisere røntgendata i tre dimensionerKredit:Pixabay/CC0 Public Domain Computere har været i stand til hurtigt at behandle 2D-billeder i nogen tid. Din mobiltelefon kan tage digitale fotografier og manipulere dem på en række måder. Me
Nu i 3D:Deep learning-teknikker hjælper med at visualisere røntgendata i tre dimensionerKredit:Pixabay/CC0 Public Domain Computere har været i stand til hurtigt at behandle 2D-billeder i nogen tid. Din mobiltelefon kan tage digitale fotografier og manipulere dem på en række måder. Me -
 Slående støj via superposition af ordreKredit:CC0 Public Domain Information kan med succes overføres via støjende kanaler ved hjælp af kvantemekanik, ifølge ny forskning fra The University of Queensland og Griffith University. Vi ved
Slående støj via superposition af ordreKredit:CC0 Public Domain Information kan med succes overføres via støjende kanaler ved hjælp af kvantemekanik, ifølge ny forskning fra The University of Queensland og Griffith University. Vi ved -
 Månen er en hård elskerinde-tyngdekraftspåvirkninger på NSLS-IIDette billede viser de daglige ændringer i NSLS-IIs radiofrekvens i overensstemmelse med månens faser. Forskere ved NSLS-II har observeret, at virkningerne af månens faser fremstår som en tydelig dukk
Månen er en hård elskerinde-tyngdekraftspåvirkninger på NSLS-IIDette billede viser de daglige ændringer i NSLS-IIs radiofrekvens i overensstemmelse med månens faser. Forskere ved NSLS-II har observeret, at virkningerne af månens faser fremstår som en tydelig dukk -
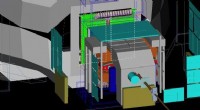 MoEDAL jagter dyonerIllustration af MoEDAL -detektorsystemet (guld- og lyseblå komponenter), omkring LHCb -eksperimentets VELO -detektor (central grå struktur). Kredit:CERN En magnetisk monopol er en teoretisk partik
MoEDAL jagter dyonerIllustration af MoEDAL -detektorsystemet (guld- og lyseblå komponenter), omkring LHCb -eksperimentets VELO -detektor (central grå struktur). Kredit:CERN En magnetisk monopol er en teoretisk partik
- At gruppere smarte byer i typer kan hjælpe håbefulde byplanlæggere med at finde en vej
- Fællesskabets stemme bør vejlede ekspanderende afrikanske byer
- hvordan overføres kulstof fra planter til dyr?
- Hvad er polariserbare anioner?
- Hvorfor opløses natriumchlorid i benzin?
- Hvad matematik fortæller os om sociale dilemmaer


