Hvad sker der med bevægelsen af partikler i en fast og flydende gas?
faste stoffer
* Partikelarrangement: Partikler er tæt pakket i et fast, regelmæssigt arrangement.
* Bevægelse: Partikler vibrerer på plads omkring deres faste positioner. De har meget begrænset bevægelse og kan ikke bevæge sig frit forbi hinanden.
* nøglegenskab: Faststoffer opretholder en bestemt form og volumen på grund af de stærke intermolekylære kræfter, der holder partikler sammen.
væsker
* Partikelarrangement: Partikler er tættere sammen end i en gas, men ikke så tæt pakket som i et fast stof. De har mere frihed til at bevæge sig rundt.
* Bevægelse: Partikler er i stand til at bevæge sig forbi hinanden og flyde, men de forbliver stadig i tæt kontakt. De udviser vibrations-, rotations- og translationelle bevægelse.
* nøglegenskab: Væsker har formen på deres beholder, men opretholder et konstant volumen. De er mindre komprimerbare end gasser på grund af den tættere partikelafstand.
Gasser
* Partikelarrangement: Partikler er bredt fordelt og bevæger sig frit uden fast arrangement.
* Bevægelse: Partikler har høj kinetisk energi og bevæger sig hurtigt i tilfældige retninger. De kolliderer med hinanden og væggene i deres beholder.
* nøglegenskab: Gasser fylder deres beholder helt og er meget komprimerbare, fordi partiklerne er langt fra hinanden.
Kortfattet:
* fast: Vibrationsbevægelse dominerer; Partikler er i det væsentlige låst på plads.
* væske: Vibrations-, rotations- og translationelle bevægelse; Partikler kan bevæge sig forbi hinanden, men forbliver i kontakt.
* gas: Tilfældig, hurtig translationel bevægelse; Partikler er langt fra hinanden og bevæger sig frit.
Vigtig note:
* Temperatur spiller en afgørende rolle i partiklernes bevægelse. Højere temperaturer betyder større kinetisk energi og hurtigere partikelbevægelse.
* Dette er en forenklet model. Ægte materialer kan udvise mere kompleks opførsel, især ved ekstreme temperaturer og tryk.
 Varme artikler
Varme artikler
-
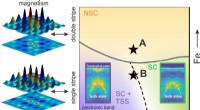 Kortlægning af de elektroniske tilstande i en eksotisk superleder(Venstre) Gennem neutronspredningsforsøg, forskere observerede distinkte mønstre af magnetiske korrelationer i superledende (enkelt-stribe magnetisme) og ikke-superledende (dobbelt-stribe magnetisme)
Kortlægning af de elektroniske tilstande i en eksotisk superleder(Venstre) Gennem neutronspredningsforsøg, forskere observerede distinkte mønstre af magnetiske korrelationer i superledende (enkelt-stribe magnetisme) og ikke-superledende (dobbelt-stribe magnetisme) -
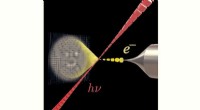 Ny teknik muliggør formning af elektronstrålerNylige eksperimenter ved universitetet i Wien viser, at lys (rødt) kan bruges til vilkårlig at forme elektronstråler (gul), hvilket åbner nye muligheder inden for elektronmikroskopi og metrologi. Kred
Ny teknik muliggør formning af elektronstrålerNylige eksperimenter ved universitetet i Wien viser, at lys (rødt) kan bruges til vilkårlig at forme elektronstråler (gul), hvilket åbner nye muligheder inden for elektronmikroskopi og metrologi. Kred -
 Fjerde gravitationsbølge detekteres, med europæisk hjælpEn del af Jomfru -detektoren i Italien, en af tre interferometre, der opsamlede en gravitationsbølge forårsaget af kollision af to sorte huller En fjerde gravitationsbølge er blevet opdaget-denn
Fjerde gravitationsbølge detekteres, med europæisk hjælpEn del af Jomfru -detektoren i Italien, en af tre interferometre, der opsamlede en gravitationsbølge forårsaget af kollision af to sorte huller En fjerde gravitationsbølge er blevet opdaget-denn -
 Mikroskopi plus AI er lig med hurtig COVID-19-detektion:undersøgelseGabriel Popescu, en professor i elektro- og computerteknik ved University of Illinois Urbana-Champaign, var en del af et team, der kombinerede mærkefri mikroskopisk billeddannelse med kunstig intellig
Mikroskopi plus AI er lig med hurtig COVID-19-detektion:undersøgelseGabriel Popescu, en professor i elektro- og computerteknik ved University of Illinois Urbana-Champaign, var en del af et team, der kombinerede mærkefri mikroskopisk billeddannelse med kunstig intellig
- Hvad mennesker vil have i en automatiseret bil
- Hvilke planter vokser i Det Indiske Ocean?
- Langsomme jordskælv i Cascadia er forudsigelige
- Skovbesøg i Schweiz ramt af lockdown af coronavirus
- Undersøgelse af de afgørende ladningsbæreroverførselsprocesser og dynamik inden for perovskite a…
- Virkninger af coronavirus -lockdowns:Ny undersøgelse indsamler data om forurenende stoffer i atmosf…


