Hvad er en styrke, der holder to atomer sammen?
* kovalente obligationer: Disse bindinger dannes, når to atomer deler elektroner. Denne deling skaber en stærk attraktion mellem atomerne og holder dem sammen. Kovalente bindinger er den stærkeste type kemisk binding.
* ioniske bindinger: Disse bindinger dannes, når et atom mister et elektron, og et andet atom får en elektron. Dette skaber en positiv og negativ ladning på atomerne, som derefter tiltrækker hinanden. Ioniske bindinger er typisk svagere end kovalente bindinger.
* Metalliske obligationer: Disse bindinger forekommer mellem metalatomer. Elektroner delokaliseres og kan bevæge sig frit gennem metallet. Dette skaber en stærk attraktion mellem atomerne, hvilket gør metaller stærke og ledende.
Den specifikke type binding, der dannes mellem to atomer, afhænger af de involverede atomer og deres elektronkonfigurationer.
 Varme artikler
Varme artikler
-
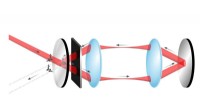 Fysikere udvikler en perfekt lysfældeLysfælden opsætningen er vist, bestående af et delvist gennemsigtigt spejl, en tynd, svag absorber, to konvergerende linser og et totalt reflekterende spejl. Normalt vil det meste af den indfaldende l
Fysikere udvikler en perfekt lysfældeLysfælden opsætningen er vist, bestående af et delvist gennemsigtigt spejl, en tynd, svag absorber, to konvergerende linser og et totalt reflekterende spejl. Normalt vil det meste af den indfaldende l -
 Gennembrud inden for kvantefotonik lover en ny æra inden for optiske kredsløbKredit:CC0 Public Domain Den moderne verden drives af elektriske kredsløb på en chip - halvlederchippen, der understøtter computere, mobiltelefoner, internettet, og andre applikationer. I år 2025,
Gennembrud inden for kvantefotonik lover en ny æra inden for optiske kredsløbKredit:CC0 Public Domain Den moderne verden drives af elektriske kredsløb på en chip - halvlederchippen, der understøtter computere, mobiltelefoner, internettet, og andre applikationer. I år 2025, -
 Måling af den fine strukturkonstant sætter tvivl om mørke fotonteorierPræcisionsmålinger af den fine strukturkonstant. En sammenligning af målinger. “0” på plottet er CODATA 2014 anbefalede værdi. De grønne punkter er fra fotonrekylforsøg; de røde er fra elektron g e
Måling af den fine strukturkonstant sætter tvivl om mørke fotonteorierPræcisionsmålinger af den fine strukturkonstant. En sammenligning af målinger. “0” på plottet er CODATA 2014 anbefalede værdi. De grønne punkter er fra fotonrekylforsøg; de røde er fra elektron g e -
 Universelle optotermiske mikro/nanoskala rotorerArbejdsmekanisme for lysdrevet rotation ud af planet af mikro/nanoskala rotorer. (A) Et forenklet skema, der illustrerer den eksperimentelle opsætning og drift for OTER af mikro/nanopartikler. (B) Arb
Universelle optotermiske mikro/nanoskala rotorerArbejdsmekanisme for lysdrevet rotation ud af planet af mikro/nanoskala rotorer. (A) Et forenklet skema, der illustrerer den eksperimentelle opsætning og drift for OTER af mikro/nanopartikler. (B) Arb
- Hvad gør Sroutum?
- T. rex havde et unikt fleksibelt kranium
- Nyt liv for Ukraines krigshærgede bjergobservatorium
- Den seneste opvarmning af Atlanterhavet uden fortilfælde i næsten 3, 000 år
- Første undersøgelse til at kombinere 3-D klimamodellering med kemi forfiner hvilke exoplaneter der…
- Hvorfor er det meste vand i atmosfæren usynligt?


