Har attraktive kræfter mindre hold på elektroner længere væk fra kernen?
* Coulombs lov: Tiltrækningskraften mellem ladede partikler (som kernen og elektronerne) er direkte proportional med produktet af deres ladninger og omvendt proportional med kvadratet i afstanden mellem dem.
* afskærmning: Indre elektroner "skjold" ydre elektroner fra kernenes fulde kraft. De indre elektroner skaber en negativ ladningssky, der delvist annullerer den positive ladning af kernen, hvilket reducerer den effektive atomladning, som ydre elektroner oplever.
Kortfattet:
* Afstand: Efterhånden som afstand øges, falder tiltrækningskraften markant (omvendt firkantet forhold).
* afskærmning: Tilstedeværelsen af indre elektroner svækker den attraktive kraft, der opleves af ydre elektroner.
Konsekvenser:
* ioniseringsenergi: Ydre elektroner er lettere at fjerne (lavere ioniseringsenergi), fordi de er mindre tæt holdt.
* Kemisk reaktivitet: Ydre elektroner er mere involveret i kemisk binding på grund af deres svagere tiltrækning til kernen.
* atomstørrelse: Atomer med flere elektronskaller (og derfor er elektroner længere væk fra kernen) større i størrelse.
Fortæl mig, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
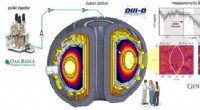 Brændstofindsprøjtning hjælper med at reducere magnetiske ø -ustabilitetVed at skyde pellets af frosset deuterium (en isotop af brint) i en fusionsreaktor, forskere ved DIII-D National Fusion Facility i San Diego har været i stand til at kontrollere ustabilitet i det magn
Brændstofindsprøjtning hjælper med at reducere magnetiske ø -ustabilitetVed at skyde pellets af frosset deuterium (en isotop af brint) i en fusionsreaktor, forskere ved DIII-D National Fusion Facility i San Diego har været i stand til at kontrollere ustabilitet i det magn -
 Nye simuleringer bekræfter effektiviteten af affaldsfjernelsesprocessen i plasmaenhedenKandidatstuderende Eugene Evans foran PPPLs feltvendte konfigurationsenhed. Kredit:Elle Starkman Ligesom ild producerer aske, Kombinationen af lette elementer i fusionsreaktioner kan producere m
Nye simuleringer bekræfter effektiviteten af affaldsfjernelsesprocessen i plasmaenhedenKandidatstuderende Eugene Evans foran PPPLs feltvendte konfigurationsenhed. Kredit:Elle Starkman Ligesom ild producerer aske, Kombinationen af lette elementer i fusionsreaktioner kan producere m -
 Fysikere finder måde at kontrollere detonationsbølgen i lovende ny type motorSkematisk af tredimensionel roterende detonationsmotor, der viser detonationsbølge. Kredit:D. Schwer et. al./49. AIAA Aerospace Sciences Meeting, herunder New Horizons Forum og Aerospace Exposition
Fysikere finder måde at kontrollere detonationsbølgen i lovende ny type motorSkematisk af tredimensionel roterende detonationsmotor, der viser detonationsbølge. Kredit:D. Schwer et. al./49. AIAA Aerospace Sciences Meeting, herunder New Horizons Forum og Aerospace Exposition -
 Ny varmemodel kan hjælpe elektroniske enheder med at holde længereEt plot af sammenligning af tre forskellige modeller for dislokation (defekt) tæthed versus termisk ledningsevne af fire populære galliumnitrid halvlederfremstillingsteknikker. Kredit:Can Bayram E
Ny varmemodel kan hjælpe elektroniske enheder med at holde længereEt plot af sammenligning af tre forskellige modeller for dislokation (defekt) tæthed versus termisk ledningsevne af fire populære galliumnitrid halvlederfremstillingsteknikker. Kredit:Can Bayram E
- Hvordan klimamønstre bidrager til koralblegning i Great Barrier Reef
- Krigen mod kvindelige trænere
- Forskere demonstrerer grundlæggende principper for nukleinsyreberegning inde i celler
- Hvad er elektroforese i kloning?
- Kun halvdelen af emballageaffaldet genanvendes – sådan gør du det bedre
- Dyrtilpasninger omkring vulkaner


