Aufbau-princippet:Forståelse af elektronorbitalfyldning
Elektroner fylder atomare orbitaler i rækkefølge efter stigende energi.
Dette betyder, at elektroner først vil besætte de laveste energi-orbitaler, der er tilgængelige, før de flytter til højere energi-orbitaler. Rækkefølgen af påfyldning bestemmes af (n + l) reglen , hvor:
* n er det vigtigste kvantetal (energiniveau)
* l er det azimutale kvantetal (subshell-type, f.eks. s, p, d, f)
Sådan fungerer det:
1. Beregn (n + l) for hver orbital. For eksempel, for 2p orbitalen, n =2 og l =1, så (n + l) =3.
2. Bestil orbitaler ved at øge (n + l) værdi.
3. Hvis to orbitaler har samme (n + l) værdi, udfyldes orbitalen med den laveste n-værdi først.
Eksempel:
* 1s (n + l =1)
* 2s (n + l =2)
* 2p (n + l =3)
* 3s (n + l =3)
* 3p (n + l =4)
* 4s (n + l =4)
* 3d (n + l =4)
* 4p (n + l =5)
* 5s (n + l =5)
* 4d (n + l =5)
* 5p (n + l =6)
* 6s (n + l =6)
* 4f (n + l =6)
Vigtige bemærkninger:
* Aufbau-princippet er en nyttig retningslinje til at forudsige elektronkonfigurationer, men det er ikke altid perfekt. Der er nogle undtagelser på grund af faktorer som elektron-elektron frastødning og stabiliteten af halvfyldte og fuldt udfyldte underskaller.
* Aufbau-princippet bruges hovedsageligt til at forstå den elektroniske struktur af atomer i deres grundtilstand (laveste energitilstand).
Ved at følge Aufbau-princippet kan vi forstå, hvordan elektroner er fordelt i et atoms orbitaler, og hvordan denne fordeling bestemmer atomets kemiske egenskaber.
Sidste artikelHvad er materie? Forstå masse og volumen
Næste artikelSpecifik gravitationsflasker (pyknometre):Form og funktion
 Varme artikler
Varme artikler
-
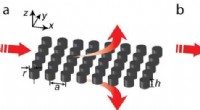 Mod applikationer:ultra-low-loss on-chip nulindeksmaterialeren, Nulindeks PhC-plade uden BICer. En fotonisk dipoltilstand, der danner nulindekset, resulterer i stråling uden for planet, dramatisk øget spredning af materialet. b, Nulindeks PhC-plade med en BIC.
Mod applikationer:ultra-low-loss on-chip nulindeksmaterialeren, Nulindeks PhC-plade uden BICer. En fotonisk dipoltilstand, der danner nulindekset, resulterer i stråling uden for planet, dramatisk øget spredning af materialet. b, Nulindeks PhC-plade med en BIC. -
 Dette nanoelektroniske gennembrud kan føre til mere effektive kvanteenhederKredit:Concordia University Forskere fra Concordia har lavet et gennembrud, der kan hjælpe dine elektroniske enheder til at blive endnu smartere. Deres resultater, som undersøger elektronadfærd i
Dette nanoelektroniske gennembrud kan føre til mere effektive kvanteenhederKredit:Concordia University Forskere fra Concordia har lavet et gennembrud, der kan hjælpe dine elektroniske enheder til at blive endnu smartere. Deres resultater, som undersøger elektronadfærd i -
 Ny forskning tilføjer Prandtls arbejde, far til moderne aerodynamikKonturvisualisering af blandet tilstand ustabilitet i Prandtl-modellen for en hældningsvinkel på 30 (grader). Flow er fra top til bund. Vortikale strukturer identificeres ved hjælp af Q-kriteriet. Kre
Ny forskning tilføjer Prandtls arbejde, far til moderne aerodynamikKonturvisualisering af blandet tilstand ustabilitet i Prandtl-modellen for en hældningsvinkel på 30 (grader). Flow er fra top til bund. Vortikale strukturer identificeres ved hjælp af Q-kriteriet. Kre -
 Magisk vinkel tre-lags grafen kan være en sjælden, magnetsikker superlederMIT fysikere har observeret tegn på en sjælden type superledning i et materiale kaldet magic-angle snoet trelags grafen. Kredit:Pablo Jarillo-Herrero, Yuan Cao, Jeong Min Park, et al MIT-fysikere
Magisk vinkel tre-lags grafen kan være en sjælden, magnetsikker superlederMIT fysikere har observeret tegn på en sjælden type superledning i et materiale kaldet magic-angle snoet trelags grafen. Kredit:Pablo Jarillo-Herrero, Yuan Cao, Jeong Min Park, et al MIT-fysikere
- Nanofiber-baserede sårbandager inducerer produktion af antimikrobielt peptid
- Hvilket jordlag består primært fast jern?
- Hvad bestemmer en syres styrke? En klar guide til protondissociation
- Hvilken type kraft findes, når to objekter har den samme ladning?
- Colombias caribiske juvel synker langsomt, efterhånden som havvandet stiger
- Hvilke kan du fysisk se genotyper eller fænotyper?


