Forståelse af kovalente bindinger:Hvordan ikke-metalatomer binder sig i molekyler
* Deling af elektroner: Ikke-metaller har en høj elektronegativitet, hvilket betyder, at de har en stærk tiltrækning af elektroner. Når ikke-metaller binder, deler de elektroner i stedet for at overføre dem (som i ionbindinger). Denne deling skaber et stabilt, afbalanceret arrangement af elektroner, der danner en kovalent binding.
* Stærk tiltrækning: De delte elektroner skaber en stærk tiltrækning mellem kernerne i de bundne atomer og holder dem sammen.
* Typer af kovalente bindinger: Kovalente bindinger kan yderligere kategoriseres som:
* Enkeltobligationer: Et par elektroner er delt mellem atomerne.
* Dobbeltobligationer: To par elektroner er delt mellem atomerne.
* Tredobbelt obligationer: Tre par elektroner er delt mellem atomerne.
Eksempler:
* Vand (H₂O): To brintatomer deler elektroner med et oxygenatom og danner to kovalente bindinger.
* Carbondioxid (CO₂): Et carbonatom deler to elektronpar med hvert oxygenatom og danner to dobbeltkovalente bindinger.
* Nitrogen (N₂): To nitrogenatomer deler tre par elektroner og danner en tredobbelt kovalent binding.
Nøglepunkt: Mens kovalente bindinger er den mest almindelige type binding mellem ikke-metalatomer, er der nogle undtagelser. For eksempel danner diatomiske molekyler som brom (Br₂) og iod (I₂) relativt svage kovalente bindinger.
 Varme artikler
Varme artikler
-
 Sikker, simpelt tilsætningsstof kan reducere agrokemisk forureningKredit:CC0 Public Domain Tilføjelse af en simpel polymer til gødning eller pesticider kan dramatisk reducere landbrugets forurening, foreslår en ny undersøgelse foretaget af forskere ved Universit
Sikker, simpelt tilsætningsstof kan reducere agrokemisk forureningKredit:CC0 Public Domain Tilføjelse af en simpel polymer til gødning eller pesticider kan dramatisk reducere landbrugets forurening, foreslår en ny undersøgelse foretaget af forskere ved Universit -
 Ansigtsmasker langsom spredning af COVID-19; typer masker, anvendelseslængdeVolumen af brøkdel af åndedrætsluft ved begyndelsen/inspirationstoppen og udløbet under ventilationshastighederne på både 7,5 liter pr. Minut (tilfælde I) og 15 liter i minuttet (tilfælde II). Farve
Ansigtsmasker langsom spredning af COVID-19; typer masker, anvendelseslængdeVolumen af brøkdel af åndedrætsluft ved begyndelsen/inspirationstoppen og udløbet under ventilationshastighederne på både 7,5 liter pr. Minut (tilfælde I) og 15 liter i minuttet (tilfælde II). Farve -
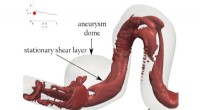 Aneurismenummer kan hjælpe kirurger med at træffe behandlingsbeslutningerDisse skemaer viser hvirvelringen versus det stationære forskydningslag i sidevæggens anatomiske aneurisme. Kredit:Hafez Asgharzadeh, Hossein Asadi, Hui Meng og Iman Borazjani Aneurismer dannes so
Aneurismenummer kan hjælpe kirurger med at træffe behandlingsbeslutningerDisse skemaer viser hvirvelringen versus det stationære forskydningslag i sidevæggens anatomiske aneurisme. Kredit:Hafez Asgharzadeh, Hossein Asadi, Hui Meng og Iman Borazjani Aneurismer dannes so -
 Unik polymerbaseret fremstillingsproces til lave omkostninger, højere udbytte omprogrammerbare foto…Kredit:Eindhoven University of Technology Fremtiden ser lys ud for fotoniske integrerede kredsløb (PICer), da de ser ud til at blive brugt i kvantecomputere og deep learning-teknologier. Da PICer
Unik polymerbaseret fremstillingsproces til lave omkostninger, højere udbytte omprogrammerbare foto…Kredit:Eindhoven University of Technology Fremtiden ser lys ud for fotoniske integrerede kredsløb (PICer), da de ser ud til at blive brugt i kvantecomputere og deep learning-teknologier. Da PICer
- Hvad er en Blue-Tailed Fly?
- Hvad er afstanden mellem identiske punkter på to bølger?
- Teleomerer er unødvendige i bakterier, fordi DNA'et er cirkulært?
- Hvilke to elementer komponerer phosphid?
- Brug mere på overgangsboliger, og teenagere i familiepleje er mindre tilbøjelige til at være hjem…
- Hvad er den mest kendte form for energi?


