Forståelse af elektronunderskalsformer:vinkelmoment-kvantetallet (l)
Her er en oversigt:
* Hovedkvantetal (n): Bestemmer elektronens energiniveau.
* Vinkelmomentum kvantetal (l): Bestemmer formen på elektronens orbital. Den kan have værdier fra 0 til n-1.
* l =0:s orbital (sfærisk)
* l =1:p orbital (håndvægt-formet)
* l =2:d orbital (mere komplekse former)
* l =3:f orbital (endnu mere komplekse former)
* Magnetisk kvantetal (ml): Bestemmer orienteringen af orbitalen i rummet.
* Spin kvantetal (ms): Beskriver det iboende vinkelmoment af en elektron, ofte omtalt som "spin".
Så for at bestemme formen på en elektronunderskal skal du se på værdien af vinkelmomentum kvantetal (l) .
 Varme artikler
Varme artikler
-
 Forskere finder en måde at pakke korn og medicin mest effektivt påDr. Mohammad Saadatfar fra ANU Research School of Physics and Engineering. Kredit:Stuart Hay, ANU Forskere har opdaget en måde at løse et problem, som har forvirret mennesker så længe, at det er
Forskere finder en måde at pakke korn og medicin mest effektivt påDr. Mohammad Saadatfar fra ANU Research School of Physics and Engineering. Kredit:Stuart Hay, ANU Forskere har opdaget en måde at løse et problem, som har forvirret mennesker så længe, at det er -
 Forskere måler og syntetiserer den musikalske akustik i en 5-strenget banjoDeering banjoen, et skematisk tværsnit af kroppen med hovedkomponenter tegnet tilnærmelsesvis efter målestok, og et nærbillede af broen. De hvide pletter på broen er reflekterende tape til laservibrom
Forskere måler og syntetiserer den musikalske akustik i en 5-strenget banjoDeering banjoen, et skematisk tværsnit af kroppen med hovedkomponenter tegnet tilnærmelsesvis efter målestok, og et nærbillede af broen. De hvide pletter på broen er reflekterende tape til laservibrom -
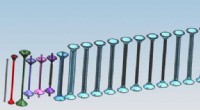 Målpraksis:Perfektion af Mu2e-produktionsmåletForskere udviklede mange iterationer af Mu2e-produktionsmålet, hvoraf nogle er vist her. Det første og enkleste design (yderst til venstre) er en wolframstang, mens det næstsidste design (yderst til h
Målpraksis:Perfektion af Mu2e-produktionsmåletForskere udviklede mange iterationer af Mu2e-produktionsmålet, hvoraf nogle er vist her. Det første og enkleste design (yderst til venstre) er en wolframstang, mens det næstsidste design (yderst til h -
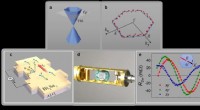 Ingeniører udvikler en ny metode til at løse spintekstur af topologiske overfladetilstande ved hjæ…Figur:(a) Skematisk diagram, der illustrerer Dirac-keglen af en topologisk isolator. (b) Spin-momentum låst overfladetilstand med sekskantet vridning. (c, d) Hallbar enhed af topologisk isolator Bi2
Ingeniører udvikler en ny metode til at løse spintekstur af topologiske overfladetilstande ved hjæ…Figur:(a) Skematisk diagram, der illustrerer Dirac-keglen af en topologisk isolator. (b) Spin-momentum låst overfladetilstand med sekskantet vridning. (c, d) Hallbar enhed af topologisk isolator Bi2
- Hvilke kulturmedier er specifikke for Staphylococcus aureus?
- Er der carbonatomer i en pickle?
- Stigende havniveauer sætter strandenge i Stillehavet i fare for at uddø, undersøgelse finder
- Uran skal erstatte plastik? Kemiens gennembrud kan bane vejen for nye materialer
- Hvad betyder eksperiment i et videnskabsmæssigt projekt?
- Mere præcis løsning til grænseoverskridende internetkøb


