Loven om bevarelse af masse:Hvordan det holder i hverdags- og nukleare processer
Guido Mieth/Getty Images
Et af de mest elegante begreber i fysik er hypotesen om "nul-energiunivers", som foreslår, at den samlede energi i kosmos balancerer til nul. Ifølge ideen, når du opsummerer massen-energien af hver planet, stjerne, molekyle og partikel - inklusive endda kolibrier - annulleres de positive og negative bidrag nøjagtigt. Selvom det praktisk talt er umuligt at måle universets totale masseenergi, er hypotesen i overensstemmelse med etablerede fysiske love og tilbyder en overbevisende ramme for kosmologi.
Bevarelsen af masse siger, at masse ikke kan skabes eller ødelægges. Gamle filosoffer bemærkede, at kemiske og fysiske processer blot omarrangerer stof, aldrig tilintetgør det. For eksempel producerer afbrænding af træ røg, aske og kuldioxid - alligevel forsvinder ingen masse. Selvom tidlige observationer var anekdotiske, vandt princippet videnskabeligt fodfæste i den moderne æra.
I 1789 demonstrerede Antoine Lavoisier, at massen af et lukket kemisk system forbliver konstant, uanset hvilken reaktion der finder sted. Hans omhyggelige eksperimenter etablerede loven om bevarelse af masse, som blev en hjørnesten i kemi. Årtier senere blev princippet forfinet for at anerkende, at masse og energi er udskiftelige, et synspunkt, der satte scenen for at forstå nukleare reaktioner.
Når bevarelsen af massen holder stik - og når den ikke gør det
Elnur/Shutterstock
I både fysiske og kemiske reaktioner forbliver det samlede antal atomer - og derfor systemets masse - uændret. Fysiske ændringer, såsom vand, der fryser til is, ændrer tilstanden, men ikke sammensætningen:et gram flydende vand og et gram is indeholder identiske atomer. Kemiske reaktioner omarrangerer atombindinger; selvom de kan producere gasser, lys eller forkullet, er det samlede atomantal bevaret. Den energi, der frigives eller absorberes, afspejler simpelthen de nye bindingsenergier.
Disse observationer fører til et fascinerende spørgsmål:gælder loven stadig, når den indre struktur af et atom ændres, som i nukleare processer?
Hvordan Einstein reddede bevarelsen af massen
Hulton Archive/Getty Images
Ved første øjekast synes nukleare reaktioner at krænke massebevaring, fordi massen af produkterne er lidt mindre end reaktanternes. Einsteins relativitetsteori løser dette tilsyneladende paradoks med den ikoniske ligning E=mc², som viser, at masse og energi er to aspekter af den samme virkelighed. Ved nuklear fission og fusion omdannes den "manglende" masse til energi, hvilket bevarer den samlede masse-energibalance.
Den første eksperimentelle bekræftelse kom i 1932, da Cockroft og Walton accelererede partikler for at udløse højenergiske nukleare reaktioner. De observerede, at massen tabt i reaktionen nøjagtigt matchede den frigivne energi, hvilket gav stærke beviser for masse-energi-ækvivalensen.
Den aktuelle tilstand af loven om bevarelse af masse
Cavan Images/Getty Images
Mens bevarelsen af masse forbliver et grundlæggende princip, kræver dets anvendelse i kernefysik den masse-energi-ramme, som Einstein introducerede. I hverdagen ser vi massekonservering i velkendte processer som forbrænding og fotosyntese.
Overvej at brænde træ:reaktionen forbruger ilt og producerer kuldioxid, vanddamp og aske. Alle de atomer, der er til stede ved starten, dukker op igen i produkterne; kun deres arrangementer ændres, og systemets masse forbliver den samme. Fotosyntese demonstrerer på samme måde massebevaring i større skala:planter omdanner atmosfærisk CO₂ til kulhydrater, mens de frigiver O₂. Når organismer indtager disse kulhydrater, vender kulstoffet tilbage til atmosfæren som CO₂ eller CH₄, hvilket fuldender en lukket cyklus, der bevarer massen.
I begge tilfælde udveksles energi med omgivelserne, men systemets samlede masse bevares, hvilket illustrerer princippets robusthed på tværs af skalaer.
 Varme artikler
Varme artikler
-
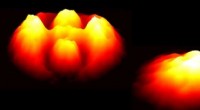 Forskere ser kvanteknob løsnePartikeltætheder relateret til forfaldet af kvanteknuden (til venstre), som overraskede forskere ved at binde sig selv efter et par mikrosekunder og til sidst blive til spin -hvirvelen (til højre). Kr
Forskere ser kvanteknob løsnePartikeltætheder relateret til forfaldet af kvanteknuden (til venstre), som overraskede forskere ved at binde sig selv efter et par mikrosekunder og til sidst blive til spin -hvirvelen (til højre). Kr -
 Forskere udvikler en ny metode til at detektere kernedannelseArray1 (a) umiddelbart efter generation, bundlinje (linje 9) er den senest genererede, 527 μDs med indledende dråberadius på 25,1 μm ± 0,8 (for linje 9), med et volumen på 60,7pL under forudsætning af
Forskere udvikler en ny metode til at detektere kernedannelseArray1 (a) umiddelbart efter generation, bundlinje (linje 9) er den senest genererede, 527 μDs med indledende dråberadius på 25,1 μm ± 0,8 (for linje 9), med et volumen på 60,7pL under forudsætning af -
 Udskæring af diamanter til optiske komponenterKredit:Ecole Polytechnique Federale de Lausanne Takket være en ny teknik udviklet på EPFL, optiske diffraktionsgitre kan nu laves af ren diamant, med deres overflader glattet ned til det allersids
Udskæring af diamanter til optiske komponenterKredit:Ecole Polytechnique Federale de Lausanne Takket være en ny teknik udviklet på EPFL, optiske diffraktionsgitre kan nu laves af ren diamant, med deres overflader glattet ned til det allersids -
 Nye spor om et uhåndgribeligt materiale:En superleder, der kan syntetiseres i laboratorietKredit:Alchemist-hp Titaniummonoxid (TiO), en uorganisk kemisk forbindelse, er et materiale, der har unddraget sig nærmere undersøgelser af fysikere på grund af mangel på enkeltkrystalprøver med h
Nye spor om et uhåndgribeligt materiale:En superleder, der kan syntetiseres i laboratorietKredit:Alchemist-hp Titaniummonoxid (TiO), en uorganisk kemisk forbindelse, er et materiale, der har unddraget sig nærmere undersøgelser af fysikere på grund af mangel på enkeltkrystalprøver med h
- Hvilken effektkraft kan have på et objekts bevægelse. Giv eksempel hver, du skriver?
- Hvilke typer sten skal du lave en brand?
- Klimaændringer overladede en varmekuppel, hvilket intensiverede 2021-brandsæsonen, viser undersøg…
- Loopende fodtrinsmønster i moderne perlehøns kaster lys over dinosaurus spor
- Vil du forbedre virksomhedens ydeevne? Få flere kvinder i bestyrelseslokalet
- How does the movement of air molecules cause pressure?


