At omdanne vand til brint mere effektivt

Kredit:Leiden Universitet
Forskere har længe været forundret over, hvorfor det er lettere at producere brint fra vand i et surt miljø end i et alkalisk miljø. Marc Koper kommer med en forklaring:Årsagen er det elektriske felt ved overfladen af katalysatoren, som er større i et alkalisk miljø, som han skriver i en publikation i Naturenergi den 20. marts.
At producere brint mere effektivt
Marc Koper er professor i katalyse og overfladekemi og forsker i bæredygtig energi, såsom brugen af brint som brændstof. "Brint er en ren energikilde, som vi endnu ikke kan lave på en ren måde i stor skala. Fordi vi nu ved, at det elektriske felt spiller en vigtig rolle, vi er bedre i stand til at finjustere nuværende systemer for at gøre dem mere effektive, «siger Koper.
At elektrokemisk omdanne vand til brint og ilt, elektroder er nødvendige:en negativ katode og en positiv anode. "Katoden er, hvor der produceres brint. Til dette, platin er den bedste katalysator, i hvert fald i et surt miljø. Til anoden, hvor ilt dannes, iridium er den bedste katalysator. Og det er det sjældneste metal på jorden. "
Billig nikkel
"I et alkalisk miljø kan du bruge nikkel i stedet for iridium, hvilket er meget billigere. Imidlertid, produktionen af brint er meget sværere i et alkalisk miljø end i et surt miljø. Katoden kræver en højere spænding for at producere brint, hvilket gør hele processen mindre effektiv."
Svømning i et elektrisk felt
Marc Koper og hans gruppe havde mistanke om, at styrken af det elektriske felt spiller en rolle i reaktionshastigheden. "I et surt miljø, der er et svagere elektrisk felt ved platinelektroden ved en given spænding end i et alkalisk miljø. Et stærkt elektrisk felt gør, at vandmolekylerne nærmest er "frosne". Ladede partikler såsom protoner og hydroxidioner har få problemer med at bevæge sig, når vandmolekylerne let bevæger sig. Men i et alkalisk miljø er det elektriske felt stærkt, resulterer i vandmolekyler, der ikke kan bevæge sig, når en ladet partikel skal passere. For disse partikler, det er sværere at nå platinelektroden. Det er grunden til, at reaktionen er langsommere end i et surt miljø, " Koper illustrerer sin teori.
Vi spurgte os selv:hvordan måler man et elektrisk felt nær overfladen af elektroden?" Koper siger. "Kolleger ved universitetet i Alicante i Spanien udviklede en særlig metode til at måle dette felt, så vores ph.d. Isis Ledezma-Yanez besøgte dem. Målingerne stemte overens med vores model. Næste, vi vil teste, om modellen også er korrekt med andre katalysatorer end platin."
Desuden, denne forskning tilbyder Koper en ny måde at forbedre systemer, der producerer brint ud af vand. "Inden denne undersøgelse, vi fokuserede kun på katalysatorens bindingsenergi med brint. Dette må ikke være for stærkt, men den skal heller ikke være for svag. Vi ved nu, at styrken af det elektriske felt også spiller en vigtig rolle. Vi vil udføre yderligere eksperimenter for at teste dette, for eksempel ved at variere sammensætningen af opløsningen.
Den måde, hvorpå hydrogen dannes, er anderledes i et surt miljø sammenlignet med et alkalisk miljø.
Surt miljø
En proton (en partikel med en positiv ladning) bevæger sig gennem vandopløsningen mod platinoverfladen og binder sig til platinet som et hydrogenatom.
To hydrogenatomer, der er bundet ved overfladen, bindes sammen og danner brint.
Alkalisk miljø
Vand reagerer på platinoverfladen, hvilket resulterer i et hydrogenatom bundet til platin og en negativt ladet hydroxidion (OH - ).
Hydroxidionen bevæger sig mod vandopløsningen væk fra platinoverfladen. På grund af det stærke elektriske felt og det tilsvarende 'frosne' vand, dette trin er langsomt.
Sidste artikelOprettelse af materialer på en ny måde ved hjælp af 3D-trykbakterier
Næste artikelTransport af molekylære motorer til cilia
 Varme artikler
Varme artikler
-
 Tube orm slim viser langtidsholdbar, selvdrevet glødFotografiet til venstre viser den marine pergamentrørorm (Chaetopterus sp.) under naturligt lys. Ormen er krøllet sammen, stikker halen under hovedet. Billedet til højre viser den samme orm, men i mør
Tube orm slim viser langtidsholdbar, selvdrevet glødFotografiet til venstre viser den marine pergamentrørorm (Chaetopterus sp.) under naturligt lys. Ormen er krøllet sammen, stikker halen under hovedet. Billedet til højre viser den samme orm, men i mør -
 Undersøgelse afslører en simpel kemisk proces, der kan have ført til livets oprindelse på JordenEt vådt-tørt scenarie i en præbiotisk varm kilde eller tidevandspool. A) viser poolen med de fem slags alfa-hydroxysyrer, der blev brugt i denne undersøgelse. B) viser tørrebassinet, hvor et bibliotek
Undersøgelse afslører en simpel kemisk proces, der kan have ført til livets oprindelse på JordenEt vådt-tørt scenarie i en præbiotisk varm kilde eller tidevandspool. A) viser poolen med de fem slags alfa-hydroxysyrer, der blev brugt i denne undersøgelse. B) viser tørrebassinet, hvor et bibliotek -
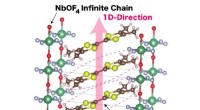 Forskere opdager ny organisk lederKrystalstruktur af en-dimensionel ladningsoverføringssalt med en uendelig anionkæde (TMTTF) (NbOF 4 ) Kredit:NINS/IMS Salte er langt mere komplicerede end fødevarekrydderiet - de kan endda funge
Forskere opdager ny organisk lederKrystalstruktur af en-dimensionel ladningsoverføringssalt med en uendelig anionkæde (TMTTF) (NbOF 4 ) Kredit:NINS/IMS Salte er langt mere komplicerede end fødevarekrydderiet - de kan endda funge -
 Hvilke elementer udgør bagningssoda?Bagepulver, også kaldet natriumbicarbonat, er en almindelig bagebestanddel, renser, deodorizer og pH-regulator. Det sælges ofte som et hvidt pulver, der ligner bagepulver. I modsætning til bagepulv
Hvilke elementer udgør bagningssoda?Bagepulver, også kaldet natriumbicarbonat, er en almindelig bagebestanddel, renser, deodorizer og pH-regulator. Det sælges ofte som et hvidt pulver, der ligner bagepulver. I modsætning til bagepulv
- Sådan konverteres SCFM til NM3
- Strømstyring i dalen viser vej til enheder med meget lav strøm
- MtGox bitcoin-baron får betinget dom for datamanipulation
- I stressede økosystemer vendte jura-dinosaurerne sig til oprydning, måske endda kannibalisme
- Anvendelse af vedvarende energikilder
- Gør social forandringsindsats mere effektiv


