Forskere finjusterer systemet for at skabe syngas fra CO2
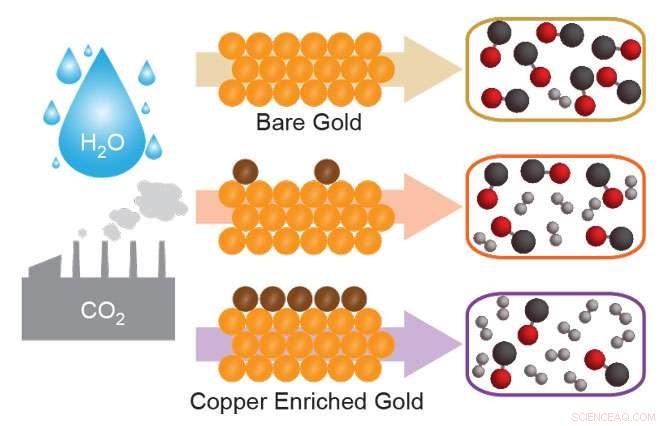
Skematisk skildring af produktionen af syngas fra kuldioxid og vand. Bare guldkatalysatorer fremstiller syngasblandinger, der er rige på carbonmonoxid, hvorimod guldkatalysatorer beriget med kobber laver syngasblandinger, der er mere brintrige. Kredit:Michael Ross/Berkeley Lab
Forskere har udviklet en ny opskrift til fremstilling af syntesegasblandinger, eller syngas, det involverer at tilføje en knivspids kobberatomer drysset oven på en guldoverflade. Det nye materiale understøtter en elektrokemisk reaktion ved stuetemperatur, der kan omdanne kuldioxid og vand til syngas, en blanding af kulilte og brint, og en vigtig forløber i produktionen af kemikalier og syntetiske brændstoffer.
Forskerne siger, at syngas kan omdannes nedstrøms til små molekyler, som ethanol, eller større kulbrinter, som dem i benzin, ved gæring eller termokemi. At designe et materiale og en proces, der nemt kan kontrollere sammensætningen af syngas, ville være en vigtig forbedring med hensyn til at reducere miljøpåvirkningerne af disse industrielle processer.
De beskriver deres design i et papir for nylig offentliggjort i Journal of the American Chemical Society . Undersøgelsen blev ledet af Peidong Yang, senior fakultetsforsker ved Department of Energy's Lawrence Berkeley National Laboratory (Berkeley Lab) Materials Sciences Division, og Edward Sargent, professor ved University of Toronto's Department of Electrical and Computer Engineering.
"Vi kender ingen anden enkelt elektrokatalysator, der kombinerer høje produktionshastigheder med en så omfattende kontrol af syngassammensætning, " sagde Yang, som også er professor i kemi ved University of California, Berkeley. "Mange processer, der bruger syngas, kræver forskellige sammensætninger af gas, så vi ønskede at skabe en familie af elektrokatalysatorer, der let kan justeres."

Der er vist et scanningselektronmikroskopbillede af nanostrukturerede syngaskatalysatorer. Kredit:Michael Ross/Berkeley Lab
Forskerne fandt ud af, at de kunne kontrollere mængden af kulilte og brint, der genereres af elektrokatalysatoren, ved at justere mængden af kobberatomer lagt på en nanostruktureret guldoverflade.
"Kobberet ændrer styrken, hvormed CO2 binder sig til overfladen, " sagde studielederforfatter Michael Ross, en postdoc-forsker i Yangs laboratorium. "En nanostruktureret overflade, der primært er guld, giver for det meste kulilte. For at fremstille en blanding, der er mere brintrig, vi tilføjer mere kobber."
Forskerne brugte røntgenfotoelektronspektroskopiteknikker ved Berkeley Labs Molecular Foundry til at kvantificere mængden af kobber på guldelektrokatalysatoren, der er nødvendig for at skabe forskellige syngasblandinger. For eksempel, et 1-atom-tykt lag af kobber, der dækker guldoverfladen, kan producere en 2-til-1 blanding af brint til carbonmonoxid. Når guldet efterlades uforfalsket, hydrogen-til-carbonmonoxid-blandingen er 1-til-10, demonstrerer bred fleksibilitet i syngas output.
"Hvis disse elektrokatalysatorer kunne skaleres op til at fungere i industrielle reaktorer, vi kunne lave syngas ved hjælp af vedvarende produceret elektricitet og CO2, " sagde Ross. "Syngas bliver i øjeblikket omdannet til methanol, dieselbrændstof, og andre nyttige kemikalier over hele verden. Dette kan gøre produktionen af disse kemikalier meget mere bæredygtig."
 Varme artikler
Varme artikler
-
 Pig-Pen-effekt:Blanding af hudolie og ozon kan producere en personlig forureningsskyNår ozon rammer olier på huden og i snavset tøj, det kan producere en personlig sky af irriterende stoffer. Kredit:Penn State Når ozon og hudolier mødes, den resulterende reaktion kan hjælpe med a
Pig-Pen-effekt:Blanding af hudolie og ozon kan producere en personlig forureningsskyNår ozon rammer olier på huden og i snavset tøj, det kan producere en personlig sky af irriterende stoffer. Kredit:Penn State Når ozon og hudolier mødes, den resulterende reaktion kan hjælpe med a -
 Video:Hvorfor flamingoer er sejere, end du trorKredit:The American Chemical Society For mange mennesker, flamingoer er synonyme med Florida, tarvelige plænepynt og cocktails på stranden. Men deres tåbelige ry modsiger deres utrolige overlevels
Video:Hvorfor flamingoer er sejere, end du trorKredit:The American Chemical Society For mange mennesker, flamingoer er synonyme med Florida, tarvelige plænepynt og cocktails på stranden. Men deres tåbelige ry modsiger deres utrolige overlevels -
 Ny immunterapiteknik kan specifikt målrette tumorceller, undersøgelsesrapporterDenne teknologi er særligt spændende, fordi den afmonterer store udfordringer inden for kræftbehandlinger, ” siger Weian Zhao. Kredit:Steve Zylius / UCI En ny immunterapi screening prototype udvik
Ny immunterapiteknik kan specifikt målrette tumorceller, undersøgelsesrapporterDenne teknologi er særligt spændende, fordi den afmonterer store udfordringer inden for kræftbehandlinger, ” siger Weian Zhao. Kredit:Steve Zylius / UCI En ny immunterapi screening prototype udvik -
 Forskere opfinder håndholdt enhed til hurtig overvågning af drikkevandskvalitetenNTU -forskere udviklede en bærbar enhed, inspireret af menneskekroppens evne, at opdage spor af tungmetaller i drikkevand på bare fem minutter. L-R:Assoc Prof Yong Ken-Tye og hans ph.d.-studerende Ste
Forskere opfinder håndholdt enhed til hurtig overvågning af drikkevandskvalitetenNTU -forskere udviklede en bærbar enhed, inspireret af menneskekroppens evne, at opdage spor af tungmetaller i drikkevand på bare fem minutter. L-R:Assoc Prof Yong Ken-Tye og hans ph.d.-studerende Ste
- En livreddende grund til at have flere kvinder i bestyrelser:at sikre forbrugernes sikkerhed
- At gøre en sag for at returnere luftskibe til skyerne
- Hvad er sulfat?
- Monsanto CEO og andre til at forlade efter Bayer-overtagelsen
- Følsom ny test påviser antistoffer mod SARS-CoV-2 på kun 10 minutter
- Forskere opdager nyt anti-cancer molekyle


