Udvikling af nyt protein kan føre til nye behandlingsmuligheder for kræft, fødselsdefekt
Forskere har konstrueret et kunstigt protein, der kan blokere kræftcellers ondartede egenskaber samt korrigere visse fødselsdefekter.
Fundene, som står i journalen Proceedings of the National Academy of Sciences , kan føre til identifikation af nye molekylære mål, der er egnede til terapeutisk intervention.
Celler i den menneskelige krop skal kommunikere med hinanden for at fungere korrekt. Dette opnås ved en molekylær mekanisme kaldet signaltransduktion, og dens dysregulering fører til menneskelig sygdom. En gruppe molekyler kaldet G-proteiner fungerer som en signalmekanisme, der sætter celler i stand til at ændre deres adfærd, når de aktiveres af overfladereceptorer.
Ifølge forskerne, G-proteinerne kan aktiveres via alternative mekanismer uafhængigt af overfladereceptorer, som også påvirker normal celleadfærd og patogenese. Desværre, der er ingen effektive værktøjer til at undersøge disse alternative G-proteinaktivatorer og lære, hvordan man tackler deres afvigende adfærd ved sygdom, indtil nu.
"Vi har konstrueret et kunstigt protein, der, når det udtrykkes i celler, specifikt kan sløve receptoruafhængig G-proteinaktivering og efterfølgende ændringer i celleadfærd. Vi implementerede dette for at blokere kræftcellers ondartede egenskaber og for at korrigere fødselsdefekter forbundet med den afvigende dysregulering af cellulære celler. meddelelse, " forklarede den tilsvarende forfatter Mikel Garcia-Marcos, PhD, lektor i biokemi ved Boston University School of Medicine (BUSM).
Forskerne startede med et naturligt G-protein, fjernet nogle dele og ændret nogle andre for at skabe et nyt protein, der binder meget tæt til en familie af G-proteinaktivatorer, mens det mister evnen til at binde sig til enhver anden kendt partner. Ved at bruge denne tilgang skabte de et protein, der specifikt hæmmer en familie af G-proteinaktivatorer uden at påvirke nogen anden komponent i det cellulære maskineri. Derefter introducerede de det i kræftceller og observerede, at det kan forhindre deres ondartede egenskaber ved selektivt at hæmme G-proteinaktivatorer. Tilsvarende da de introducerede det konstruerede protein i en eksperimentel model, det sløvede udviklingsdefekter induceret af en G-proteinaktivator.
"Vores resultater giver et principbevis for at målrette mod en ny familie af G-proteinregulatorer, som er kendt for at bidrage til udviklingen af kræft og forekomsten af fødselsdefekter.
Selvom de kliniske implikationer for denne opdagelse er indirekte - da det konstruerede protein ikke kan leveres til patienter - repræsenterer det et betydeligt fremskridt i identifikationen af en ny klasse af molekylære mål i cancer eller neonatale misdannelser," sagde Garcia-Marcos.
 Varme artikler
Varme artikler
-
 Bæredygtig separationsteknologi gør nye applikationer muligeKredit:Hollandsk Organisation for Videnskabelig Forskning (NWO) Membraner er meget brugt til at adskille stoffer fra hinanden, fx ved vandbehandling eller nyredialyse. Membranteknologi sparer ener
Bæredygtig separationsteknologi gør nye applikationer muligeKredit:Hollandsk Organisation for Videnskabelig Forskning (NWO) Membraner er meget brugt til at adskille stoffer fra hinanden, fx ved vandbehandling eller nyredialyse. Membranteknologi sparer ener -
 Hvad er funktionerne ved kulhydratanhydrase?Kulhydridanhydrase er et afgørende enzym, der fungerer i dyreceller, planteceller og i miljøet for at stabilisere kuldioxidkoncentrationer. Uden dette enzym ville omdannelsen fra kuldioxid til bicarbo
Hvad er funktionerne ved kulhydratanhydrase?Kulhydridanhydrase er et afgørende enzym, der fungerer i dyreceller, planteceller og i miljøet for at stabilisere kuldioxidkoncentrationer. Uden dette enzym ville omdannelsen fra kuldioxid til bicarbo -
 En ny måde at direkte omdanne metan til methanol ved hjælp af guld-palladium nanopartiklerRepræsentative HAADF-billeder og partikelstørrelsesfordelinger for den ikke-understøttede AuPd-PVP-sol i frisk (A til C) og efter en CH4-oxidationsreaktion (D til F). Kredit:Graham J. Hutchings og Chr
En ny måde at direkte omdanne metan til methanol ved hjælp af guld-palladium nanopartiklerRepræsentative HAADF-billeder og partikelstørrelsesfordelinger for den ikke-understøttede AuPd-PVP-sol i frisk (A til C) og efter en CH4-oxidationsreaktion (D til F). Kredit:Graham J. Hutchings og Chr -
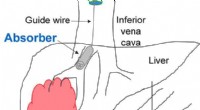 Lægemiddelsvamp kan minimere bivirkninger af kræftbehandlingForeslået tilgang til lægemiddelfangst ved hjælp af en 3D-printet absorber til endovaskulær behandling af leverkræft. Kemoterapimedicinen administreres intra-arterielt via leverarterien (bunden). Over
Lægemiddelsvamp kan minimere bivirkninger af kræftbehandlingForeslået tilgang til lægemiddelfangst ved hjælp af en 3D-printet absorber til endovaskulær behandling af leverkræft. Kemoterapimedicinen administreres intra-arterielt via leverarterien (bunden). Over
- Sprudlende rent vand fra nanodiamant-indlejrede membranfiltre
- Forskellige størrelser af Railroad Spikes
- Overtrumfer det politiske parti ideologi?
- Rumfartøj åbner nytår med forbiflyvning på solsystemets kant (opdatering)
- Fodgængere:En tobenet robot, der tilpasser sin gangstil som reaktion på miljøændringer
- Engager studerende på afstand med et escape room-spil


