Hydrogengas fra enzymproduktion
Forskere ved Freie Universität Berlin og Ruhr-Universität Bochum har afdækket et afgørende reaktionsprincip for brintproducerende enzymer. Team ledet af Dr. Ulf-Peter Apfel i Bochum og Dr. Sven T. Stripp ved Freie Universität undersøgte produktionen af molekylært brint i encellede grønne alger. De var i stand til at demonstrere, hvordan enzymet lykkes i at overføre to elektroner i træk til to hydrogenioner og derved antage stabile mellemliggende tilstande. Hydrogengas betragtes som fremtidens energikilde. Dermed, der er stor industriel interesse i at belyse mekanismen for biologisk produktion. Resultaterne blev offentliggjort i det seneste nummer af tidsskriftet Angewandte Chemie .
I den levende natur finder en række kemiske reaktioner sted meget langsomt. Anvendelsen af enzymer øger sandsynligheden eller hastigheden for en reaktion (katalyse). Ofte spiller levering og fjernelse af elektroner også en rolle - dette kaldes reduktion og oxidation. Særlige enzymer, hydrogenaser, fremskynde omdannelsen af hydrogenioner (protoner) til hydrogengas med høj effektivitet. De absorberer overskydende elektroner, der genereres under fotosyntesen og frigiver hydrogengas som et biprodukt. Denne proces kan beskrives som en reduktion af to protoner med to elektroner, hvorved reaktionen finder sted i flere trin.
"Efter at have modtaget en første elektron, et enzym er typisk mindre tilbøjeligt til at acceptere et andet, "understreger Dr. Sven Stripp. På trods af dette, to elektroner kan overføres til to protoner. Ved hjælp af syntetiske hydrogenaseenzymer, avanceret infrarød spektroskopi, og elektrokemiske metoder, forskerne undersøgte, hvordan dette er muligt. De demonstrerede, at optagelsen af en elektron i enzymets katalytiske centrum er koblet med bindingen af en proton. Protonens positive ladning kompenserer for elektronens negative ladning. I kemi er denne proces kendt som protonkoblet elektronoverførsel (PCET). "Dermed, den anden elektron kan overføres med tilsvarende sandsynlighed som den første, "siger Dr. Ulf-Peter Apfel.
Ifølge forfatterne, denne observation har stor relevans for at forstå den katalytiske mekanisme for hydrogenaser og for design af syntetiske komplekser til produktion af hydrogengas. Ud over, forskerne spekulerer i, at PCET -processer også kunne forklare optagelsen af flere elektroner i andre enzymer, fordi mange af disse makromolekyler bærer katalytiske centre af jern og svovlatomer, svarende til hydrogenases.
Sidste artikelDet er et spørgsmål om gradienter
Næste artikelStressede kakaotræer kan producere mere smagfuld chokolade
 Varme artikler
Varme artikler
-
 Blyfri magnetiske perovskitterKredit:CC0 Public Domain Forskere ved Linköpings Universitet, Sverige, arbejder med perovskite-materialefamilien, har udviklet en optoelektronisk magnetisk dobbeltperovskit. Opdagelsen åbner mulig
Blyfri magnetiske perovskitterKredit:CC0 Public Domain Forskere ved Linköpings Universitet, Sverige, arbejder med perovskite-materialefamilien, har udviklet en optoelektronisk magnetisk dobbeltperovskit. Opdagelsen åbner mulig -
 Opbygning af en bedre biosensorpolymerFlere kritiske udfordringer blev overvundet for at udvikle den nye type polymer, der har et stort potentiale for næste generations biosensorer. Kredit:KAUST; Xavier Pita Der er udviklet et nyt org
Opbygning af en bedre biosensorpolymerFlere kritiske udfordringer blev overvundet for at udvikle den nye type polymer, der har et stort potentiale for næste generations biosensorer. Kredit:KAUST; Xavier Pita Der er udviklet et nyt org -
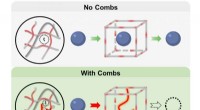 Hydrogeler med fintandet molekylærkam kan lave vedvarende glukoseovervågningsimplantaterKamlignende molekyler i hydrogelens masker forhindrer små molekyler, ligesom glukosefølende assays, fra at lække ud. Kredit:Dr. Melissa Grunlan/Texas A&M University College of Engineering I en ny
Hydrogeler med fintandet molekylærkam kan lave vedvarende glukoseovervågningsimplantaterKamlignende molekyler i hydrogelens masker forhindrer små molekyler, ligesom glukosefølende assays, fra at lække ud. Kredit:Dr. Melissa Grunlan/Texas A&M University College of Engineering I en ny -
 Hvorfor bruges magnesiumklorid i PCR?Når en efterforsker eller en læge får en DNA-prøve, er der ofte ikke nok DNA til rådighed til korrekt analyse. For at simulere kroppens egen DNA-replikationsproces udviklede forskere en proces kald
Hvorfor bruges magnesiumklorid i PCR?Når en efterforsker eller en læge får en DNA-prøve, er der ofte ikke nok DNA til rådighed til korrekt analyse. For at simulere kroppens egen DNA-replikationsproces udviklede forskere en proces kald
- Forskere skaber sammenfiltrede fotoner 100 gange mere effektivt end tidligere muligt
- Lava flyder fra den filippinske vulkan, tusinder evakueret
- Nanofotonikorkestret præsenterer:Vridning til lyset af nanopartikler
- At afsløre hykleri kan effektivt reducere muslimernes kollektive skyld for individuelle voldelige h…
- Kulstof viser kvanteeffekter
- C-vitamin i kroppen kan spores ved fluorescens


