Hydrogeler med fintandet molekylærkam kan lave vedvarende glukoseovervågningsimplantater
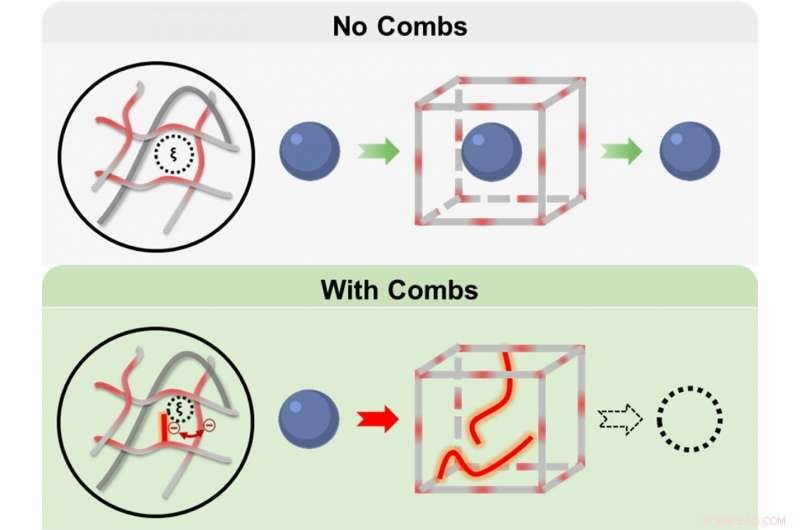
Kamlignende molekyler i hydrogelens masker forhindrer små molekyler, ligesom glukosefølende assays, fra at lække ud. Kredit:Dr. Melissa Grunlan/Texas A&M University College of Engineering
I en ny undersøgelse, offentliggjort online i tidsskriftet American Chemical Society (ACS) Anvendte polymermaterialer , forskere ved Texas A&M University rapporterede, at de har designet en hydrogelmembran, der kan bruges til at rumme optiske glukosemåling materialer, mod opbygning af en biosensor til overvågning af sukkerniveauer hos diabetikere.
Ved at inkorporere dinglende, kam-type molekylære kæder inden for en type hydrogel kaldet poly (N-isopropylacrylamid) eller poly NIPAAm for kort, de viste, at membranen kunne forhindre lækage af små molekyler, som dem til glukosemåling, samtidig med at glukose stadig kan diffundere ind og ud.
Når den er klar til klinisk brug, forskerne sagde, at disse membraner kunne bruges til at danne biosensorer, der let kunne implanteres under håndleddet og kunne tilbyde et mere behageligt alternativ til transdermale implantater, som sidder delvist uden for huden. I øvrigt, i modsætning til transdermale implantater, der skal udskiftes hvert par uger, Denne type subkutant implantat skal muligvis kun udskiftes hvert par måneder.
"Vi har udført et stort arbejde med hydrogelmaterialer, der kigger på mekaniske egenskaber og reaktioner fra fremmedlegemer, men vores store mål har altid været at bruge poly NIPAAm membraner til at bygge en subkutan glukose biosensor, "sagde Dr. Melissa Grunlan, professor og indehaver af Charles H. og Bettye Barclay -professoratet i Institut for Biomedicinsk Teknik. "I dette studie, vi har været i stand til at finjustere diffusionsegenskaberne for disse hydrogeler, som vi tidligere har identificeret som en lovende kandidat til at opbygge langsigtede glukosebiosensorer. "
Poly NIPAAms er en klasse af organiske hydrogeler, der har en blød tekstur, som kontaktlinser. En af deres attraktive egenskaber er, at de kan undergå cyklisk hævelse og nedsvulning med små temperatursvingninger i kroppen. Da deres overflade dynamisk ændrer sig med temperaturen, de afskrækker vedhæftningen af celler og biomolekyler. Denne aktive, Selvrensende mekanisme gør poly NIPAAm-hydrogeler tiltalende for implantater, da de minimerer angrebet fra immunsystemet.
For at bruge poly NIPAAm -membranen til overvågning af blodsukker, den skal indeholde nok glukosefølende molekyler eller assays. Desuden, Hydrogelens levetid afhænger også af membranens evne til at fastholde disse assaymolekyler uden at de lækker ud.
"Tænk på NIPAAm -hydrogelen som en strikket sweater, hvor mellemrummene mellem maskerne dannes af krydsestingene. Lige nu, disse rum eller vinduer i hydrogelerne er for store, lad analysemolekylerne gå lige igennem, "sagde Grunlan." Hvis analyserne bliver ved med at udvaskes på denne måde, vi kommer ikke til at have en længe fungerende sensor. "
Derfor, Grunlan og hendes team fokuserede deres bestræbelser på at finjustere egenskaberne af poly NIPAAms for at begrænse lækage af glukosefølende molekyler, samtidig med at glukosen stadig kunne diffundere gennem hydrogel.
For at reducere størrelsen på huller, forskerne indsatte dinglende molekyler af forskellige ladninger, længder og koncentrationer til poly NIPAAm hydrogel. Når den er inkorporeret i hydrogel, disse molekyler skaber kamformede barrierer, hvis tænder er designet til at blokere diffusion af små assaystørrelsesmolekyler. For at teste, om denne kamlignende arkitektur kan begrænse diffusion af glukosesensorer, de lægger også i hydrogel, fluorescensmærkede molekyler kaldet dextrans, som tjente som fuldmagter for glukosefølende molekyler. Næste, de placerede hydrogel i vand og målte mængden af fluorescens i vandet på grund af lækage af dextraner fra hydrogel.
Forskerne fandt ud af, at når de brugte et negativt ladet molekyle kaldet poly (2-acrylamido-2-methyl-1-propansulfonsyre) eller PAMP, kamme forhindrede diffusion af dextraner. Desuden, de observerede også, at glukosemolekyler var uhindret i deres strømning ind og ud af hydrogel.
Grunlan bemærkede, at nu hvor de har bevis på, at deres hydrogeler kan bremse lækage af små dextraner, det næste trin i deres forskning ville være at bygge en biosensor med glukosefølende molekyler indeholdt i membranen.
"Selvom vores nuværende undersøgelse ikke involverede egentlige sansemolekyler, det viser meget endegyldigt og præcist, hvad kamarkitekturer kan gøre for hydrogeler for at begrænse diffusion, "sagde Grunlan." Dette var en systematisk undersøgelse for at vise effektiviteten af vores tilgang og muligheden for at udvide vores fund til andre forskningsområder end glukosemåling, som hydrogeler med begrænset diffusion skal designes til. "
 Varme artikler
Varme artikler
-
 Lægemiddelbibliotekar opdager en ny forbindelse, der kan modvirke almindelig kirurgisk komplikationRapadocin -molekyle. Kredit:Liu laboratorium I en strategisk søgning, Johns Hopkins -forskere oprettede og screenede et bibliotek med 45, 000 nye forbindelser, der indeholder kemiske elementer af
Lægemiddelbibliotekar opdager en ny forbindelse, der kan modvirke almindelig kirurgisk komplikationRapadocin -molekyle. Kredit:Liu laboratorium I en strategisk søgning, Johns Hopkins -forskere oprettede og screenede et bibliotek med 45, 000 nye forbindelser, der indeholder kemiske elementer af -
 Registrering af forurening med en kompakt laserkildeKredit:Ecole Polytechnique Federale de Lausanne (EPFL) Forskere ved EPFL er kommet med en ny mellem infrarød lyskilde, der kan registrere drivhusgasser og andre gasser, samt molekyler i en persons
Registrering af forurening med en kompakt laserkildeKredit:Ecole Polytechnique Federale de Lausanne (EPFL) Forskere ved EPFL er kommet med en ny mellem infrarød lyskilde, der kan registrere drivhusgasser og andre gasser, samt molekyler i en persons -
 Et intelligent blødt materiale, der krøller under tryk eller udvider sig, når det strækkesEt intelligent blødt materiale kan krølle under tryk eller mekanisk belastning. Kredit:American Chemical Society Planter og dyr kan hurtigt reagere på ændringer i deres miljø, såsom en Venus flyve
Et intelligent blødt materiale, der krøller under tryk eller udvider sig, når det strækkesEt intelligent blødt materiale kan krølle under tryk eller mekanisk belastning. Kredit:American Chemical Society Planter og dyr kan hurtigt reagere på ændringer i deres miljø, såsom en Venus flyve -
 Var ursuppen en solid pre-protein gryderet?De første livspolymerer kan være opstået ved en daglig proces, der stadig observeres på Jorden i dag, såsom gentagen tørring og genopfyldning af damvand. Kredit:Ram Krishnamurthy / Center for Chemical
Var ursuppen en solid pre-protein gryderet?De første livspolymerer kan være opstået ved en daglig proces, der stadig observeres på Jorden i dag, såsom gentagen tørring og genopfyldning af damvand. Kredit:Ram Krishnamurthy / Center for Chemical
- Ingeniører bygger kemisk drevne hjul, der skifter til gear for at udføre mekanisk arbejde
- Første bekræftede forekomst af en lambeosaurin dinosaur fundet på Alaskas nordlige skråning
- Boeing 707
- Undersøgelse opfordrer til, at EU's handelspolitik foregriber etisk og ansvarlig AI -regulering
- 2017-prognose:Betydelig chance for jordskælvsskader i det centrale og østlige USA
- Grafen forkæmper næste generations 3D-displayteknologi


