Forskere udfylder et stykke af kobbertransportpuslespillet
Forskere har identificeret det protein, der transporterer kobber til mitokondrier, hvor kobber er påkrævet for funktionen af cellens energiomdannelsesmaskineri. Opdagelsen, offentliggjort i 9. februar -udgaven af Journal of Biological Chemistry , udfylder et stykke af puslespillet om, hvordan kobber fordeles og bruges i cellen.
Mennesker erhverver kobber i spormængder fra mad. På trods af sine lave niveauer, kobber er afgørende for funktionen af mange vigtige enzymer, for eksempel nogle af dem, der er involveret i syntetisering af kollagen og neurotransmittere. Især kobber er påkrævet til opbygning af cytochrom c -oxidase, kendt som COX, et stort proteinkompleks i mitokondrier, der udgør det sidste trin i elektrontransportkæden, som høster energi til produktion af ATP, cellens energivaluta.
Paul Cobine fra Auburn University og hans samarbejdspartner Scot Leary ved University of Saskatchewan har arbejdet i mere end 10 år på at forstå, hvordan kobber bruges til at samle COX. Et af de grundlæggende spørgsmål var:Hvordan kommer kobber over membranerne i mitokondrier?
"For at få (kobber) til den korrekte adresse (i cellen) uden at forstyrre andre proteiner, eller forstyrre andre mål, der har stor chance for at binde kobber, er en herkulsk leveringsindsats, "Cobine sagde." Det ligner at finde vej til en udgang i en overfyldt bar uden at røre de andre mennesker eller blive omdirigeret. Efter at have fundet udgangen skal du sørge for at gå gennem den rigtige dør. "
I det nye papir, forskerne brugte flere bevislinjer for at nå frem til et svar:Kobber transporteres inden for mitokondrier af et protein kaldet SLC25A3. Denne opdagelse var overraskende, fordi SLC25A3 allerede var kendt for at transportere fosfat, en negativt ladet ion, der henviser til, at kobberioner bærer en positiv ladning. Forskerne spekulerer i, at kobberionerne muligvis skal binde sig til en anden partner, danner et negativt ladet kompleks, for at SLC25A3 kan transportere den. Hvordan transportøren skelner mellem sine meget forskellige lasttyper, er det næste spørgsmål, forskerne ønsker at tage fat på.
Tidligere kendte mutationer i genet, der koder for SLC25A3, er ansvarlige for dårligt forståede genetiske lidelser, der involverer dysfunktionelle hjerte- og muskelfibre, fører til forstørrede hjerter og lav muskeltonus. Da disse væv kræver store mængder energi, det virker sandsynligt, at de symptomer, disse patienter oplever, kan være relateret til utilstrækkelig kobbertransport i mitokondrier.
"(Disse symptomer) lyder alle som om de kan være relateret til både ATP -produktion og cytochrom c -oxidase, "Sagde Cobine.
Med opdagelsen af kobbertransportvejen inden for mitokondrier, sundhedseffekterne af kobber kan studeres mere detaljeret, fordi forskere vil være i stand til at skelne virkningerne af kobber på COX fra de andre veje, det er involveret i.
"Hvis vi ikke håndterer kobber korrekt i hele vores liv, hvad er de stofskiftesygdomme, der (kunne) dukke op? "spørger Cobine." Nu har vi evnen til at se på, hvad der sker, når du mister mitokondrielt kobber på forskellige (udviklingsmæssige) stadier. "
Sidste artikelForskere fandt et alternativ til vandchlorering
Næste artikelIagttager en skiftende platinelektrode
 Varme artikler
Varme artikler
-
 Tweaking af en molekylstruktur kan sende den ned ad en anden vej til krystallisationEn lille ændring til en peptoid, der krystalliserer i et trin (venstre), sender den modificerede peptoid ned ad en mere kompliceret vej fra uordnet klump til krystal (højre). Kredit:Jim De Yoreo/PNNL
Tweaking af en molekylstruktur kan sende den ned ad en anden vej til krystallisationEn lille ændring til en peptoid, der krystalliserer i et trin (venstre), sender den modificerede peptoid ned ad en mere kompliceret vej fra uordnet klump til krystal (højre). Kredit:Jim De Yoreo/PNNL -
 Ny tilgang forudsiger glas altid udviklende adfærd ved forskellige temperaturerMultiskala modellering af et polymerglas for at forudsige dets temperaturafhængige egenskaber. Kredit:Wenjie Xia/NIST Ikke alt ved glas er klart. Hvordan dets atomer er arrangeret og opfører sig,
Ny tilgang forudsiger glas altid udviklende adfærd ved forskellige temperaturerMultiskala modellering af et polymerglas for at forudsige dets temperaturafhængige egenskaber. Kredit:Wenjie Xia/NIST Ikke alt ved glas er klart. Hvordan dets atomer er arrangeret og opfører sig, -
 Forskning afslører en ny måde at fremstille chirale katalysatorer påHænder er et simpelt eksempel på chirale objekter - spejlbilleder, men ikke identiske. Kredit:University of Southampton Forskere ved University of Southampton har opdaget en ny måde at skabe en hå
Forskning afslører en ny måde at fremstille chirale katalysatorer påHænder er et simpelt eksempel på chirale objekter - spejlbilleder, men ikke identiske. Kredit:University of Southampton Forskere ved University of Southampton har opdaget en ny måde at skabe en hå -
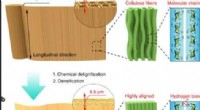 En enkeltcifret-mikrometer tykkelse træhøjttalerSkematisk af top-down tilgangen til direkte at transformere naturlig balsa til ultratynde træfilm. (a) Venstre:skematisk af det naturlige træ med dets porøse struktur. Midten:mikrostrukturen af cell
En enkeltcifret-mikrometer tykkelse træhøjttalerSkematisk af top-down tilgangen til direkte at transformere naturlig balsa til ultratynde træfilm. (a) Venstre:skematisk af det naturlige træ med dets porøse struktur. Midten:mikrostrukturen af cell
- Forskere annoncerer opdagelsen af en atomisk elektronisk simulator
- Bevarelse af indholdet af New York Public Library i en teskefuld protein, uden energi, i millioner a…
- Tab af arktisk havis i fortiden var forbundet med pludselige klimabegivenheder
- Sådan bestemmes det, hvor langt du er fra Lightning
- Sundhedskrise:Op mod en milliard tons affald, der potentielt brændes i det fri hvert år
- Rettighedsgrupper opfordrer Google til ikke at bøje sig for Kinas censorer


