Selvbærende sløjfe af kemiske reaktioner kan revolutionere lægemiddelproduktionen
Eksperter fra University of Nottingham har skabt et selvbærende kredsløb af reaktioner, som er en grønnere og mere effektiv metode til kemisk produktion. offentliggjort i Nature Catalysis, Drs. Francesca Paradisi og Martina Contente fra University of Nottingham producerer kemikalier mere effektivt gennem et løkkesæt af reaktioner ved hjælp af enzymer i flow. Kredit:University of Nottingham
Eksperter fra University of Nottingham har skabt et selvbærende kredsløb af reaktioner, som er en grønnere og mere effektiv metode til kemisk produktion.
I deres artikel Self-sustaining closed-loop multienzyme-medieret omdannelse af aminer til alkoholer i kontinuerlige reaktioner, udgivet i Naturkatalyse , Drs. Francesca Paradisi og Martina Contente fra University of Nottingham producerer kemikalier mere effektivt gennem et løkkesæt af reaktioner ved hjælp af enzymer i flow.
Reaktionerne reducerer miljøaffald, er selvbærende og producerer højere kvaliteter af slutproduktet.
Enzymer i flow, som brugt som en række 'søjler' pakket med immobiliserede enzymer og en bæreropløsning, strømmer reagenserne ind og produkterne ud med meget hurtigere reaktionshastigheder end ved normale batch-reaktioner.
Dr. Paradisi, Lektor i biokatalyse og enzymteknik på Kemiskolen, forklaret, at vand ofte bruges som det medium, hvori enzymmedierede kemiske reaktioner kan finde sted, men der er et problem med at bortskaffe affaldet i slutningen af processen.
Hun sagde:"Dit vand er nu noget forurenet med kemiske molekyler, som stammer fra den komplekse transformation, der har fundet sted, så det er ikke miljøvenligt at hælde det i afløbet. Det kan være meget dyrt at håndtere forurenet vand.
"Med den sløjfe, vi har skabt, bliver vandet genbrugt, de genererede biprodukter fjernes løbende og genvindes gennem processen, og det rene vand bruges igen som bærer for reagenserne i reaktionen."
Reaktionskæden er blevet til i en løkke, som er selvforstærkende og betyder, at produkter skabes, renset, og isoleret uden behov for manuel indgriben på hvert trin i processen.
"Forestil dig, at du har en hane, som i sin vandstrøm, producerer værdifulde produkter blandt de mindre værdifulde. Forestil dig, at du har en si, der filtrerer det produkt fra, du ønsker", sagde Dr. Paradisi.
"Så forestil dig, hvis denne vandhane kunne monteres på en vandgenbrugsfontæne, nu ved du, at vandet og de mindre værdifulde produkter (som stadig er værdifulde) aldrig går tabt, de fungerer bare som bæreren af de værdifulde molekyler.
"Dette øger ikke kun effektiviteten og sparer tid, det skaber et nul-affaldssystem. Vi opdagede også, at arbejdet på denne måde betød, at udbyttet af nogle "vanskelige at lave" højværdiprodukter også er meget højere end for traditionelle kemiske reaktioner - med over 20 gange."
I forskningen, som blev finansieret gennem en bevilling fra Bioteknologi og Biologisk Forskningsråd, parret brugte aminer naturligt produceret i kroppen, såsom dopamin, tryptamin og histaminer. De brugte derefter løkken af reaktioner til at omdanne disse til alkoholer såsom 4-hydroxytyrosol, som er en antioxidant og typisk sværere at producere.
Dr. Paradisi sagde:"Disse alkoholer er meget eftertragtede i fremstillingen af lægemidler, fødevaretilsætningsstoffer, at skabe parfume og aromaer, og de er svære og meget dyre at fremstille. Traditionelle kemiske strategier kan tage op til to uger for at producere et udbytte på 5-13 procent for det mest udfordrende molekyle. Vi har fundet ud af, at vi kan producere omkring 70 procent på 45 minutter."
Og forskningen er ikke begrænset til alkoholer, da processen kan overføres til at skabe andre produkter.
"Mulighederne for dette er enorme, det handler bare om den rigtige anvendelse", tilføjede Dr. Paradisi. "Vi kan tage ethvert molekyle af interesse og se, om vi kan dissekere det trin for trin, tænker på hvilket enzym der kan katalysere reaktionen omvendt, indtil vi kommer til et simpelt udgangsmateriale. Vi kan derefter samle enzymerne i rækkefølge, meget som at skabe et kunstigt biosystem, hvor det første produkt er substratet for det næste enzymatiske trin, indtil det endelige molekyle er opnået. I modsætning til et biologisk system, denne ex-vivo enzymfabrik er meget mere robust, vi kan dramatisk øge mængden af enzym, der er ansvarligt for hvert trin (fordi det aldrig går tabt, det er indeholdt i reaktoren), finjuster den relative hastighed af hver reaktion, for meget hurtige konverteringer.
"Vi behøver ikke bekymre os om cellens integritet, eller molekylets/molekylernes potentielle toksicitet for det biologiske system. Flow betyder effektivt, at hvis hvert trin er optimeret, vi kan behandle hver del af kaskaden som en separat enhed. Endelig, sløjfe spildevandet tilbage til begyndelsen, bærer nogle af de hjælpekomponenter, som enzymerne behøver for at virke, vi øger systemets produktivitet eksponentielt. Dette er en ny måde at arbejde med enzymer på, som aldrig er blevet gjort før."
 Varme artikler
Varme artikler
-
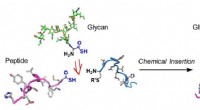 En vindende kombination til glykoproteinsynteseGlycoproteinsyntese ved kemisk indsættelse ved hjælp af en thiosyremedieret strategi:Metoden samler et fuldt glycoproteinsegment i to trin. Kredit:Osaka University Mange processer i kroppen regule
En vindende kombination til glykoproteinsynteseGlycoproteinsyntese ved kemisk indsættelse ved hjælp af en thiosyremedieret strategi:Metoden samler et fuldt glycoproteinsegment i to trin. Kredit:Osaka University Mange processer i kroppen regule -
 Designerbakterier producerer koralantibiotikaHornkoraller af arten Antillogorgia elisabethae producerer antibiotiske naturlige stoffer. Et forskerhold på TUM har med succes produceret et af disse stoffer i laboratoriet. Kredit:Thomas Brück/TUM
Designerbakterier producerer koralantibiotikaHornkoraller af arten Antillogorgia elisabethae producerer antibiotiske naturlige stoffer. Et forskerhold på TUM har med succes produceret et af disse stoffer i laboratoriet. Kredit:Thomas Brück/TUM -
 Gennembrud skabt ved påvisning af kulstof -urenheder i galliumnitridkrystaller via lysGaN-krystaller under foto-excitation. Kulstofkoncentration fra venstre mod højre:høj, medium, og lav. Kredit:Kazunobu Kojima Kulstofrenhed har længe hindret effektiviteten i nitridbaserede elektro
Gennembrud skabt ved påvisning af kulstof -urenheder i galliumnitridkrystaller via lysGaN-krystaller under foto-excitation. Kulstofkoncentration fra venstre mod højre:høj, medium, og lav. Kredit:Kazunobu Kojima Kulstofrenhed har længe hindret effektiviteten i nitridbaserede elektro -
 Solar fordamper tilbyder en frisk rute til ferskvandEn selvrensende anordning lavet af træ har til formål at gøre småskala afsaltning mere praktisk. Kredit:John T. Consoli/University of Maryland Omkring en milliard mennesker verden over mangler adg
Solar fordamper tilbyder en frisk rute til ferskvandEn selvrensende anordning lavet af træ har til formål at gøre småskala afsaltning mere praktisk. Kredit:John T. Consoli/University of Maryland Omkring en milliard mennesker verden over mangler adg
- Rapport opfordrer indtrængende til overordnet strategi for national sikkerhed og klimakrise
- Billioner af ekstra økonomiske skader forudsagt i ny undersøgelse af virkningerne af klimaændring…
- Undersøgelse sår tvivl om elektroniske ankelmonitorer som alternativ til fængsling
- At kaste lys over hemmeligheder om galakserotation
- Vestlige sibiriske floder og søer udsender drivhusgasser til atmosfæren
- Vi vurderer, at der er op til 14 millioner tons mikroplast på havbunden. Det er værre end vi troed…


