Kortlægning af kræftbevægelser
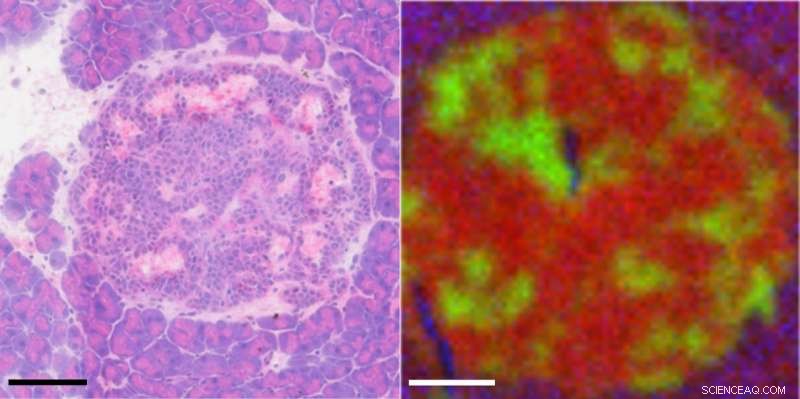
Kræftforskere kæmper for at identificere tumorceller, der er spredt i ikke-maligne væv, fordi tumorceller udnytter vævsmiljøet og monopoliserer tilgængelige ressourcer for at fortsætte med at vokse. Forskere tilskriver kræftcellers evne til at bruge cellesignalering og metaboliske veje, der tilsidesætter normale cellevækstbegrænsninger, til komplicerede kemiske udvekslinger mellem væv og tumorceller. En ny tilgang viser løfte om at begynde at analysere celle-til-celle-interaktioner i dette komplekse miljø. Forskerne diskuterer deres arbejde i Biointerphases. På dette billede, en ø-tumorregion vist med normal farvning og med time-of-flight sekundær ion massespektrometri. Fedtmolekyler vises i rødt, jern og andre blodrelaterede komponenter er grønne, og det omgivende væv er blåt. Kredit:Dan Graham og Blake Bluestein
Kræftforskere kæmper for at identificere tumorceller, der er spredt i ikke-maligne væv, fordi tumorceller udnytter vævsmiljøet og monopoliserer tilgængelige ressourcer for at fortsætte med at vokse. Forskere tilskriver kræftcellers evne til at bruge cellesignalering og metaboliske veje, der tilsidesætter normale cellevækstbegrænsninger, til komplicerede kemiske udvekslinger mellem væv og tumorceller. En ny tilgang viser løfte om at begynde at analysere celle-til-celle-interaktioner i dette komplekse miljø.
Forskere ved University of Washington har demonstreret en ny teknik til at kortlægge strømmen af biomolekyler i og omkring solide tumorer. I et særnummer af Biointerfaser der fremhæver kvinder inden for biointerfacevidenskab, gruppen bruger time-of-flight sekundær ion massespektrometri (ToF-SIMS) til at observere, hvordan molekyler bevæger sig, og hvordan tumorer sender signaler til deres mikromiljø og opdrætter lokalt væv af ressourcer.
"Folk vil se, at denne TOF-SIMS-teknik, kombineret med viden om tumorcelleadfærd, vil give forskere mulighed for at forstå, hvad der sker på det kemiske molekylære niveau, " sagde Lara Gamble, en forfatter på papiret. "Er der visse molekyler, lipider eller brændstoffer, som tumorer suger væk fra almindeligt væv for at hjælpe dem med at vokse?"
Tumorceller kan trække lipider fra naboceller for at hjælpe med at bygge større membraner og give energi til oppustede tumorceller. Blodkar kan blive ødelagt, efterlader "blodsøer" inde i tumorer, som nogle forskere mener fodrer den voksende tumor.
Forskellige metoder er blevet udviklet til at identificere, hvor en tumor er, og hvordan den bruger bindevæv som blodkar til at opretholde sin vækst, men, indtil for nylig, der er lidt blevet forstået om, hvilke slags signaler tumorer bruger til at opnå dette. For at besvare dette spørgsmål, Gamble og hendes kolleger bruger TOF-SIMS til at sprænge nanoskalaområder af en tumor, så dele forlader prøven og kommer ind i et massespektrometer. Denne enhed adskiller og tæller derefter molekyler baseret på deres molekylvægt.
Scanningsområder på 800 nanometer eller mindre, fremgangsmåden genererer et kort for, hvor et bestemt molekyle er til stede i en tumorprøve. En kvadratmillimeter siges at tage omkring halvanden time at kortlægge.
Gruppen testede deres teknik på en inducerbar musemodel af pancreas neuroendokrin tumorigenese, der er veletableret som en model til at studere interaktionen mellem onkogener og tumorsuppressorer, som tilsammen genererer meget aggressive kræftformer.
Når kortlagt, musetumor-mikromiljøerne viste signifikante ændringer i stofskiftet. ToF-SIMS-teknikken var i stand til at identificere ændringer i den normale strøm af en lang række molekyler lige fra større lipider og nukleotider ned til enkelte ioner.
Næste, Gamble og hendes gruppe planlægger at bruge deres teknik på tidligere tidspunkter for tumorinduktion i et forsøg på at kortlægge en række kemiske signaler, der fortæller historien om bugspytkirteltumorvækst.
"Vi søger også at se, om der er krydstale mellem tumorer, " sagde Gamble. "Vi vil gerne identificere de molekyler, der både kan starte og vedligeholde tumorvækst."
 Varme artikler
Varme artikler
-
 Forskere måler elektronemission for at forbedre forståelsen af laserbaseret 3-D-tryk i metalForskere målte emission af elektroner fra overfladen af rustfrit stål under laserpulverbedfusion (LPBF) betingelser, demonstrere potentialet for at bruge termioniske emissionssignaler til at detekte
Forskere måler elektronemission for at forbedre forståelsen af laserbaseret 3-D-tryk i metalForskere målte emission af elektroner fra overfladen af rustfrit stål under laserpulverbedfusion (LPBF) betingelser, demonstrere potentialet for at bruge termioniske emissionssignaler til at detekte -
 Forskere sporer nye biokatalysatorerEn videnskabsmand undersøger bakterievækst efter fytasescreening. Kredit:G A Castillo Villamizar Fosfat er et nøgleelement i mange processer i kroppen og afgørende for den globale fødevareprodukti
Forskere sporer nye biokatalysatorerEn videnskabsmand undersøger bakterievækst efter fytasescreening. Kredit:G A Castillo Villamizar Fosfat er et nøgleelement i mange processer i kroppen og afgørende for den globale fødevareprodukti -
 Solar fordamper tilbyder en frisk rute til ferskvandEn selvrensende anordning lavet af træ har til formål at gøre småskala afsaltning mere praktisk. Kredit:John T. Consoli/University of Maryland Omkring en milliard mennesker verden over mangler adg
Solar fordamper tilbyder en frisk rute til ferskvandEn selvrensende anordning lavet af træ har til formål at gøre småskala afsaltning mere praktisk. Kredit:John T. Consoli/University of Maryland Omkring en milliard mennesker verden over mangler adg -
 Ny tilgang gør det letteste bilmetal mere økonomisk, nyttigEt rør med en diameter på 50 mm med en vægtykkelse på 1,5 mm skabt af en solid luns magnesiumlegering ved hjælp af PNNLs ShAPE™-ekstruderingsproces. Kredit:PNNL Magnesium - det letteste af alle st
Ny tilgang gør det letteste bilmetal mere økonomisk, nyttigEt rør med en diameter på 50 mm med en vægtykkelse på 1,5 mm skabt af en solid luns magnesiumlegering ved hjælp af PNNLs ShAPE™-ekstruderingsproces. Kredit:PNNL Magnesium - det letteste af alle st
- Hvad er lossning, og hvordan bidrager det til vejrforhold?
- Forskere skaber anti-laser til et kondensat af ultrakølede atomer
- Facebooks Vægtens valuta under beskydning
- Forsker studerer, hvordan og hvorfor folk trykker på knapper
- Luftkvalitetsforskning kan forbedre folkesundheden i Vestafrika
- Blæksprutte inspireret klæbemiddel fungerer under vand


