Designer enzym erobrer sulfitreduktion, en flaskehals i miljøoprydning

Kemiprofessor Yi Lu, venstre, og kandidatstuderende Evan Mirts har designet et nyt syntetisk enzym, der reducerer forbindelsen sulfit til sulfid - en notorisk kompleks flertrins kemisk reaktion, der har unddraget kemikere i årevis. Kredit:L. Brian Stauffer
Forskere har ryddet en forhindring mod miljømæssig oprydning af visse forurenende stoffer med et nydesignet syntetisk enzym, der reducerer forbindelsen sulfit til sulfid - en notorisk kompleks flerstegs kemisk reaktion, der har unddraget kemikere i årevis.
I journalen Videnskab , kemikere ved University of Illinois i Urbana-Champaign beskrev deres enzym indeholdende to forskellige jernholdige centre forbundet med et enkelt enzym.
Sulfitreduktion, en almindelig oxidationsreduktion-eller redoxreaktion-kan forstyrre oprydningen af en større klasse af miljøforurenende stoffer, herunder nitrat, arsenat og perchlorat. Disse forurenende stoffer kommer ud i miljøet som biprodukter fra produktionen af raketbrændstof, ammunition og gødning. Sulfit forekommer også naturligt og forstyrrer fjernelsen af mere giftige forbindelser, og kemikere har ikke været i stand til at skabe katalysatorer for at fjerne sulfit, fordi det kræver flere trin i reaktioner ved hjælp af et komplekst aktivt sted, der er svært at designe og syntetisere.
"Mange biokemiske reaktioner kræver, at en række enzymer arbejder sammen for at udføre reaktioner på flere trin, men sulfitreduktion bruger kun ét enzym, kaldet sulfitreduktase, der gør alt arbejdet, "sagde Yi Lu, professor i kemi i Illinois. "Naturen skabte en meget kompleks enzymstruktur til at håndtere denne kemiske reaktion, og forskere har ikke været i stand til at replikere det før nu. "
Tidligere grupper, der har forsøgt at bygge et syntetisk sulfitreducerende enzym, har koncentreret sig om at lave strukturelle modeller, der ligner det aktive sted for native enzymer, sagde kemi kandidatstuderende Evan Mirts. Til denne undersøgelse, holdet brugte et enzym som et stillads til at forankre klynger af jern- og svovlatomer, der opfører sig som små molekylære batterier, overføre de elektroner, der er nødvendige for at skubbe redoxreaktionen.
"Jeg tror, vi havde succes, fordi vi fokuserede på funktionaliteten af vores syntetiske enzym, ikke genopbygge den enklest mulige struktur, "Mirts sagde." Vi stod for interaktioner, der typisk betragtes som sekundære, eller mindre vigtig for den samlede redoxreaktion. Det viser sig, at disse interaktioner er ekstremt vigtige. "
"Da vi tegnede os for de såkaldte svagere interaktioner i vores designede enzym, vi så pludselig redoxreaktionsaktivitet, der lignede meget det naturligt forekommende sulfitreducerende enzym, "sagde Lu, også en fælles udpeget ved U.S. Department of Energy's Pacific Northwest National Laboratory.
Teamet forestiller sig, at deres nyudviklede enzym inspirerer en ny generation af katalysatorer til at hjælpe med at rense giftigt affald i miljøet og hjælpe med at forbedre kvaliteten af olieprodukter.
"Bortset fra de praktiske anvendelser, Jeg tror, at vores arbejde her har avanceret grænsen for kunstigt enzymdesign med hensyn til at dechifrere kompleksiteten af redoxreaktioner og designe multifaktorkatalysatorer med meget høj aktivitet, "Sagde Lu." Med den vellykkede demonstration af dette system, vi kan nu begynde at designe mange andre multicofactor -enzymer, der udfører endnu mere komplekse, vanskelige reaktioner, som vi kun kunne drømme om før. "
 Varme artikler
Varme artikler
-
 Sort silicium forhindrer øjenimplantat i at stivneKunstnerens skildring af et okulært implantat. Kredit:Lee, Jeong Oen, Vinayak Narasimhan, Juan Du, David W. Sretavan, og Hyuck Choo:Sort silicium som en biokompatibel antirefleksbelægning til medicins
Sort silicium forhindrer øjenimplantat i at stivneKunstnerens skildring af et okulært implantat. Kredit:Lee, Jeong Oen, Vinayak Narasimhan, Juan Du, David W. Sretavan, og Hyuck Choo:Sort silicium som en biokompatibel antirefleksbelægning til medicins -
 Nikkelatom hjælper med at reducere kuldioxidFigur 1:At vide, hvordan en nikkeljernsulfidkatalysator hjælper med at reducere kuldioxid til kulilte og andre kulbaserede produkter, kan føre til teknologier, der kan omdanne kuldioxid i atmosfæren t
Nikkelatom hjælper med at reducere kuldioxidFigur 1:At vide, hvordan en nikkeljernsulfidkatalysator hjælper med at reducere kuldioxid til kulilte og andre kulbaserede produkter, kan føre til teknologier, der kan omdanne kuldioxid i atmosfæren t -
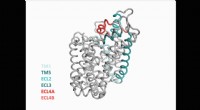 Neurovidenskabsmænd opdager ny struktur af vigtigt protein i hjernenAnimation af LeuT-transporterens fire trin sat sammen til en fuld cyklus. Kredit:Københavns Universitet Efter fem års eksperimenter, Det er lykkedes forskere fra Københavns Universitet at udkrysta
Neurovidenskabsmænd opdager ny struktur af vigtigt protein i hjernenAnimation af LeuT-transporterens fire trin sat sammen til en fuld cyklus. Kredit:Københavns Universitet Efter fem års eksperimenter, Det er lykkedes forskere fra Københavns Universitet at udkrysta -
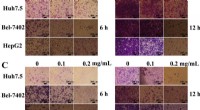 Marine bakterielt exopolysaccharid EPS11 hæmmer migration og invasion af levercancercellerFigur 1EPS11 hæmmer migration, invasion og kolonidannelse af levercancerceller (Huh7.5, Bel-7402, og HepG2 -cellelinjer). (A) Observation af fi liform-strukturer i Bel-7402 og HepG2-celler efter behand
Marine bakterielt exopolysaccharid EPS11 hæmmer migration og invasion af levercancercellerFigur 1EPS11 hæmmer migration, invasion og kolonidannelse af levercancerceller (Huh7.5, Bel-7402, og HepG2 -cellelinjer). (A) Observation af fi liform-strukturer i Bel-7402 og HepG2-celler efter behand
- Hvad er Jordens tykkelse?
- Stadig for tidligt til at sige, hvilken effekt #MeToo har
- Genoplivning af bjærgede træskibe og artefakter med smart nanoteknologi
- Sådan magnetiserer du en magnet
- Demokraterne ønsker, at feds skal målrette den sorte kasse med AI -bias
- Tørke antænder konflikt mellem mennesker og vilde dyr i Zimbabwe


