En måde at bruge en to-nikkel katalysator til at syntetisere cyclopentener
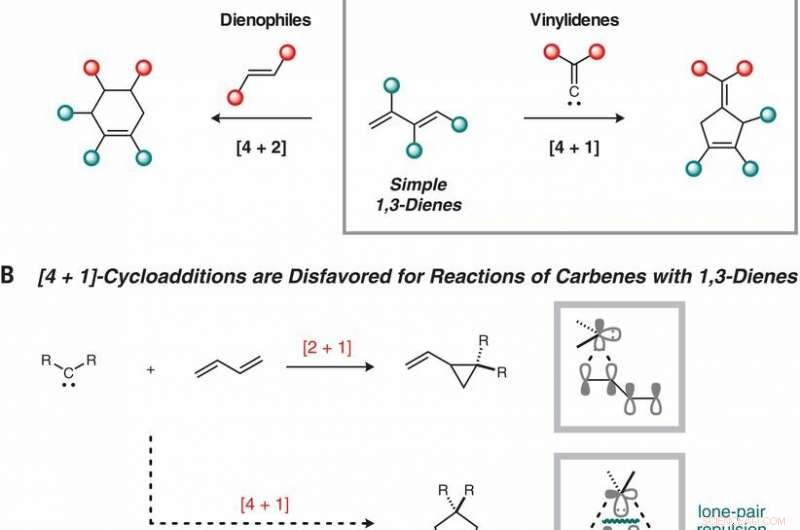
Reaktionsudvikling. (A) Komplementære cykloadditionsruter til fem- og seksleddede ringe fra 1, 3-diener. (B) Pericykliske [4 + 1]-cykloadditioner lider af store elektroniske barrierer på grund af frastødning mellem det enlige carbenpar og Ψ1 orbitalen af 1, 3-dien. (C) Dinickel-katalyseret reduktiv [4 + 1] -cykloddition på 1, 1-dichloralkener og 1, 3-diener. NMP, N-methyl-2-pyrrolidon; rt, stuetemperatur; c-Pent, cyclopentyl. Kredit:(c) Videnskab (2019). DOI:10.1126/science.aau0364
Et par forskere ved Purdue University har fundet en måde at bruge en diatomisk Ni-Ni-katalysator til at syntetisere cyclopentenes. I deres papir offentliggjort i tidsskriftet Videnskab , You-Yun Zhou og Christopher Uyeda beskriver deres metode og skitserer, hvorfor de mener, at cyclopentenprodukter ville være nyttige. Keywan Johnson og Daniel Weix fra University of Wisconsin har publiceret et Perspective-stykke i samme tidsskriftsudgave, der beskriver det arbejde, teamet har udført i Indiana.
Johnson og Weix bemærker, at opdagelsen af nye molekyler ligger bag mange af de nye materialer, som videnskabsmænd har skabt gennem årene. En af måderne, hvorpå nye molekyler opdages, er ved at observere dem i naturen og derefter syntetisere dem i et laboratorium. De bemærker også, at overgangsmetalkatalyse er blevet brugt i vid udstrækning til at syntetisere mange nye molekyler, der i øjeblikket bruges i en lang række produkter. De bemærker endvidere, at størstedelen af overgangsmetalkatalyse involverer brugen af kun ét metalatom, men der har været undtagelser, hvor katalysatorer har en to-metal atomkerne. I denne nye indsats, forskerne brugte en diatomisk Ni-Ni-katalysator til at udføre stereostyret syntese af cyclopentener (ringe lavet af fem kulstofatomer).
Forskerne bemærker, at i typiske Diels-Alder-reaktioner, en dien og en alken får lov til at reagere, resulterer i en cyclohexen (en ring lavet af seks carbonatomer). De bemærker også, at fem-leddet ringe er lavet i naturen på en række forskellige måder, hvilket tyder på, at de kunne vise sig nyttige, hvis de let kunne syntetiseres. Tidligere bestræbelser på at gøre det, imidlertid, ikke har panoreret. Problemet har været at beskæftige sig med [4 + 1] reaktioner - der er vanskeligheder forbundet med at generere dem ved hjælp af stabile molekyler. Også, reaktivitet med dem har vist sig at være en udfordring.
Zhou og Uyeda tog en anden tilgang, ved i stedet at bruge en tometalkatalysator. De fandt ud af, at i deres tilgang, de to metalkerner delte opgaven med at kontrollere, hvordan reaktionen fandt sted, og med at danne carbenet. Dette muliggjorde brugen af dichloralkener, som var mere stabile end diazoforbindelser. Derudover kun et af rhodiumcentrene var ansvarligt for bindingsdannelsen med katalysatoren - det andet modulerede reaktiviteten af det første gennem bindingen. Resultatet var en femsidet cyclopenten.
© 2019 Science X Network
 Varme artikler
Varme artikler
-
 Sådan indlæses den periodiske tabel i en videnskabelig lommeregnerEn videnskabelig lommeregner, også kaldet en grafregner, kan bruges i en række matematik- og videnskabsklasser. Apps, såsom en Periodic Table-app, kan downloades til graferegnemaskiner, inklusive de p
Sådan indlæses den periodiske tabel i en videnskabelig lommeregnerEn videnskabelig lommeregner, også kaldet en grafregner, kan bruges i en række matematik- og videnskabsklasser. Apps, såsom en Periodic Table-app, kan downloades til graferegnemaskiner, inklusive de p -
 Nye spilskiftende zeolitkatalysatorer syntetiseretKredit:Pohang University of Science &Technology (POSTECH) Et forskerhold hos POSTECH har afsløret en lovende ny zeolit, forventes at blive et vendepunkt for olieraffinaderi og petrokemisk industri
Nye spilskiftende zeolitkatalysatorer syntetiseretKredit:Pohang University of Science &Technology (POSTECH) Et forskerhold hos POSTECH har afsløret en lovende ny zeolit, forventes at blive et vendepunkt for olieraffinaderi og petrokemisk industri -
 Fjerlette metalkatoder til stabile lithium-ilt batterierNanoporøse nikkelkatoder til lithium-iltbatterier er ultralette, vist her balanceret på blomsterstøvdragere. Kredit:American Chemical Society Lithium-oxygen-systemer kan en dag overgå nutidens lit
Fjerlette metalkatoder til stabile lithium-ilt batterierNanoporøse nikkelkatoder til lithium-iltbatterier er ultralette, vist her balanceret på blomsterstøvdragere. Kredit:American Chemical Society Lithium-oxygen-systemer kan en dag overgå nutidens lit -
 Rekordstor ny analytisk metode til fingeraftryk af olie og andre komplekse blandingerKredit:University of Warwick Forskere ved University of Warwick har udviklet en mere kraftfuld metode til analyse af kemiske blandinger, som har været i stand til at tildele et rekordstort antal p
Rekordstor ny analytisk metode til fingeraftryk af olie og andre komplekse blandingerKredit:University of Warwick Forskere ved University of Warwick har udviklet en mere kraftfuld metode til analyse af kemiske blandinger, som har været i stand til at tildele et rekordstort antal p
- Kønsbias i kommentarer udgør barrierer for kvindelige forskere
- Ny metode sniger medicin ind i kræftceller, før den udløser frigivelse
- Sådan fungerer Space Camp
- Forskere skaber unikke grafen-nanoporer med optiske antenner til DNA-sekventering
- Storbritanniens olie- og gasreserver kan kun vare et årti, undersøgelse tyder på
- Sådan finder du standardiserede værdier for korrelation


