C. elegans rundorme høster et vigtigt coenzym fra de bakterier, de indtager
Caenorhabditis elegans. Kredit:Wikipedia
En undersøgelse udført i C. elegans nematode rundorm kan føre til forbedret behandling af en sjælden menneskelig genetisk lidelse, der forårsager alvorlige neurologiske symptomer, der fører til død i den tidlige barndom. I deres rapport offentliggjort i Naturens kemiske biologi , to efterforskere fra Massachusetts General Hospital (MGH) beskriver at finde det C. elegans kan erhverve molybdæn-kofaktoren (Moco) - et molekyle, der er afgørende for funktionen af essentielle enzymer - ved at indtage E.coli-bakterier, det første bevis på, at Moco kan overføres mellem arter. Efterforskerne identificerede også den metaboliske vej, der er ansvarlig for symptomerne observeret ved Moco-mangel.
"Indtil nu, Moco blev anset for at være for ustabil til at blive handlet mellem celler og væv, meget mindre mellem organismer adskilt af en milliard års evolution, " siger hovedforfatter Kurt Warnhoff, Ph.D., MGH Molekylær Biologi. "Men vi fandt, at interaktionen mellem disse arter var ret robust. Bakterier isoleret fra rådnende frugter - en typisk C. elegans habitat - var i stand til at levere Moco til nematoderne. Denne evne til C. elegans at udvinde Moco fra sit mikrobiom er spændende og giver håb om, at vi måske kan udnytte lignende systemer til at levere moden Moco til patienter med Moco-mangel."
Mange livsvigtige reaktioner kræver virkning af enzymer, hvoraf flere, på tur, kræver molekyler kaldet cofaktorer eller coenzymer for at fungere korrekt. Et sådant coenzym, Moco, er nødvendig for inkorporering af grundstoffet molybdæn i flere vigtige enzymer. Hos mennesker, genetiske mutationer i Moco-syntetiserende enzymer forårsager Moco-mangel. Berørte spædbørn udvikler anfald, forringelse af hjernevæv, udviklingsforsinkelse og dør normalt inden for de første måneder af livet. Moco-mangel anslås at påvirke 1 ud af 100, 000 til 200, 000 fødsler.
Sunde dyr fra C. elegans til mennesker kan syntetisere Moco i deres kroppe. I mutant C. elegans der ikke kan syntetisere Moco, normal udvikling stopper, og dyrene dør, medmindre de fodres med en bakteriediæt indeholdende coenzymet, parallelt med virkningerne af Moco-mangel hos mennesker. Ved brug af C. elegans genetik for at undersøge, hvordan Moco-mangel fører til døden, Warnhoff og seniorforfatter Gary Ruvkun, Ph.D., også af MGH Molekylær Biologi, identificeret den vej, der normalt nedbryder de svovlholdige aminosyrer methionin og cystein, som synderen. Et biprodukt af denne nedbrydning er frigivelsen af sulfit, et toksin, der bruges som konserveringsmiddel i mange fødevarer, og forskerne fandt ud af, at mangel på Moco inaktiverer SUOX-enzymet, der normalt afgifter sulfit, fører til nematodernes død.
siger Ruvkun, professor i genetik ved Harvard Medical School, "Disse molekylære indsigter tilbyder potentielle terapeutiske veje til behandling af Moco-mangel. Begrænsning af eksponeringen for svovlholdige forbindelser og inaktivering af de enzymer, der genererer sulfit, kan lindre de fysiologiske defekter og deraf følgende død, som er uundgåelige ved human Moco-mangel."
At finde ud af, at blot indtagelse af Moco-producerende E.coli var tilstrækkeligt til at understøtte væksten og udviklingen af Moco-deficient C. elegans tyder på, at coenzymet kan fungere som et vitamin. Forskerne fandt ud af, at omkring to tredjedele af bakterielle genomer syntetiserer Moco, hvilket indikerer, at nematoderne kunne være afhængige af bakterier til at levere denne essentielle cofaktor det meste af tiden. Nu Warnhoff og Ruvkun og arbejder på at skelne hvordan C. elegans bestemmer, hvornår Moco skal syntetiseres i sin krop, og hvornår den skal indtages som et "kosttilskud, " fra de bakterier, den forbruger.
 Varme artikler
Varme artikler
-
 Nye tilgange til at undersøge de molekylære årsager til amyloiddannelseIllustration af en voksende fibril i fælden og laseren. Kredit:Martin Fränzl Mere end 24 millioner mennesker verden over lider af neurodegenerative sygdomme som Alzheimers, Parkinsons eller Huntin
Nye tilgange til at undersøge de molekylære årsager til amyloiddannelseIllustration af en voksende fibril i fælden og laseren. Kredit:Martin Fränzl Mere end 24 millioner mennesker verden over lider af neurodegenerative sygdomme som Alzheimers, Parkinsons eller Huntin -
 Ny tekstilfarvningsmetode reducerer drastisk vandbehov og giftig udledning af farvestoffer drastiskAnuradhi Liyanapathiranage er ph.d. kandidat i College of Family and Consumer Sciences. Kredit:Nancy Evelyn/UGA Anuradhi Liyanapathiranage brænder for bæredygtighed og beskyttelse af miljøet genne
Ny tekstilfarvningsmetode reducerer drastisk vandbehov og giftig udledning af farvestoffer drastiskAnuradhi Liyanapathiranage er ph.d. kandidat i College of Family and Consumer Sciences. Kredit:Nancy Evelyn/UGA Anuradhi Liyanapathiranage brænder for bæredygtighed og beskyttelse af miljøet genne -
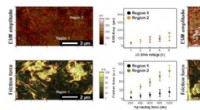 Visualisering af funktionelle komponenter for at karakterisere optimale kompositelektroderAFM -billeder af (a, c) prøver A og (b, d) B. (a, b) Topografiske højdebilleder og (c, d) friktionskraftbilleder, henholdsvis. Alle billeder blev optaget med en spidsbelastningskraft på 400 nN. Røde l
Visualisering af funktionelle komponenter for at karakterisere optimale kompositelektroderAFM -billeder af (a, c) prøver A og (b, d) B. (a, b) Topografiske højdebilleder og (c, d) friktionskraftbilleder, henholdsvis. Alle billeder blev optaget med en spidsbelastningskraft på 400 nN. Røde l -
 Ny metode kunne hjælpe med at producere renere, sikrere stofferOptisk aktivitet af molekyler forstærkes i mere end 10 gange, ved strukturspecifik adsorption af molekylerne på chirale nanopartikler. Kredit:HKBU Fysik- og kemiforskere fra Hong Kong Baptist Univ
Ny metode kunne hjælpe med at producere renere, sikrere stofferOptisk aktivitet af molekyler forstærkes i mere end 10 gange, ved strukturspecifik adsorption af molekylerne på chirale nanopartikler. Kredit:HKBU Fysik- og kemiforskere fra Hong Kong Baptist Univ
- Sådan kalibrerer du et FTIR spektrometer
- Trump -administrationen udhuler EPA's videnskabsintegritetskort
- Grundforskning til verdensforandrende applikationer kan tage 6 måneder – eller 50 år
- Biologer identificerer gammel stressrespons i koraller
- GPM -data, der bruges til at evaluere hawaiiernes oversvømmelse af nedbør
- Orkanen Isaias brøler i land på den amerikanske østkyst


