Forskere laver de første kort over to melatoninreceptorer, der er afgørende for søvn
Det søvnfremmende hormon melatonin (vist som et stjernebillede på nattehimlen) syntetiseres fra serotonin (vist som en drage) om natten, og begge disse arkaiske molekyler går forud for dyrenes evolution. Høje melatoninniveauer om natten tillader det at etablere sine søvnfremmende egenskaber ved at virke gennem højaffinitetsreceptorer, afbildet i højre side af billedkompositionen. Kredit:Yekaterina Kadyshevskaya, Bridge Institute ved USC Michelson Center for Convergent Bioscience.
Et internationalt team af forskere brugte en røntgenlaser ved Department of Energy's SLAC National Accelerator Laboratory til at skabe de første detaljerede kort over to melatoninreceptorer, der fortæller vores kroppe, hvornår vi skal sove eller vågne og guider andre biologiske processer. En bedre forståelse af, hvordan de virker, kunne gøre det muligt for forskere at designe bedre lægemidler til at bekæmpe søvnforstyrrelser, kræft og type 2-diabetes. Deres resultater blev offentliggjort i to aviser i dag i Natur .
Holdet, ledet af University of Southern California, brugte røntgenstråler fra SLACs Linac Coherent Light Source (LCLS) til at kortlægge receptorerne, MT1 og MT2, bundet til fire forskellige forbindelser, der aktiverer receptorerne:et lægemiddel mod søvnløshed, et lægemiddel, der blander melatonin med det antidepressive middel serotonin, og to melatoninanaloger.
De opdagede, at begge melatoninreceptorer indeholder smalle kanaler, der er indlejret i de fedtholdige membraner i cellerne i vores kroppe. Disse kanaler tillader kun melatonin - som kan findes i både vand og fedt - at passere igennem, blokering af serotonin, som har en lignende struktur, men kun er glad i vande miljøer. De afslørede også, hvordan nogle meget større forbindelser kun kan målrette MT1 og ikke MT2, på trods af de strukturelle ligheder mellem de to receptorer. Dette bør informere designet af lægemidler, der selektivt retter sig mod MT1, hvilket indtil videre har været udfordrende.
"Disse receptorer udfører uhyre vigtige funktioner i den menneskelige krop og er vigtige lægemiddelmål af stor interesse for den farmaceutiske industri, " sagde Linda Johansson, en postdoc ved USC, der ledede det strukturelle arbejde med MT2. "Gennem dette arbejde var vi i stand til at opnå en meget detaljeret forståelse af, hvordan melatonin er i stand til at binde til disse receptorer."
Sengetid
Folk gør det, fugle gør det, fisk gør det. Næsten alle levende væsener i dyreriget sover, og med god grund.
"Det er afgørende for hjernen at tage hvile og behandle og gemme minder, som vi har akkumuleret i løbet af dagen, " sagde medforfatter Alex Batyuk, en videnskabsmand ved SLAC. "Melatonin er det hormon, der regulerer vores søvn-vågen-cyklusser. Når der er lys, produktionen af melatonin hæmmes, men når mørket kommer, er det signalet for vores hjerner om at gå i dvale."
Melatoninreceptorer tilhører en gruppe af membranreceptorer kaldet G-proteinkoblede receptorer (GPCR'er), som regulerer næsten alle de fysiologiske og sensoriske processer i den menneskelige krop. MT1 og MT2 findes mange steder i hele kroppen, inklusive hjernen, nethinden, kardiovaskulære system, lever, nyre, milt og tarm..
Disse receptorer overvåger vores urgener, tidtagere af kroppens indre ur, eller døgnrytme. I en perfekt verden, vores indre ure ville synkronisere med solens opgang og nedgang. Men når folk rejser på tværs af tidszoner, arbejde natten over eller bruge for meget tid foran skærme eller andre kunstige kilder til blåt lys, disse tidtagere er smidt ud af skyggen.
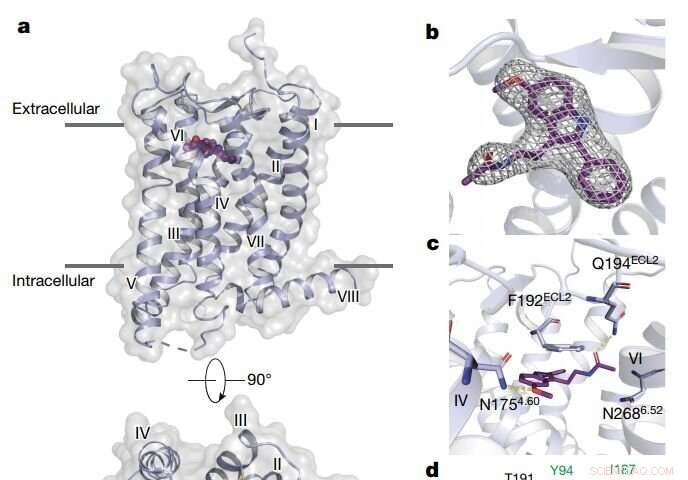
Oversigt over MT2-strukturen. Kredit: Natur (2019). DOI:10.1038/s41586-019-1144-0
Styring af rytmen
Når vores døgnrytme forstyrres, det kan føre til psykiatrisk, stofskifte, onkologiske og mange andre tilstande. Især MT1 spiller en vigtig rolle i at kontrollere disse rytmer, men det har vist sig vanskeligt at designe lægemidler, der selektivt kan målrette mod denne receptor. Mange mennesker tager over-the-counter melatonin kosttilskud for at bekæmpe søvnproblemer eller ændre deres døgnrytme, men virkningerne af disse lægemidler aftager ofte inden for få timer.
Ved at knække tegningerne af disse receptorer og kortlægge, hvordan ligander binder til og aktiverer dem, forskerne viste vejen for andre til at designe lægemidler, der er sikrere, mere effektiv og i stand til selektivt at målrette hver receptor.
"Siden opdagelsen af melatonin for 60 år siden, der har været mange skelsættende opdagelser, der førte til dette øjeblik, " sagde Margarita L. Dubocovich, en SUNY anerkendt professor i farmakologi og toksikologi ved universitetet i Buffalo, der var pioner inden for identifikation af funktionelle melatoninreceptorer i begyndelsen af 80'erne og gav et eksternt perspektiv på denne forskning. "På trods af bemærkelsesværdige fremskridt, opdagelsen af selektive MT1-lægemidler har været uhåndgribelig for mit team og forskere rundt om i verden. Belysningen af krystalstrukturerne for MT1- og MT2-receptorerne åbner et spændende nyt kapitel for udviklingen af lægemidler til behandling af søvn- eller døgnrytmeforstyrrelser, der vides at forårsage psykiatriske, stofskifte, onkologiske og mange andre tilstande."
Høst af krystaller
At kortlægge biomolekyler som proteiner, forskere bruger ofte en metode kaldet røntgenkrystallografi, at sprede røntgenstråler fra krystalliserede versioner af disse proteiner og bruge de mønstre, dette skaber, for at opnå en tredimensionel struktur. Indtil nu, udfordringen med at kortlægge MT1, MT2 og lignende receptorer var, hvor svært det var at vokse store nok krystaller til at opnå højopløsningsstrukturer.
"Med disse melatoninreceptorer, vi var virkelig nødt til at gå den ekstra mil, sagde Benjamin Stauch, der ledede strukturarbejdet på MT1. "Mange mennesker havde forsøgt at krystallisere dem uden held, så vi skulle være lidt opfindsomme."
En vigtig del af denne forskning var den unikke metode, forskerne brugte til at dyrke deres krystaller og til at indsamle røntgendiffraktionsdata fra dem. Til denne forskning, holdet udtrykte disse receptorer i insektceller og ekstraherede dem ved at bruge vaskemiddel. De muterede disse receptorer for at stabilisere dem, muliggør krystallisation. Efter at have renset receptorerne, de placerede dem i en membranlignende gel, som understøtter krystalvækst direkte fra membranmiljøet. Efter at have opnået mikrokrystaller suspenderet i denne gel, de brugte en speciel injektor til at skabe en smal strøm af krystaller, som de zappede med røntgenstråler fra LCLS.
"På grund af den lille krystalstørrelse, dette arbejde kunne kun udføres på LCLS, " sagde Vadim Cherezov, en USC-professor, der overvågede begge studier. "Sådanne små krystaller diffrakterer ikke godt ved synkrotronkilder, da de hurtigt lider af strålingsskader. Røntgenlasere kan overvinde strålingsskadeproblemet gennem 'diffraktion-før-destruktion'-princippet."
Forskerne indsamlede hundredtusindvis af billeder af de spredte røntgenstråler for at finde ud af den tredimensionelle struktur af disse receptorer. De testede også virkningerne af snesevis af mutationer for at uddybe deres forståelse af, hvordan receptorerne virker.
Ud over at opdage bittesmå, gatekeeping melatoninkanaler i receptorerne, forskerne var i stand til at kortlægge type 2-diabetes-associerede mutationer på MT2-receptoren, for første gang at se den nøjagtige placering af disse mutationer i receptoren.
At lægge grunden
I disse forsøg, forskerne så kun på forbindelser, der aktiverer receptorerne, kendt som agonister. At følge op på, de håber at kortlægge de receptorer, der er bundet til antagonister, som blokerer receptorerne. De håber også at bruge deres teknikker til at undersøge andre GPCR-receptorer i kroppen.
"Som strukturbiolog, det var spændende at se strukturen af disse receptorer for første gang og analysere dem for at forstå, hvordan disse receptorer selektivt genkender deres signalmolekyler, " sagde Cherezov. "Vi har kendt til dem i årtier, men indtil nu har ingen kunne sige, hvordan de rent faktisk ser ud. Nu kan vi analysere dem for at forstå, hvordan de genkender specifikke molekyler, som vi håber lægger grunden til det bedre, mere effektive lægemidler."
 Varme artikler
Varme artikler
-
 Tilfældig gang mellem varmebærere i amorfe polymerer(a) Diameterafhængigheden af termisk ledningsevne af polyimid -nanofibre. Romben repræsenterer eksperimentdata. Der er en dimensionel crossover af varmediffusion i molekylære kæder fra quasi-1D til
Tilfældig gang mellem varmebærere i amorfe polymerer(a) Diameterafhængigheden af termisk ledningsevne af polyimid -nanofibre. Romben repræsenterer eksperimentdata. Der er en dimensionel crossover af varmediffusion i molekylære kæder fra quasi-1D til -
 Stort gennembrud i fremstillingen af røde blodlegemerScanning elektronmikrografi af blodceller. Fra venstre mod højre:human erytrocyt, trombocyt (blodplader), leukocyt. Kredit:offentlig ejendom Forskere har genereret de første udødelige cellelinjer,
Stort gennembrud i fremstillingen af røde blodlegemerScanning elektronmikrografi af blodceller. Fra venstre mod højre:human erytrocyt, trombocyt (blodplader), leukocyt. Kredit:offentlig ejendom Forskere har genereret de første udødelige cellelinjer, -
 Touchscreen-alternativ dæmper frygten for verdensmangel på indiumDet nye materiale er skabt ved hjælp af en proces kaldet plasmasputtering. Kredit:Behnam Akhavan Har du nogensinde forestillet dig din smartphone eller tablet uden en berøringsskærm? Dette kan sna
Touchscreen-alternativ dæmper frygten for verdensmangel på indiumDet nye materiale er skabt ved hjælp af en proces kaldet plasmasputtering. Kredit:Behnam Akhavan Har du nogensinde forestillet dig din smartphone eller tablet uden en berøringsskærm? Dette kan sna -
 Kraftværker drevet af lysKredit:CC0 Public Domain Grønne planter, alger og nogle bakterier bruger sollys til at omdanne energi. Pigmenterne i klorofyl absorberer elektromagnetisk stråling, som fremkalder kemiske reaktione
Kraftværker drevet af lysKredit:CC0 Public Domain Grønne planter, alger og nogle bakterier bruger sollys til at omdanne energi. Pigmenterne i klorofyl absorberer elektromagnetisk stråling, som fremkalder kemiske reaktione
- Sydney og Naroomas hotspot for havopvarmning er mere end tre gange det globale gennemsnit
- Antarktishav er vært for en overraskende blanding af livsformer - og nu kan vi kortlægge dem
- Proba-V udsigt over Aralhavet
- John Lear og den mørke side
- Fakta om kvarts klipper
- Sporing af rumvirksomheder vil ændre regnskab, siger professor


