Den rettede evolution åbner døren til nye antibiotika
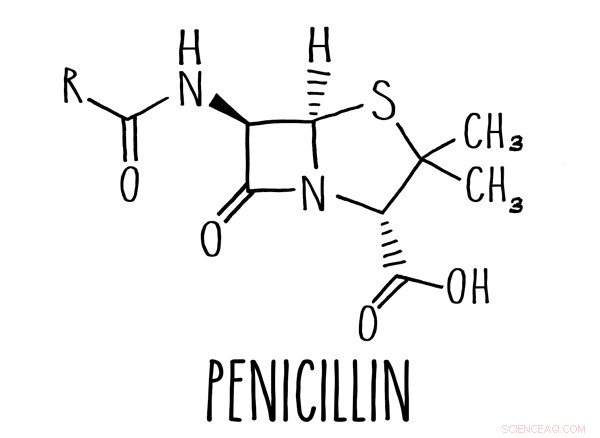
En beta-lactam ring er kernen i mange antibiotika, inklusive penicillin. Kredit:Caltech
I det igangværende våbenkapløb med mennesker og deres antibiotika på den ene side, og bakterier med deres evne til at udvikle forsvar mod antibiotika på den anden side, mennesker har fået en ny allieret - andre bakterier.
Mange almindelige antibiotika, inklusive det mest berømte antibiotikum, penicillin, er baseret på en molekylær struktur kendt som en beta-lactam ring. Disse stoffer, det passende navn beta-lactam antibiotika, forstyrre en bakteries evne til at bygge sin cellevæg.
Efterhånden som bakterier udvikler resistens over for eksisterende antibiotika, forskere og medicinalvirksomheder arbejder på at skabe nye. Det betyder, at der bliver gjort meget arbejde med at skabe nye slags beta-lactamer, og det er her Frances Arnolds laboratorium kommer ind i billedet.
Beta-lactamer fremstilles ved at tage et kædelignende molekyle og sløjfe det, lidt som at tage den ene ende af en snor og binde den i en knude til midten af snoren.
Den altoverskyggende udfordring er at kontrollere præcist, hvor langs molekylet reaktionen finder sted. Med traditionel syntetisk kemi, kemikere er nødt til at klæbe ekstra stykker på molekyler, som de ønsker at omdanne til beta-lactamer. Uden de ekstra stykker, knuderne vil ende med at blive bundet på inkonsekvente steder, hvilket resulterer i nogle løkker, der er store og nogle, der er små. Det er uønsket for nogen, der forsøger at fremstille en ensartet batch af antibiotika. Men tilføjelsen af disse ekstra stykker gør syntesen mere kompliceret, fordi der kræves yderligere trin for at tilføje dem og endnu flere trin for at fjerne dem, efter at sløjfen er fuldført.

En lactamring skabes ved at sløjfe et molekyle på sig selv, meget som at binde en løkke i et stykke snor. Kredit:Caltech
Kandidatstuderende Inha Cho og postdoktor Zhi-Jun Jia, begge fra Arnolds laboratorium, har udviklet noget enklere ved at bruge rettet evolution, en teknik udviklet af Arnold, Linus Pauling professor i kemiteknik, Bioteknik og biokemi, og direktør for Donna og Benjamin M. Rosen Bioengineering Center. I rettet evolution, som Arnold udviklede i 1990'erne, og som hun modtog Nobelprisen i kemi i 2018 for, enzymer udvikles i et laboratorium, indtil de opfører sig på den ønskede måde. Den genetiske kode for et nyttigt enzym overføres til bakterier som Escherichia coli. Efterhånden som bakterierne vokser, dele, og gå om deres liv, de udskiller enzymet.
I dette tilfælde, Cho og Jia tog et enzym kendt som cytochrom P450, som har været en alsidig arbejdshest i Arnold-laboratoriet, og udviklede det til at producere beta-lactamer. To andre versioner af enzymer blev også skabt til at konstruere andre ringstørrelser af lactamer. En version skaber en gamma-lactam, en sløjfe med fire carbonatomer og et nitrogenatom. Og den anden version skaber en delta-lactam, en sløjfe med fem carbonatomer og et nitrogenatom.
"Vi udvikler nye enzymer med aktivitet, der ikke kan findes i naturen, " siger Cho. "Lactamer kan findes i mange forskellige lægemidler, men især i antibiotika, og vi har altid brug for nye."
Jia påpeger, at de enzymer, de har skabt, også er utroligt effektive, med hvert molekyle af enzym, der er i stand til at producere op til en million beta-lactam molekyler. "De repræsenterer de mest effektive enzymer skabt i vores laboratorium, og er klar til industrielle anvendelser, " siger Jia.
Papiret, med titlen "Site-selektiv enzymatisk CH-amidering til syntese af forskellige lactamer" og medforfatter af Arnold, vises i 10. maj-nummeret af Videnskab .
 Varme artikler
Varme artikler
-
 Forskere skaber smart stål, 30% stærkereDjalal Mirzayev. Kredit:SUSU Forskere fra South Ural State University arbejder på at producere en innovativ, superlys, og superstærk slags stål kaldet bainit. Dette nye materiale har potentielle a
Forskere skaber smart stål, 30% stærkereDjalal Mirzayev. Kredit:SUSU Forskere fra South Ural State University arbejder på at producere en innovativ, superlys, og superstærk slags stål kaldet bainit. Dette nye materiale har potentielle a -
 Grøn brint:Hvorfor forbedres visse katalysatorer i drift?Mineralet erytrit består af kobolt- og arsenoxider med en molekylformel på (Co3(AsO4)2∙8H2O). Det er et modelsystem for en gruppe katalysatormaterialer, som forbedres med tiden. Kredit:CC BY 3.0, via
Grøn brint:Hvorfor forbedres visse katalysatorer i drift?Mineralet erytrit består af kobolt- og arsenoxider med en molekylformel på (Co3(AsO4)2∙8H2O). Det er et modelsystem for en gruppe katalysatormaterialer, som forbedres med tiden. Kredit:CC BY 3.0, via -
 En ny proces til fuld udnyttelse af bark af nåletræKredit:CC0 Public Domain I den finske mekaniske og kemiske skovbrugsindustri, tre millioner tons bark af nåletræ produceres årligt, bruges hovedsageligt til energiproduktion. Ved at bruge en metod
En ny proces til fuld udnyttelse af bark af nåletræKredit:CC0 Public Domain I den finske mekaniske og kemiske skovbrugsindustri, tre millioner tons bark af nåletræ produceres årligt, bruges hovedsageligt til energiproduktion. Ved at bruge en metod -
 Kemikalier, der absorberer fugtTørremidler er kemikalier, der let absorberer fugt fra den omgivende atmosfære eller tørrer den ud; disse kaldes også hygroskopiske forbindelser. Mange af dem er, selvom ikke alle, salte. De nyder en
Kemikalier, der absorberer fugtTørremidler er kemikalier, der let absorberer fugt fra den omgivende atmosfære eller tørrer den ud; disse kaldes også hygroskopiske forbindelser. Mange af dem er, selvom ikke alle, salte. De nyder en
- Udnyttelse af grafen-defekter
- Hvordan man forstår barometriske tryklæsninger
- Lab udvikler en hidtil uset langsigtet forudsigelsesmodel for naturbrande
- Fortjeneste op 10% hos Indias Infosys
- Gel bekæmper lægemiddelresistente bakterier og inducerer kroppens naturlige immunforsvar
- Karakteristika ved gode buffere


