Kunstige muskler drevet af glukose

Den kunstige muskel udviklet af forskere ved Linköpings Universitet består af polymermateriale, som forskerne har integreret enzymer i. En opløsning af glucose og oxygen i vand driver polymeraktuatoren, på samme måde som biologiske muskler. Kredit:Thor Balkhed/Linköpings universitet
Kunstige muskler fremstillet af polymerer kan nu drives af energi fra glukose og ilt, ligesom biologiske muskler. Dette fremskridt kan være et skridt på vejen til implanterbare kunstige muskler eller autonome mikrorobotter drevet af biomolekyler i deres omgivelser. Forskere ved Linköpings Universitet, Sverige, har præsenteret deres resultater i tidsskriftet Avancerede materialer .
Bevægelsen af vores muskler er drevet af energi, der frigives, når glukose og ilt deltager i biokemiske reaktioner. På lignende måde, fremstillede aktuatorer kan omdanne energi til bevægelse, men energien i dette tilfælde kommer fra andre kilder, såsom elektricitet. Forskere ved Linköpings Universitet, Sverige, ønskede at udvikle kunstige muskler, der fungerer mere som biologiske muskler. De har nu demonstreret princippet ved hjælp af kunstige muskler drevet af den samme glukose og ilt, som vores kroppe bruger.
Forskerne har brugt en elektroaktiv polymer, polypyrrol, som ændrer volumen, når en elektrisk strøm passeres. Den kunstige muskel, kendt som en "polymeraktuator, " består af tre lag:et tyndt membranlag mellem to lag elektroaktiv polymer. Dette design har været brugt i marken i mange år. Det virker, når materialet på den ene side af membranen får en positiv elektrisk ladning og ioner udstødes, får det til at skrumpe. På samme tid, materialet på den anden side får en negativ elektrisk ladning og ioner indsættes, hvilket får materialet til at udvide sig. Ændringerne i volumen får aktuatoren til at bøje i én retning, på samme måde som en muskel trækker sig sammen.

Forskere ved Linköpings universitet har vist, at kunstige muskler fremstillet af polymerer nu kan drives af energi fra glukose og ilt, ligesom biologiske muskler. Kredit:Thor Balkhed/Linköpings Universitet
Elektronerne, der forårsager bevægelse i kunstige muskler, kommer normalt fra en ekstern kilde, såsom et batteri. Men batterier lider af flere åbenlyse ulemper:de er normalt tunge, og skal oplades regelmæssigt. Forskerne bag undersøgelsen besluttede i stedet at bruge teknologien bag bioelektroder, som kan omdanne kemisk energi til elektrisk energi ved hjælp af enzymer. De har brugt naturligt forekommende enzymer, integrere dem i polymeren.
"Disse enzymer omdanner glucose og oxygen, på samme måde som i kroppen, at producere de elektroner, der kræves for at drive bevægelse i en kunstig muskel fremstillet af en elektroaktiv polymer. Der kræves ingen spændingskilde:det er nok blot at nedsænke aktuatoren i en opløsning af glukose i vand", siger Edwin Jager, lektor i sensor- og aktuatorsystemer, i Fysisk Institut, Kemi og biologi ved Linköpings universitet. Sammen med Anthony Turner, professor emeritus, han har ledet undersøgelsen.
Ligesom i biologiske muskler, glukosen omdannes direkte til bevægelse i de kunstige muskler.
"Da vi havde fuldt integrerede enzymer på begge sider af aktuatoren, og den faktisk flyttede - ja, det var bare fantastisk, " siger Jose Martinez, medlem af forskningsgruppen.
Det næste skridt for forskerne bliver at kontrollere de biokemiske reaktioner i enzymerne, sådan at bevægelsen kan være reversibel i mange cyklusser. De har allerede vist, at bevægelsen er reversibel, men de måtte bruge et lille trick for at gøre det. Nu vil de skabe et system, der er endnu tættere på en biologisk muskel. Forskerne ønsker også at teste konceptet ved hjælp af andre aktuatorer som "tekstilmusklen, "og anvende det i mikrorobotik.
"Glucose er tilgængelig i alle kroppens organer, og det er et nyttigt stof at starte med. Men det er muligt at skifte til andre enzymer, som ville gøre det muligt at bruge aktuatoren i, for eksempel, autonome mikrorobotter til miljøovervågning i søer. De fremskridt, vi præsenterer her, gør det muligt at drive aktuatorer med energi fra stoffer i deres naturlige omgivelser, " siger Edwin Jager.
 Varme artikler
Varme artikler
-
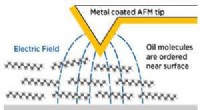 Endnu et skridt tættere på afstembare væskerDen skarpe, metalbelagt spids af en AFM kan anvende meget høje elektriske felter på tværs af flydende molekyler (i dette tilfælde en olie) lige ved siden af en overflade. Kredit:A*STAR Institute of
Endnu et skridt tættere på afstembare væskerDen skarpe, metalbelagt spids af en AFM kan anvende meget høje elektriske felter på tværs af flydende molekyler (i dette tilfælde en olie) lige ved siden af en overflade. Kredit:A*STAR Institute of -
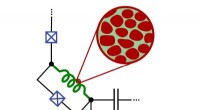 Granulært aluminium til fremtidige computereDen fluxonium-qubit, der indeholder granulært aluminium, kan forblive i en tilstand mellem 0 og 1 i en tid på op til 30 mikrosekunder (fig. Ioan Pop, SÆT) Computere baseret på kvantemekaniske prin
Granulært aluminium til fremtidige computereDen fluxonium-qubit, der indeholder granulært aluminium, kan forblive i en tilstand mellem 0 og 1 i en tid på op til 30 mikrosekunder (fig. Ioan Pop, SÆT) Computere baseret på kvantemekaniske prin -
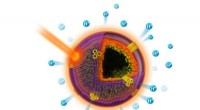 Høst energi fra lys ved hjælp af bioinspirerede kunstige cellerPlasmoniske kunstige celler dannes ved selvsamling af Au-Ag nanoroder i hule rum. Kredit:Billede med tilladelse fra Wiley-VCH (Angew. Chem. Int. Ed., 58, 4896 (2019)). Forskere designede og forban
Høst energi fra lys ved hjælp af bioinspirerede kunstige cellerPlasmoniske kunstige celler dannes ved selvsamling af Au-Ag nanoroder i hule rum. Kredit:Billede med tilladelse fra Wiley-VCH (Angew. Chem. Int. Ed., 58, 4896 (2019)). Forskere designede og forban -
 En ny måde at levere medicin på i MOF'erOrganometalliske rammer er som svampe. De kan indeholde meget store mængder medicin, og derefter pres det ud på det krævede tidspunkt. Kredit:Grzegorz Krzyzewski, IPC PAS Forskere fra Institute of
En ny måde at levere medicin på i MOF'erOrganometalliske rammer er som svampe. De kan indeholde meget store mængder medicin, og derefter pres det ud på det krævede tidspunkt. Kredit:Grzegorz Krzyzewski, IPC PAS Forskere fra Institute of
- Kemikere udvikler nyt materiale, der hjælper smart glas med at skifte farve på rekordtid
- Forståelse af enzymkaskader er nøglen til forståelse af stofskifte
- Det er faktisk ret vanskeligt at måle temperaturerne på røde giganter
- Sådan fremstilles en DNA-model ud af perler og halm <p> <p> Deoxyribonucleic acid (DNA) modeller be…
- Ny kilde til jordskælv og tsunamier i Greater Tokyo-regionen identificeret
- Antarktis sted lover at åbne et nyt vindue på kosmos


