Høst energi fra lys ved hjælp af bioinspirerede kunstige celler
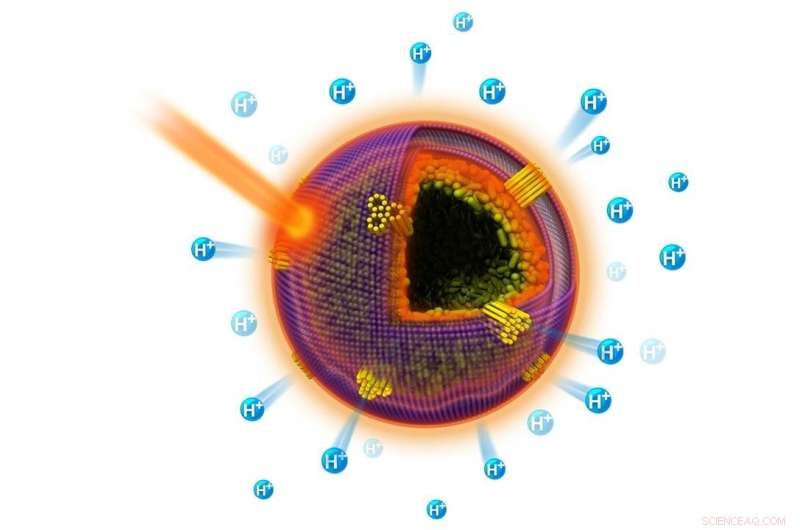
Plasmoniske kunstige celler dannes ved selvsamling af Au-Ag nanoroder i hule rum. Kredit:Billede med tilladelse fra Wiley-VCH (Angew. Chem. Int. Ed., 58, 4896 (2019)).
Forskere designede og forbandt to forskellige kunstige celler til hinanden for at producere molekyler kaldet ATP (adenosintrifosfat). ATP er den grundlæggende enhed, som alle levende ting bruger til at bære og levere energi til at køre processer i celler. Forskerne udviklede en gruppe kunstige celler, der genererer protoner, når den udsættes for lys. De udviklede også forskellige kunstige celler, der indeholder et enzym, der kan bruge disse protoner til at generere ATP. Holdet forbandt derefter de to celletyper sammen.
Dette kunstige celledesign bruger små stænger (nanoroder) lavet af sølv og guld til at skabe en biologisk cellevæg, der ligner dem i naturen. Disse stænger er i kontrast til lipiderne (såsom fedt og fedtsyrer), som biologiske celler bruger til at lave cellevægge. Disse nanoroder reagerer på lys på en måde, der fremskynder, hvor hurtigt visse proteiner kan producere protoner.
Nylige bestræbelser på at fremstille kunstige celler har membraner pakket med nanopartikler og samlet i en kolloid kapsel. Selve membransubstansen giver fordele, herunder afstembare porer, hvorigennem ioner kan passere. Imidlertid, membranmaterialet kan også påvirke iboende processer af interesse i de kunstige celler.
Udgivet i Angewandte Chemie International Edition , Studiet, "Light-Gated Synthetic Protocells for Plasmon-Enhanced Chemiosmotic Gradient Generation and ATP Synthesis" var designet til at udvikle en forståelse af sådanne effekter. Forskere ved Center for nanoskala materialer ved Argonne National Laboratory, en Department of Energy Office of Science brugerfacilitet, skabt lysreagerende kunstige celler ved hjælp af såkaldte plasmoniske materialer –nanosystemer, der kan interagere med lys på unikke måder-til de kolloidale kapsler.
Ud over, et lysporet protein bruges til at drive en fotoaktiveret synteseproces. De kunstige celler har et kolloid pakket med sølvguld (Au-Ag) nanoroder, der samler sig til kapsler. Desuden, Au-Ag nanoroderne opnår en plasmonresonans under visse lysforhold. Det lysaktiverede protein bakteriorhodopsin blev derefter fastgjort til kapselens overflade.
Bacteriorhodopsin blev valgt for sin evne til at transportere protoner hen over en membran under belysning. Bakterien hodopsin fanger lysenergi, bruger den energi til at pumpe protoner hen over membranen, og konverterer forskellene i protonkoncentrationer til kemisk energi.
Det celle-lignende potentiale i dette design blev yderligere demonstreret ved at udnytte protonerne som "kemiske signaler" til at udløse ATP-biosyntese i en sameksistent kunstig cellepopulation. I alt, de kunstige celler fungerer konsekvent med designmål. Den brede plasmonresonans af Au-Ag kolloidale kapsler øgede sandsynligheden for fotoreaktion af det lysaktiverede protein, og dermed skabe en ny lysstyrbar syntetisk "protocelle".
Den syntetiske protocellmodel giver muligheder for at udvikle alternative sol-til-kemiske energiomdannelsessystemer.
 Varme artikler
Varme artikler
-
 Teknologien bruger plantebiomasseaffald til selvdrevne biomedicinske enhederWenzhuo Wu, Ravi og Eleanor Talwar Rising Star, assisterende professor i industriteknik ved Purdues College of Engineering, er en innovator med fokus på at finde løsninger på tværs af flere discipline
Teknologien bruger plantebiomasseaffald til selvdrevne biomedicinske enhederWenzhuo Wu, Ravi og Eleanor Talwar Rising Star, assisterende professor i industriteknik ved Purdues College of Engineering, er en innovator med fokus på at finde løsninger på tværs af flere discipline -
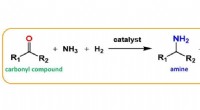 For meget aktive, bæredygtige katalysatorer, bare tilsæt fosforFig. 1. Reduktiv amination af carbonylforbindelser. Kredit:Osaka University Katalysatorer er afgørende for at gøre industrielle processer levedygtige. Imidlertid, mange af de ikke-ædelmetalkatalys
For meget aktive, bæredygtige katalysatorer, bare tilsæt fosforFig. 1. Reduktiv amination af carbonylforbindelser. Kredit:Osaka University Katalysatorer er afgørende for at gøre industrielle processer levedygtige. Imidlertid, mange af de ikke-ædelmetalkatalys -
 Forskere løser kontroverser om energigabet i Van der Waals-materialeTeYu Chien, en University of Wyoming lektor i fysik og astronomi, og Dinesh Baral, en UW kandidatstuderende, ledet forskning, der brugte scanning tunneling mikroskopi og spektroskopi målinger, der kla
Forskere løser kontroverser om energigabet i Van der Waals-materialeTeYu Chien, en University of Wyoming lektor i fysik og astronomi, og Dinesh Baral, en UW kandidatstuderende, ledet forskning, der brugte scanning tunneling mikroskopi og spektroskopi målinger, der kla -
 Ny metode til at løse plastiks bæredygtighedsproblemDr. Junpeng Wang. Kredit:University of Akron Bæredygtighed i plast er kommet langt i de seneste år, i høj grad takket være videnskabelige fremskridt. Men selvom plast bliver mere og mere miljøvenl
Ny metode til at løse plastiks bæredygtighedsproblemDr. Junpeng Wang. Kredit:University of Akron Bæredygtighed i plast er kommet langt i de seneste år, i høj grad takket være videnskabelige fremskridt. Men selvom plast bliver mere og mere miljøvenl
- Svovls livscyklus forudsiger placeringen af værdifulde mineraler
- Hvordan man laver en skummodel af jordarter Rotation
- Lenovo indregner et tab på 189 millioner dollars på et års tab ved engangsafskrivning
- Nyt syn på, hvordan havpumper påvirker klimaændringer
- Kina vil bygge et rumskib, der er kilometer langt
- Brandslukning skæmmer jorden. Californiens mandskab er ved at ordne det


