Molekylær konstruktion metalkoordinationsinteraktioner for stærke, hård, hurtigt genoprette hydrogeler
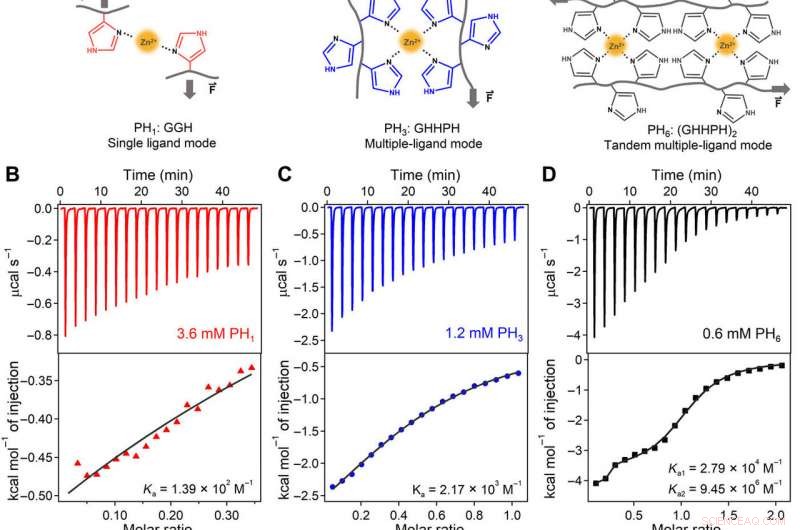
Kooperativ ingeniørvirksomhed, bindingskonstanter, og molekylær mekanisme af metalion-koordinationsinteraktioner på molekylært niveau for belastningsbærende. (A) Metalionkoordinationskomplekserne dannet af enkelte ligander (PH1, venstre) er dynamiske og svage. Når der dannes et metalchelateringssted lavet af flere ligander (PH3, midten), metalionbindingen bliver meget stærkere og mindre dynamisk end enkeltliganders. Desuden, når man arrangerer to metalcheleringssteder i tandem (PH6, ret), bindingsaffiniteten, mekanisk styrke, og tilknytningsraten kan forbedres på grund af samarbejdet mellem de to steder. (B til D) ITC-titreringsdata for PH1 (venstre), PH3 (midt), og PH1 (højre) peptider med ZnCl2 i 1 M tris buffer (pH 7,60, indeholdende 300 mM KCI) ved 25°C. (E) Zn2+-bindingskonstanter (Ka) for PH3 og muterede PH3-peptider. De muterede aminosyrer er fremhævet med rødt. Fejlbjælkerne repræsenterer tilpasningsfejlene. (F) Zn2+-bindingskonstanter for PH6 og muterede PH6-peptider. Venstre og højre paneler svarer til Ka1 og Ka2 for de to bindingssteder af PH6. Kun PH6- og (GHHGH)2-peptider udviste to bindingskonstanter. Resten af peptiderne viste single-site bindingskarakteristika. Fejlbjælkerne repræsenterer tilpasningsfejlene. (G til J) CD-spektre af (G) PH1:GGH; (H) PH3:GHHPH; (I) PH6:(GHHPH)2; og (J) (GHHGH)2-peptider i fravær og tilstedeværelse af Zn2+-ioner. Det relative indhold af PPII-strukturer af PH1 og PH3 er 9,6 og 34,2% baseret på højden af den store CD-top ved 205 nm, forudsat at PH6-Zn2+ komplekset viser 100 % PPII spiralstruktur. (K) Skematisk illustration af den kooperative Zn2+-bindingsmekanisme af PH6. Den konformationelle ændring af det første koordinationssted fører til strukturelle ændringer af det andet til en konformation, der mere favoriserer Zn2+-binding. N/A, ikke anvendelig. Kredit:Science Advances, doi:10.1126/sciadv.aaz9531
Bærebærende væv såsom muskler og brusk viser typisk høj elasticitet, sejhed og hurtig genopretningshastighed. Imidlertid, at kombinere sådanne mekaniske egenskaber i laboratoriet for at bygge syntetiske biomaterialer er fundamentalt udfordrende. I en ny undersøgelse, der nu er offentliggjort på Videnskabens fremskridt , Wenxu Sun og et forskerhold i fysik, ingeniørmekanik og smarte enheder i Kina, udviklet en stærk, sej og hurtig restituerende hydrogel. Holdet konstruerede materialet ved hjælp af tværbindere med samvirkende dynamiske interaktioner. De designede et histidinrigt decapeptid (10 aminosyrekæde) indeholdende to tandem (konsekutive) zink (Zn) bindende motiver for at lette termodynamisk stabilitet, stærkere bindingsstyrke og hurtigere bindingshastighed af konstruktionen, sammenlignet med enkeltbindende proteinmotiver eller isolerede ligandproteiner. De konstruerede hybridnetværkshydrogeler med peptidzinkkomplekset udviste høj stabilitet, sejhed og hurtig restitution på få sekunder. Forskerholdet forventer, at stilladserne effektivt kan håndtere bærende vævstekniske applikationer og fungere som byggesten til blød robotteknologi. De nye resultater giver en generel vej til at tune mekaniske og dynamiske egenskaber af hydrogeler på molekylært niveau.
Når vi går, vores muskler, brusk og sener udsættes for betydelige mekaniske belastninger, men biologiske væv kan komme sig hurtigt for at fungere pålideligt i mange mekaniske cyklusser. Bioingeniører har udforsket bløde hydrogeler med muskellignende mekaniske egenskaber som biomekaniske aktuatorer, syntetisk brusk, kunstige muskler, ionisk hud og i blød robotteknologi. De har viet mange bestræbelser på at forbedre den mekaniske styrke og sejhed af hydrogeler ved at indføre specielle energiafledningsmekanismer. Hurtig restitution er også en unik egenskab for bærende blødt væv, bortset fra mekanisk styrke og sejhed, men syntetiske hydrogeler mangler stadig en mekanisme til hurtig genopretning. For eksempel, traditionelle dobbeltnetværk (DN) eller hybridnetværk (HN) hydrogeler med korte polymerkæder som offernetværk kan typisk ikke komme sig hurtigt - ofte tager det fra minutter til dage.
Styrken af en hydrogel afhænger af levetiden af dens tværbindere, hvor langsom binding/afbindingskinetik fører til stærke hydrogeler, mens hurtige valutakurser giver bløde. For at opnå høj styrke og sejhed skal tværbinderne være langsomme, men for at opnå hurtig bedring, tværbinderne skal være dynamiske med høje frekvenser af association og dissociation. For at overvinde denne modsigelse, naturligt forekommende bærende materialer har brugt kooperativitet af svage interaktioner. I dette arbejde, Sun et al. tilsvarende manipulerede hybridnetværk (HN) hydrogeler med et specifikt designet peptid-metal kompleks som den fysiske tværbinder. Holdet dannede effektive metalbindingssteder i en peptidsekvens for at konstruere hydrogeler med de nødvendige egenskaber.
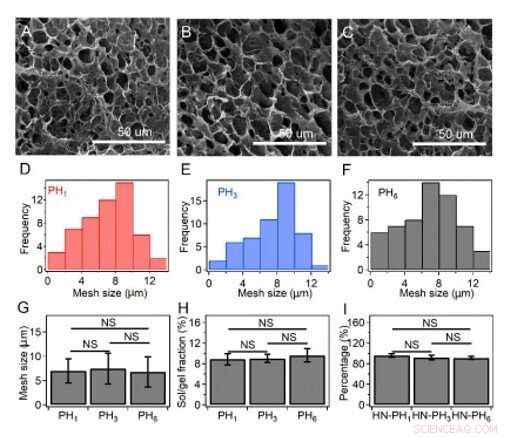
Maskestørrelse, sol/gel fraktioner, og den faktiske procentdel af peptider, der inkorporeres i hydrogel-netværket. (A-C) SEM-billeder af HN-PH1-gelen (A), HN-PH3-gelen (B) og HN-PH3-gelen (C) før tilsætning af Zn2+-ioner. (D-F) Maskestørrelsesfordelinger af HNPH1-gelen (D), HN-PH3 gel (E) og HN-PH6 gel (F) estimeret ud fra SEM-billederne ved hjælp af ImageJ-softwaren. (G) Gennemsnitlig maskestørrelse af HN-PHn-geler i fravær af Zn2+-ioner. (H) Sol/gel-fraktioner af forskellige HN-PHn-geler før tilsætning af zink. (I) Den procentdel af peptider, der er inkorporeret i hydrogel-netværket. De indledende peptidkoncentrationer var 0,3 M, 0,10 M, og 0,05 M for PH1, PH3, og PH6, henholdsvis. Procentdelen af peptiderne, der blev inkorporeret i hydrogelerne, var ens, som estimeret ved at trække fraktionen af eluerede peptider fra den samlede anvendte mængde. Fejlbjælker angiver middelværdien ± S.D. NS:p> 0,05. Kredit:Science Advances, doi:10.1126/sciadv.aaz9531
Holdet designet først tre korte histidinrige peptider (HR-peptider) som ligander til at binde med zinkioner (Zn) 2+ og konstruer HN-hydrogeler. De betegnede peptidsekvenserne som PH 1 , PH 3 og PH 6 baseret på antallet af forbundne histidiner. Sun et al. syntetiserede peptiderne ved hjælp af fastfase peptidsyntese og oprensede det med højtydende væskekromatografi. De observerede dannelsen af Zn 2+ histidin koordinationskomplekser ved hjælp af ultraviolet (UV) og Raman spektroskopi. Den specifikt designede peptidsekvens tillod synergistisk og samarbejdsvillig Zn 2+ bindende affinitet, sammenlignet med peptider med tilfældige histidinrester på deres sekvenser. Forskerne studerede den molekylære mekanisme for kooperativ zinkionbinding til PH 6 ved hjælp af cirkulær dikroisme, resultaterne tyder på konforme ændringer af det første koordinationssted for PH 6 at være kritisk for kooperativ binding og viste, hvordan strukturelle ændringer favoriserede yderligere Zn 2+ bindende.
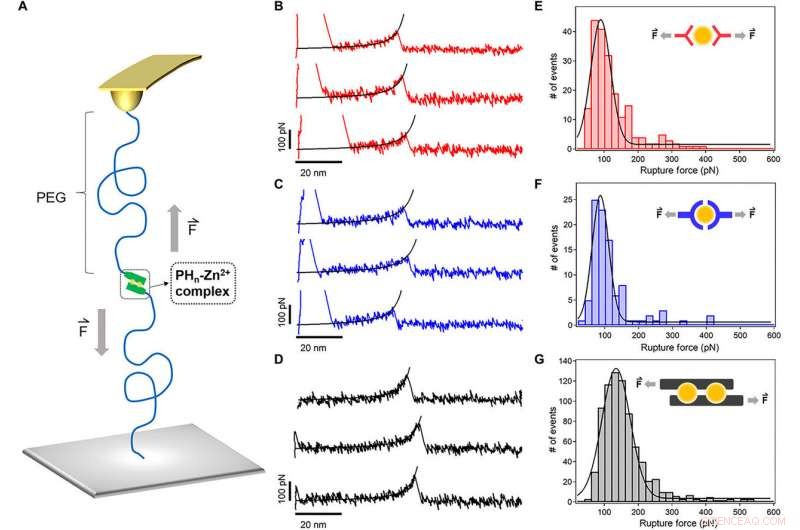
Enkeltmolekyle kraftspektroskopi af metalionkoordinationskomplekserne. (A) Skematisk diagram af de AFM-baserede enkelt-molekyle kraftspektroskopi eksperimenter. Peptidliganderne blev bundet til cantilever-spidsen og substratet via en PEG-linker (MW, 5 kDa). (B til D) Typiske kraftforlængelseskurver for brud på PH1-Zn2+ (rød), PH3-Zn2+ (blå), og PH6-Zn2+ (sort) komplekser ved en trækhastighed på 1000 nm s−1. Ormlignende kædetilpasning af kraftforlængelseskurverne (sorte linjer) bekræftede, at toppen ved en forlængelse på ~50 nm svarer til brud på en enkelt metalion-chelatbinding. (E til G) Brudkrafthistogrammerne for PH1-Zn2+ (rød), PH3-Zn2+ (blå), og PH6-Zn2+ (sort), henholdsvis. Gauss-fittingen viser de gennemsnitlige brudkræfter på 90 ± 29, 87 ± 24, og 135 ± 41 pN, henholdsvis. De foreslåede Zn2+ ionbindingsmåder for de tre peptider er vist i de indsatte. Kredit:Science Advances, doi:10.1126/sciadv.aaz9531
Sun et al. brugte avancerede teknikker såsom atomkraftmikroskopi (AFM)-baseret enkelt-molekyle kraftspektroskopi (SMF'er) til at måle den mekaniske stabilitet af HR-peptid-Zn 2+ komplekser, dvs. tværbindere af hydrogelen på molekylært niveau. De gennemsnitlige brudkræfter var meget højere for PH 6 sammenlignet med andre typer hydrogeler, bekræfter hydrogelens sejhed. The results showed that the mechanical stability of the metal-ligand complexes could be improved considerably based on the binding sites.
The team explored if changes to the intrinsic properties of crosslinkers could alter macroscopic mechanical properties of the hydrogel by preparing a series of hybrid network (HN) hydrogels. They used HR-peptide-Zn 2+ as sacrificial crosslinkers and covalent bonds as permanent crosslinkers in the constructs and named the resulting hydrogels as HN-PH 1 , HN-PH 3 , and HN-PH 6 , based on the peptide sequence used. The network structures were similar in all three hydrogels but the HN-PH 6 gel was more compressible compared to the others, while functioning effectively under stressful mechanical environments. Interessant nok, the scientists could even twist the HN-PH 6 hydrogel into a spiral shape and compress the material with a sharp blade without causing it permanent damage.

Compressing the HN-PH6 hydrogel using a sharp blade does not damage the material. Credit:Science Advances, doi:10.1126/sciadv.aaz9531
The team conducted tensile mechanical tests on the gels and correlated the results on the bulk level with those at the molecular level, to show remarkably higher break strain, Young's modulus and toughness for the HN-PH 6 gels. Sun et al. then examined the recovery property of the material based on loading-unloading cycles and found HN-PH 6 gels to almost totally recover its macroscopic mechanical properties in minutes. Imidlertid, if they cut up the HN-PH 6 gels into pieces, the hydrogel could not self-heal since covalent crosslinkers do not reform after fracture. To understand the experimental outcomes, the research team also conducted theoretical analyses and proposed cooperative zinc binding on PH 6 to be an important factor, among other factors to form strong and tough hydrogels with fast recovery rates.
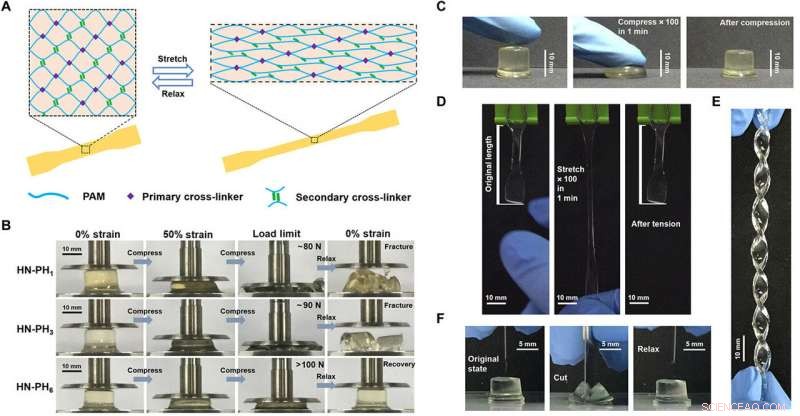
Structure and properties of HN-PHn HN hydrogels cross-linked by the peptide-Zn2+ coordination complexes. (A) Schematic illustration of the network structure of HN-PHn hydrogels. The network comprises covalent bonds as the primary cross-linkers and ligand-metal interactions as the secondary cross-linkers. (B) Optical images of the HN-PH1 (top), HN-PH3 (middle), and HN-PH6 (bottom) hydrogels under a compression-relaxation cycle. The HN-PH1 and HN-PH3 gels were fractured, whereas the HN-PH6 gel was almost fully recovered. (C) Optical images of the HN-PH6 gel under an extreme compressive condition (compressed to>70% strain for 100 times at 1.6 Hz). (D) Optical images of the HN-PH6 gel under an extreme tensile condition (stretched to>150% strain for 100 times at 1.6 Hz). (E) Optical image of the HN-PH6 gel twisted into a spiral shape. (F) Optical images of the HN-PH6 gel compressed with a sharp blade and relaxed. No detectable cut was observed on the gel. PAM, polyacrylamide. Photo credits:Wenxu Sun, Nanjing University. Credit:Science Advances, doi:10.1126/sciadv.aaz9531
På denne måde Wenxu Sun and colleagues developed a novel hydrogel material, bioinspired by histidine residues found in natural load-bearing materials. Combining such outstanding mechanical properties in the lab has remained a challenge due to the inability to effectively harness the unique metal ion binding properties that are encoded in natural proteins. In this work, Sun et al. used bioinspired Zn 2+ -binding peptide as crosslinkers to form the desired hydrogels at the molecular level, highlighting the importance of cooperative metal coordination during materials synthesis. They intend to examine additional mechanical features, such as adhesion to other tissues, before conducting practical applications in tissue engineering.
© 2020 Science X Network
 Varme artikler
Varme artikler
-
 Marshmallow-lignende silikonegeler brugt som isolering i beholdere til kryokonserverede embryonerFoto af containeren, der pakker en MG. Kredit:Gen Hayase Da den genetiske modifikation af mus er mere og mere udbredt i medicinsk og biologisk forskning, så, også, er behovet for en effektiv måde
Marshmallow-lignende silikonegeler brugt som isolering i beholdere til kryokonserverede embryonerFoto af containeren, der pakker en MG. Kredit:Gen Hayase Da den genetiske modifikation af mus er mere og mere udbredt i medicinsk og biologisk forskning, så, også, er behovet for en effektiv måde -
 Oliefangende svamp kan opsuge rester fra offshore-boringerKredit:CC0 Public Domain Boring og fracking efter olie under havbunden producerer 100 milliarder tønder olieforurenet spildevand hvert år ved at frigive små oliedråber i omgivende vand. De fleste
Oliefangende svamp kan opsuge rester fra offshore-boringerKredit:CC0 Public Domain Boring og fracking efter olie under havbunden producerer 100 milliarder tønder olieforurenet spildevand hvert år ved at frigive små oliedråber i omgivende vand. De fleste -
 En fremtid med nyttige konstruerede levende maskiner?Ny blød, mekaniske metamaterialer kan tænke over, hvordan kræfter påføres det og reagere via forprogrammerede reaktioner. Kredit:Jennifer M. McCann / Elizabeth Flores-Gomez Murray, Penn State MR K
En fremtid med nyttige konstruerede levende maskiner?Ny blød, mekaniske metamaterialer kan tænke over, hvordan kræfter påføres det og reagere via forprogrammerede reaktioner. Kredit:Jennifer M. McCann / Elizabeth Flores-Gomez Murray, Penn State MR K -
 Trækker, ikke skubbe, silke kunne revolutionere, hvordan grønnere materialer fremstillesSilkeorm trækker silke fra sin krop. Kredit:University of Sheffield. Ny indsigt i, hvordan dyr spinder silke, kan føre til nye, grønnere måder at fremstille syntetiske fibre på, ifølge akademikere
Trækker, ikke skubbe, silke kunne revolutionere, hvordan grønnere materialer fremstillesSilkeorm trækker silke fra sin krop. Kredit:University of Sheffield. Ny indsigt i, hvordan dyr spinder silke, kan føre til nye, grønnere måder at fremstille syntetiske fibre på, ifølge akademikere
- Musk slipper for det værste, men Tesla står stadig over for en ujævn vej
- Ny kontrolstrategi hjælper med at høste maksimal effekt fra vindmølleparker
- Pacific Northwest seler til rekordstor hedebølge
- Curiosity Mars rover tager en ny selfie før rekordstigning
- Forebyggelse bedre end helbredelse for at forhindre unge brugere i at blive involveret i cyberkrimin…
- Video:Hvordan laves læder?


