Forskere hæmmer kræftcellevækst ved hjælp af forbindelser, der beskytter planter mod rovdyr
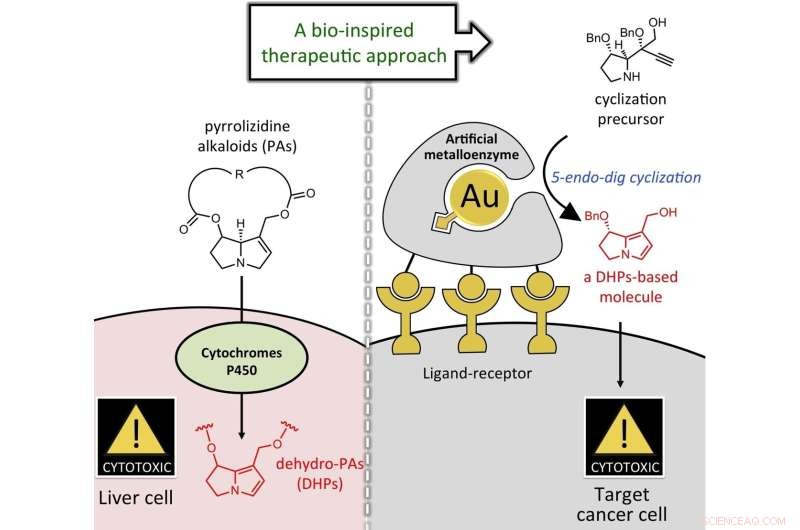
Grafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202205541
Forskere i Japan har haft held med at hæmme kræftcellevækst ved hjælp af pyrrolizidinalkaloid, en bestanddel af planteoprindelse, der tidligere blev anset for at være for giftig til at administrere.
Pyrrolizidinalkaloider findes i omkring 6.000 plantearter, herunder tusindfryd- og bønnefamilierne. Hos planter beskytter de planter mod rovdyr; Men hos mennesker har de antibakterielle og antitumoregenskaber, hvilket gør dem nyttige til urtemedicin. Tidlige undersøgelser rapporterede, at pyrrolizidinalkaloider kunne dræbe kræftceller, men forskningen blev opgivet, fordi de også forårsagede leverskade.
"Problemet med at være giftig for leveren er uadskilleligt fra aktivitetsmekanismen for pyrrolizidinalkaloider," forklarer hovedforfatter professor Satoshi Yokoshima. "Pyrrolizidinalkaloider viser kun toksicitet, når de metaboliseres i kroppen og omdannes til deres 'aktive form' indeholdende pyrrolstrukturen. Den aktive form beskadiger kræftcellens DNA, forhindrer den i at formere sig, men den gør dem også skadelige for nukleinsyrer og proteiner i leveren."
Professor Yokoshima fra Graduate School of Pharmaceutical Science, Nagoya University, undersøgte sammen med professor Katsunori Tanaka fra Tokyo Institute of Technology og RIKEN muligheden for at hæmme cancercelleproliferation uden toksicitet. Forskerne administrerede en molekylær forløber for pyrrolizidinalkaloid med en anden struktur. Derefter konverterede de det til den aktive krop, der indeholdt pyrrolstrukturen nær kræftceller for at minimere skader. Deres resultater blev offentliggjort i Angewandte Chemie International Edition .
"Jeg er interesseret i strukturen af naturlige produkter," forklarer professor Yokoshima. "Det er sjovt at syntetisere dem. Vi ser måske noget nyt i organisk kemi eller udvikler en ny metode. I dette eksperiment har vi designet en ny forbindelse med en anden struktur som forløber for den aktive form. Da det ikke skadede kroppen , introducerede vi det og konverterede det derefter til den aktive form ved hjælp af en guldkatalysator i nærvær af kræft."
For at introducere guldkatalysatorer i kroppen henvendte holdet sig til professor Tanaka fra RIKEN, som havde støttet en guldkatalysator på albumin, et protein, der findes i blod. De introducerede også flere sukkerkæder til overfladen af albumin, idet de udnyttede det faktum, at sukkerkæder genkender overfladen af kræftceller. Albuminet blev bundet til kræftcellerne, og reaktionen fandt sted tæt på kræftcellerne, hvilket begrænsede skaden på andre celler.
Holdet bekræftede konverteringen til den aktive form indeholdende pyrrolstrukturen. Dette var bevis på "syntese på stedet", hvilket betyder, at den aktive form blev skabt nær kræftceller for at begrænse skader på kroppen. De bekræftede også bemærkelsesværdig væksthæmning af de målrettede cancerceller.
"Pyrrolizidinalkaloider er giftige for leveren, men denne metode kan undgå toksicitet," siger professor Yokoshima. "Hvis vi kan anvende dette in vivo, kan det være en ny metode til kræftbehandling. Vi håber, at andre potentielle kræftbehandlinger, der blev afbrudt på grund af toksicitetsproblemer, kan testes igen som potentielle behandlinger ved hjælp af syntesemetoden på stedet. Jeg håber denne metode vil give indsigt, som andre kan bruge til at lave deres egne stoffer." + Udforsk yderligere
Aktivering af prodrug ved hjælp af proteinindkapslet guldkatalysator
 Varme artikler
Varme artikler
-
 Forskere identificerer atomstruktur af katalytisk aktiv kobber-ceria-grænsefladeAtomstruktur af kobber-ceria-grænsefladen Kredit:DICP For nylig, Dr. Zhou Yan og prof. Shen Wenjie ved Dalian Institute of Chemical Physics (DICP) fra det kinesiske videnskabsakademi og deres sama
Forskere identificerer atomstruktur af katalytisk aktiv kobber-ceria-grænsefladeAtomstruktur af kobber-ceria-grænsefladen Kredit:DICP For nylig, Dr. Zhou Yan og prof. Shen Wenjie ved Dalian Institute of Chemical Physics (DICP) fra det kinesiske videnskabsakademi og deres sama -
 Hybridmateriale flytter næste generations transportbrændstofceller tættere påUltrahøj protonkonduktion i polyoxometalatbaseret ramme Billedtekst:Ultrahøj protonkonduktion via udvidet hydrogenbindingsnetværk i polyoxometalatbaseret ramme, der er funktionaliseret med Lanthanide
Hybridmateriale flytter næste generations transportbrændstofceller tættere påUltrahøj protonkonduktion i polyoxometalatbaseret ramme Billedtekst:Ultrahøj protonkonduktion via udvidet hydrogenbindingsnetværk i polyoxometalatbaseret ramme, der er funktionaliseret med Lanthanide -
 Gør det krystalklart:Krystallinitet reducerer modstanden i all-solid-state batterierKredit:Taro Hitosugi og Tokyo Institute of Technology Forskere ved Tokyo Institute of Technology har undersøgt mekanismerne bag modstanden ved elektrode-elektrolyt-grænsefladen på hel-solid-state
Gør det krystalklart:Krystallinitet reducerer modstanden i all-solid-state batterierKredit:Taro Hitosugi og Tokyo Institute of Technology Forskere ved Tokyo Institute of Technology har undersøgt mekanismerne bag modstanden ved elektrode-elektrolyt-grænsefladen på hel-solid-state -
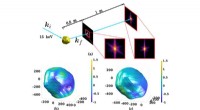 Ny beregningsteknik løser komprimerede røntgendataSkematisk (øverst) viser Braggs kohærente diffraktionsbilleddannelsesfaseindhentning af røntgenstråler spredt af en guldnanopartikel. To rekonstruktioner af guldnanopartiklen er vist forneden. Kredit:
Ny beregningsteknik løser komprimerede røntgendataSkematisk (øverst) viser Braggs kohærente diffraktionsbilleddannelsesfaseindhentning af røntgenstråler spredt af en guldnanopartikel. To rekonstruktioner af guldnanopartiklen er vist forneden. Kredit:
- Ud over bundlinjen:Investorer favoriserer virksomheder, der giver tilbage
- Nye globale migrationsestimater viser, at raterne har været stabile siden 1990, høj tilbagevenden …
- Jordforbindelse (fysik): Hvordan fungerer det og hvorfor er det vigtigt?
- Magnetiske nanopartikler til samtidig diagnosticering, overvåge og behandle
- Team udvikler ny måde at studere nanopartikler på
- Et nyt spintronisk fænomen:Chiral-spin rotation fundet i ikke-kollineær antiferromagnet


