Afsløret manglende trin i lipiddannelsen kunne muliggøre påvisning af tidligere klimaer
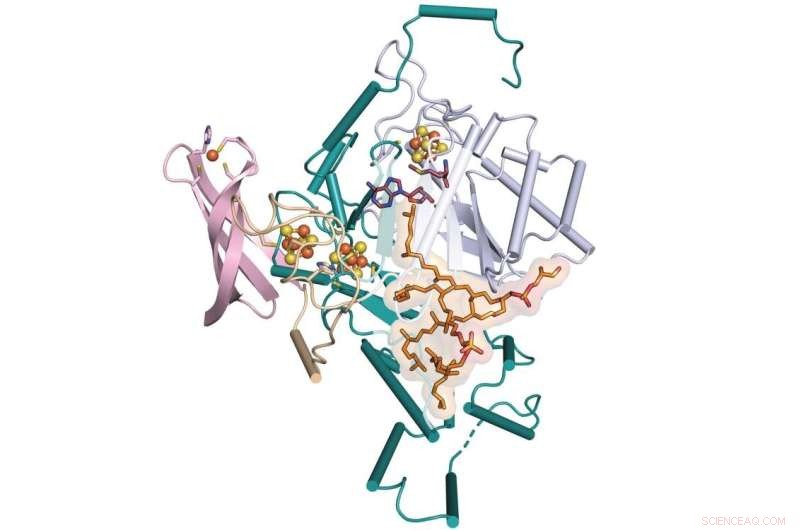
Et team fra Penn State og University of Illinois Urbana-Champaign har fastslået det manglende trin i dannelsen af et molekyle kaldet GDGT, som er en lovende kandidat til brug som en indikator for tidligere klima. Holdet bestemte røntgenkrystalstrukturen af et enzym, der letter denne proces kaldet GDGT/MAS - vist her bundet til yderligere cofaktorer. Kredit:Booker Lab / Penn State
Det manglende trin i dannelsen af et lipidmolekyle, der gør det muligt for visse encellede organismer at overleve de mest ekstreme miljøer på Jorden, er nu blevet dechifreret. Denne nye forståelse, afdækket af et team af biokemikere fra Penn State og University of Illinois Urbana-Champaign, kunne forbedre lipidernes evne til at blive brugt som en indikator for temperatur over geologisk tid.
Lipidet, kaldet glycerol dibiphytanyl glycerol tetraether (GDGT), findes i cellemembranen af nogle arter af archaea, encellede organismer, der oprindeligt blev anset for at være bakterier, men nu betragtes som en separat gruppe. Dette lipid giver stabilitet for nogle arter til at trives i miljøer med ekstremt høje temperaturer, saltholdighed eller surhedsgrad, såsom termiske åbninger i havet, varme kilder og hypersaltholdige vande. Den unikke stabilitet af GDGT gør det også muligt at detektere det hundreder eller endda tusinder af år efter, at organismen dør. Fordi disse organismer har tendens til at producere mere GDGT ved højere temperaturer, betragtes det som en lovende kandidat til at estimere temperatur over geologisk tid.
"For at GDGT kan bruges nøjagtigt som en proxy til at rekonstruere ændringer i geologiske temperaturer, skal forskerne bedre forstå, hvordan det er lavet, hvilke gener der koder for det, og hvilke arter der kan skabe det," siger Squire Booker, en biokemiker ved Penn State , en efterforsker ved Howard Hughes Medical Institute og leder af forskerholdet. "Men indtil nu har der manglet et trin i dannelsen af dette lipid. Vi brugte billeddannelsesteknikker kombineret med kemiske og biokemiske metoder til at dekonstruere den kemiske vej for dette manglende trin."
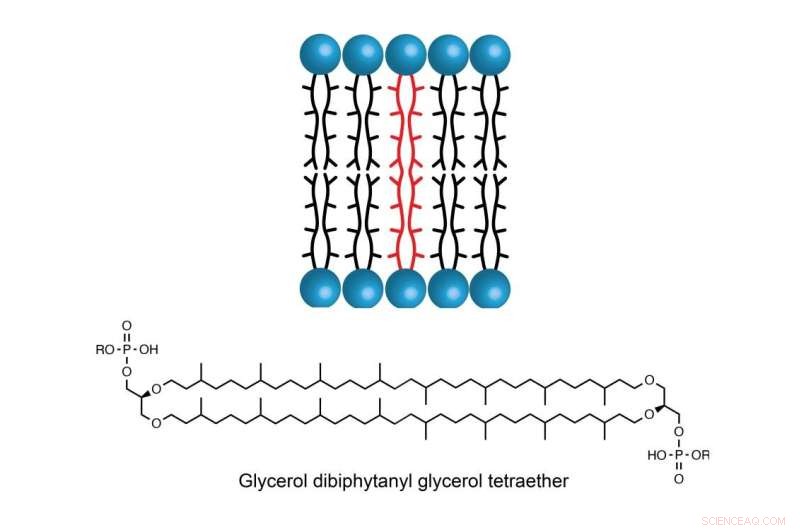
Molekylet GDGT findes i cellemembranen hos nogle arter af archaea, hvilket gør det muligt for de encellede organismer at trives i miljøer med ekstremt høje temperaturer, saltholdighed eller surhedsgrad. Kredit:Booker Lab / Penn State
GDGTs stabilitet skyldes til dels dets to lange kulbrintekæder, der strækker sig gennem membranen. Men hvordan disse to kæder bliver knyttet sammen, har forbløffet videnskabsmænd i årtier.
"At koble carbonerne for enden af de to carbonhydridkæder er en virkelig udfordrende kemi, fordi de er inerte - de er kemisk inaktive," sagde Cody Lloyd, en kandidatstuderende ved Penn State og medlem af forskerholdet. "Vi har identificeret det enzym, der aktiverer disse terminale kulstofatomer og gør denne kobling mulig. Derudover kender vi nu genet, der koder for dette enzym, hvilket skulle forbedre brugen af GDGT som en indikator for tidligere klimaer."
Enzymet, der letter koblingen af de to kulbrintekæder, tilhører en klasse af proteiner kaldet radikale SAM-proteiner, som vides at spille en vigtig rolle i en række kemiske reaktioner, herunder produktion af antibiotika, modifikation af proteiner, DNA og RNA, og skabelsen af forskellige biomolekyler.
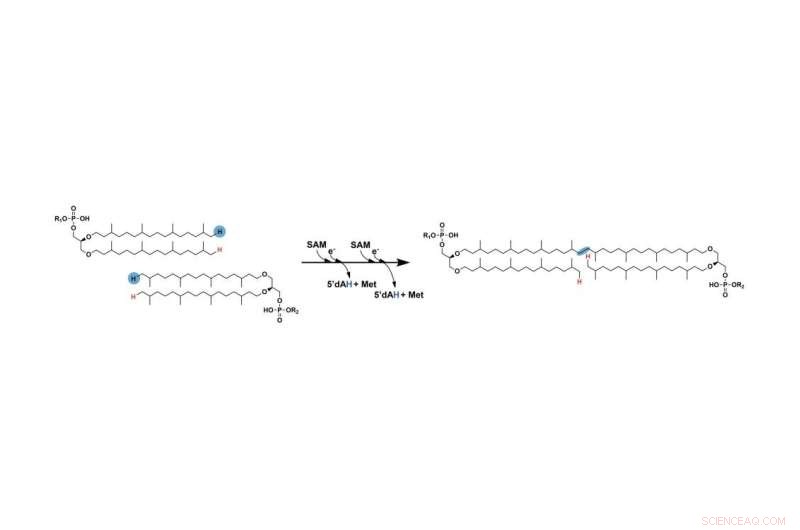
Det tidligere manglende trin i dannelsen af GDGT involverer at forbinde to lange kulbrintekæder. De to hydrogener markeret med blåt fjernes i sidste ende, og kæderne forbindes i sidste ende på de steder, hvor disse atomer blev fjernet. Et radikalt SAM-enzym letter denne proces. Kredit:Booker Lab / Penn State
Det første trin ligner det for andre reaktioner, der involverer radikale SAM-enzymer:radikale SAM-enzymet bruger en af sine jern-svovl-klynger til at spalte et molekyle kaldet S-adenosyl-L-methionin (SAM), hvilket producerer et "frit radikal" eller en uparret elektron, der er meget reaktiv og hjælper med at bevæge reaktionen fremad. Derefter plukker radikalet et brintatom fra kulstoffet i enden af kæden. På et senere trin gentages denne proces med den anden kæde under anvendelse af et andet SAM-molekyle.
"I sidste ende ender kulstofatomerne i enden af hver af kæderne med at binde til hinanden på den position, hvor brintatomerne blev fjernet," sagde Lloyd. "Men når først brinten på den første kæde er fjernet, bliver det så ustabilt, at det kan reagere med stort set hvad som helst. For midlertidigt at forhindre den første kæde i at reagere med eventuelle off-targets, binder kulstoffet sig til et svovlatom fra et andet af enzymets tre jern-svovl-klynger."
Når først brinten er blevet fjernet fra den anden kæde, tilskynder det resulterende radikal den første kæde til at fjerne sig selv fra jern-svovl-klyngen på enzymet og i stedet binde sig til den anden kæde. Dette resulterer i, at de to kæder bindes sammen, og fuldender det manglende trin i GDGTs dannelse. Forskerne præsenterer deres resultater i et papir, der vises online og på tryk i 1. september-udgaven af tidsskriftet Nature .
"Dette er en helt ny anvendelse af en jern-svovl-klynge, og dette er det første eksempel i naturen på koblingen af to fuldstændigt inerte carbonatomer med denne elektronkonfiguration, som kemikere kalder sp3 hybridiseret," sagde Booker. "Der har været stor interesse for at skabe den slags carbon-carbon-bindinger ud fra sp3-hybridiserede carboner som en del af lægemidler og andre industrielle produkter. Naturen har haft millioner af år til at finde ud af disse ting, så vi fortsætter med at se til naturen til inspiration til syntetiske reaktioner - som denne nye brug af en jern-svovl-klynge." + Udforsk yderligere
Nøglen til et kraftigt antibiotikums dannelse er nu klar
 Varme artikler
Varme artikler
-
 En laserteknik viser sig effektiv til at genvinde materiale designet til at beskytte industriprodukt…Kredit:CC0 Public Domain Fluorpolymerer er makromolekyler, der består af carbon og fluor, som, på grund af deres egenskaber, tendens til at blive brugt som non-stick og antikorrosive belægninger p
En laserteknik viser sig effektiv til at genvinde materiale designet til at beskytte industriprodukt…Kredit:CC0 Public Domain Fluorpolymerer er makromolekyler, der består af carbon og fluor, som, på grund af deres egenskaber, tendens til at blive brugt som non-stick og antikorrosive belægninger p -
 Aktive flydende krystalsystemer undersøgt i jagten på autonome materialesystemerSimuleringsøjebliksbillede af en selvkørende topologisk defekt i en aktiv flydende krystal styret af et lysmønster (skinnede i lyserødt område). Kredit:Prof. Zhang Rui, HKUST Liquid Crystals (LC)
Aktive flydende krystalsystemer undersøgt i jagten på autonome materialesystemerSimuleringsøjebliksbillede af en selvkørende topologisk defekt i en aktiv flydende krystal styret af et lysmønster (skinnede i lyserødt område). Kredit:Prof. Zhang Rui, HKUST Liquid Crystals (LC) -
 En maskinlæringsløsning til at designe materialer med ønskede optiske egenskaberStyring af lys-stof-interaktioner er central for en række vigtige applikationer, såsom kvantepunkter, som kan bruges som lysgivere og sensorer. Kredit:PlasmaChem At forstå, hvordan stof interagere
En maskinlæringsløsning til at designe materialer med ønskede optiske egenskaberStyring af lys-stof-interaktioner er central for en række vigtige applikationer, såsom kvantepunkter, som kan bruges som lysgivere og sensorer. Kredit:PlasmaChem At forstå, hvordan stof interagere -
 Forskere udvikler billig chip til at detektere tilstedeværelse og mængde af COVID-19 antistofferAntistoftestplatformen, udviklet af forskere fra Micro/Bio/Nanofluidics Unit på OIST. Kredit:OIST Robust og udbredt antistoftest er fremstået som en nøglestrategi i kampen mod SARS-CoV-2, den viru
Forskere udvikler billig chip til at detektere tilstedeværelse og mængde af COVID-19 antistofferAntistoftestplatformen, udviklet af forskere fra Micro/Bio/Nanofluidics Unit på OIST. Kredit:OIST Robust og udbredt antistoftest er fremstået som en nøglestrategi i kampen mod SARS-CoV-2, den viru
- ØPA -chefen skal genoverveje at betale krav om mineudslip
- Group udvikler carbon nanorør baseret fleksibel skærm ved hjælp af flexografisk printteknologi
- Sådan fungerer et mikronet
- Google står over for EU's anti-trust-undersøgelse for jobsøgningsværktøj
- Kødædere ved, at det at spise andre kødædende kroppe overfører sygdomme
- Forskning i svævende oliedråber kan hjælpe med at reducere luftforurening


