Kemikere producerer nyt-til-natur enzym, der indeholder bor
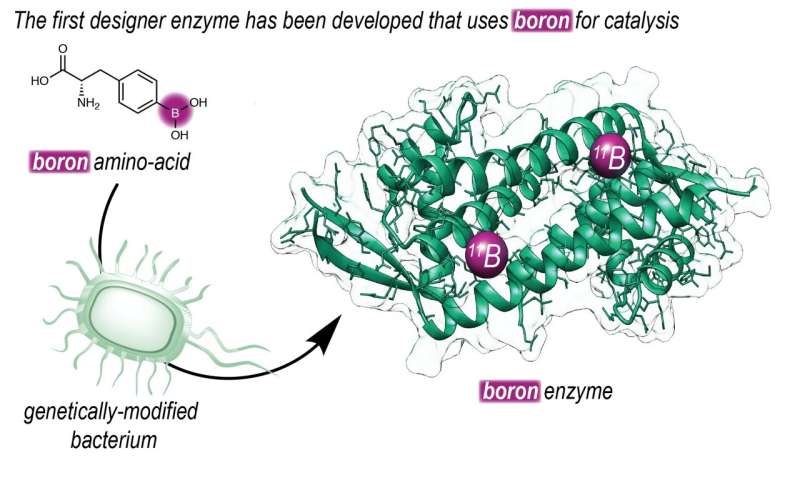
Boronsyre er blevet brugt i organisk kemi i årtier, selvom det ikke er til stede i nogen organisme. "Det giver anledning til andre kemiske reaktioner end dem, vi finder i naturen," forklarer Gerard Roelfes, professor i biomolekylær kemi og katalyse ved universitetet i Groningen.
Hans gruppe skabte et enzym med boronsyre i dets reaktive centrum og brugte derefter rettet evolution til at gøre det mere selektivt og forbedre dets katalytiske kraft. Ydermere er enzymatiske reaktioner mere bæredygtige end klassiske kemiske reaktioner, da de finder sted ved lave temperaturer og uden giftige opløsningsmidler. Undersøgelsen blev offentliggjort online i tidsskriftet Nature den 8. maj.
Anvendelsen af bor i organisk kemi går omkring halvfjerds år tilbage og blev tildelt en Nobelpris i kemi i 1979. I de senere år er interessen for bor som katalysator vokset, men endnu er dets anvendelse i den kemiske industri begrænset.
Roelfes forklarer, "Indtil videre er borkatalyse for langsom, og den er ikke særlig velegnet til enantioselektive reaktioner. Disse typer reaktioner bruges til at skabe chirale molekyler, som kan eksistere i to versioner, der er spejlbilleder af hinanden, som en venstre og en højre hånd.
"I mange lægemidler kan begge hænder have en forskellig effekt. Det er derfor vigtigt at selektivt producere den rigtige hånd, især for medicinalindustrien."
Udvidet genetisk kode
"For at gøre dette muligt satte vi os for at introducere bor i et enzym. Vores gruppe har en lang historie med at designe enzymer, der ikke findes i naturen," siger Roelfes. Roelfes-gruppen brugte en udvidet genetisk kode til at introducere en ikke-naturlig aminosyre, der indeholder en reaktiv boronsyregruppe i et enzym. "Ved brug af denne teknik kan vi på DNA-niveau bestemme, hvor vi placerer aminosyren i et protein."
Når de først lavede et enzym med boronsyre i dets reaktive center, kunne de bruge rettet evolution til at øge dets effektivitet, hvilket resulterede i hurtigere katalyse. Roelfes tilføjer:"Desuden var vi i stand til at opnå en meget enantioselektiv katalyse ved at placere boronsyren i den chirale kontekst af et enzym. Den reaktion, der er beskrevet, er et principbevis og viser vejen til at udnytte borens katalytiske kraft i enzymer."
Biokatalyse
At bruge enzymer til at skabe organiske forbindelser er vigtigt for den farmaceutiske industri. "I deres indsats mod grønnere og mere bæredygtige måder at producere lægemidler på, kigger de på biokatalyse for at erstatte konventionelle kemiske reaktioner," siger Roelfes.
På universitetet i Groningen gøres der en fælles indsats for at nå dette mål. Roelfes konkluderer:"Vi har en række forskergrupper på Det Naturvidenskabelige og Tekniske Fakultet, der er engageret i denne form for arbejde og bruger forskellige tilgange til at skabe biokatalytiske løsninger til den kemiske industri."
I denne sammenhæng vil Roelfes og hans team fortsætte med at udvikle deres boronsyreenzymer og skabe andre sådanne nye enzymer i naturen.
Flere oplysninger: Gerard Roelfes, Boron-katalyse i et designerenzym, Nature (2024). DOI:10.1038/s41586-024-07391-3. www.nature.com/articles/s41586-024-07391-3
Journaloplysninger: Natur
Leveret af University of Groningen
 Varme artikler
Varme artikler
-
 En ny måde at direkte omdanne metan til methanol ved hjælp af guld-palladium nanopartiklerRepræsentative HAADF-billeder og partikelstørrelsesfordelinger for den ikke-understøttede AuPd-PVP-sol i frisk (A til C) og efter en CH4-oxidationsreaktion (D til F). Kredit:Graham J. Hutchings og Chr
En ny måde at direkte omdanne metan til methanol ved hjælp af guld-palladium nanopartiklerRepræsentative HAADF-billeder og partikelstørrelsesfordelinger for den ikke-understøttede AuPd-PVP-sol i frisk (A til C) og efter en CH4-oxidationsreaktion (D til F). Kredit:Graham J. Hutchings og Chr -
 Ny algoritme forudsiger optimale materialer blandt alle mulige forbindelserResultaterne af en Mendelevian-søgning efter hårde og superhårde materialer Kredit:Zahed Allahyari og Artem R. Oganov / NPJ Computational Materials Skoltech-forskere har tilbudt en løsning på prob
Ny algoritme forudsiger optimale materialer blandt alle mulige forbindelserResultaterne af en Mendelevian-søgning efter hårde og superhårde materialer Kredit:Zahed Allahyari og Artem R. Oganov / NPJ Computational Materials Skoltech-forskere har tilbudt en løsning på prob -
 Forskere designer måde at bruge harmløse bakterier til at opdage tungmetaller i drikkevand(L-R) Gregoire Thouvenin og Nicholas Csicsery i UCSD Biodynamics Lab drevet af bioingeniør- og biologiprofessor Jeff Hasty ved UC San Diego. Kredit:University of California - San Diego Når det ko
Forskere designer måde at bruge harmløse bakterier til at opdage tungmetaller i drikkevand(L-R) Gregoire Thouvenin og Nicholas Csicsery i UCSD Biodynamics Lab drevet af bioingeniør- og biologiprofessor Jeff Hasty ved UC San Diego. Kredit:University of California - San Diego Når det ko -
 Mod en miljøvenlig produktion af aktive farmaceutiske ingredienser med en flowreaktorProf. Dr. Harald Gröger arbejder i ONE-FLOW på en måde at producere kemiske forbindelser gennem kombination af bio- og kemokatalyse i flowreaktorer. De kemiske reaktioner udføres f.eks. I moduler med
Mod en miljøvenlig produktion af aktive farmaceutiske ingredienser med en flowreaktorProf. Dr. Harald Gröger arbejder i ONE-FLOW på en måde at producere kemiske forbindelser gennem kombination af bio- og kemokatalyse i flowreaktorer. De kemiske reaktioner udføres f.eks. I moduler med
- Dybfalsk lyd har en fortælling:Forskere bruger flydende dynamik til at spotte kunstige bedragerstem…
- Forskere designer en løsning til trafikstyring, der hjælper med at reducere kø og forurening i by…
- Tropiske tørre skovplanter
- Grad 2 Matematikprojekter
- briter, Tjekkerne hævder verdens mest kraftfulde superlaser
- At ignorere klimaændringer vil føre til hidtil uset, samfundsforstyrrende varmeekstremiteter i Mel…


