Stærkere end naturen:Optimerede radikaler som potentielle nye katalysatorer
Naturen bruger enzymer til forskellige metaboliske processer. Disse biologiske katalysatorer er ekstremt effektive. Biomimetiske katalysatorer baseret på billige udgangsmaterialer fra laboratoriet, der kan reproducere effektiviteten af de naturlige enzymer og kan fungere under omgivende forhold, er derfor af stor interesse for forskning og industri.
I et projekt ledet af Institut for Kemi ved Humboldt-Universität zu Berlin (HU) har forskere undersøgt en særlig gruppe biologiske katalysatorer kendt som oxidaser. Disse enzymer katalyserer forskellige oxidationsreaktioner, hvor elektroner frigives fra et stof og absorberes af et andet. Små, meget reaktive partikler, såkaldte radikaler, spiller ofte en vigtig rolle i disse processer.
Oxidationskapacitet forbedret ved binding til jern
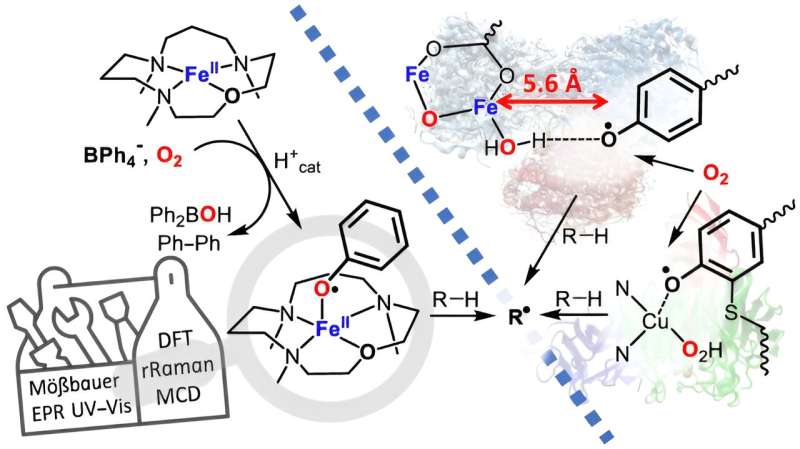
Enzymet af aktuelle interesse er galactoseoxidase, der findes i mange typer svampe, hvor et phenoxylradikal anvendes som oxidationsmiddel. Holdet ledet af HU-forsker Kallol Ray har nu fundet en måde at udnytte phenoxyl-radikalet i laboratoriet på en sådan måde, at oxidationskapaciteten kan øges markant.
I det naturligt forekommende enzym stabiliseres phenoxyl-radikalet af et svovlatom, hvilket begrænser dets oxidationsevne. Forskerne har nu forbedret oxidationsevnen ved at binde en umodificeret phenoxyl-radikal til jern og har kemisk karakteriseret denne jern-phenoxyl-radikal for første gang. Rays team samarbejdede med kolleger fra Technical University of Berlin og University of Michigan, U.S., om dette projekt.
Værket er publiceret i tidsskriftet Nature Chemistry .
Første beskrivelse af jernphenoxyl-radikalen – vigtig for forskning og industri
"Vi forventer, at vores arbejde vil være udgangspunktet for en mere målrettet indsats for at udnytte jern-phenoxyl-radikalinteraktionen til forskellige biokemiske reaktioner," siger Ray. "Dette kan understøtte udviklingen af nye katalysatorer, der er nødvendige for alternative energiteknologier og andre bioteknologiske anvendelser."
Rays og hans teams forskningsresultater er af stor betydning for både forskning og anvendelse, da reaktionen katalyseret af galactoseoxidase (oxidation af en primær alkohol til det tilsvarende aldehyd) er en af de vigtigste og mest udbredte kemiske reaktioner i organiske syntese.
Resultaterne kunne også bruges i industrien til at omdanne den klimaskadelige gas metan til flydende methanol. I modsætning til metan, som er en flygtig gas og derfor svær at håndtere, er methanol let at transportere og kan bruges som syntetisk brændstof. I øjeblikket kræves der en del energi for at omdanne metan til methanol. Den kemiske reaktion finder kun sted ved høje temperaturer (> 500 grader Celsius) og under højt tryk. Biomimetiske katalysatorer kunne reducere denne energitilførsel betydeligt.
"I dette projekt var det spændende at se den uventede strukturelle og funktionelle lighed mellem vores syntetiske system og naturlige enzymer," siger Dustin Kass, ph.d. studerende i Kallol Rays forskningsgruppe og hovedforfatter af denne undersøgelse.
Flere oplysninger: Dustin Kass et al., Indfangning af et phenoxyl-radikal ved et ikke-hæm high-spin jern(II) center, Nature Chemistry (2024). DOI:10.1038/s41557-023-01405-9
Leveret af Humboldt University of Berlin
 Varme artikler
Varme artikler
-
 Citrusderivat gør gennemsigtigt træ 100 procent vedvarendeEt stykke af det gennemsigtige træ vises. Kredit:Céline Montanari Siden det blev introduceret første gang i 2016, gennemsigtigt træ er udviklet af forskere ved KTH Royal Institute of Technology so
Citrusderivat gør gennemsigtigt træ 100 procent vedvarendeEt stykke af det gennemsigtige træ vises. Kredit:Céline Montanari Siden det blev introduceret første gang i 2016, gennemsigtigt træ er udviklet af forskere ved KTH Royal Institute of Technology so -
 Det er en fælde - Forskere identificerer processen, hvorved huller bliver fanget i ZnO nanopartikle…Argonne-forskere hjalp med at identificere den proces, hvorved huller bliver fanget i nanopartikler lavet af zinkoxid, et materiale af potentiel interesse til solenergianvendelser, fordi det absorbere
Det er en fælde - Forskere identificerer processen, hvorved huller bliver fanget i ZnO nanopartikle…Argonne-forskere hjalp med at identificere den proces, hvorved huller bliver fanget i nanopartikler lavet af zinkoxid, et materiale af potentiel interesse til solenergianvendelser, fordi det absorbere -
 Ny katalysator til brintproduktion er et skridt mod rent brændstofForsiden viser produktionen af brintgas, når elektroner og protoner mødes på ruthenium-ion-komplekserede grafitiske carbonnitrid-nanoark understøttet på grafenoverfladen. Billedet er baseret på en g
Ny katalysator til brintproduktion er et skridt mod rent brændstofForsiden viser produktionen af brintgas, når elektroner og protoner mødes på ruthenium-ion-komplekserede grafitiske carbonnitrid-nanoark understøttet på grafenoverfladen. Billedet er baseret på en g -
 Kunstig cyanobakteriel biofilm kan opretholde produktionen af grøn ethylen i over en månedEt billede af cyanobakterier, Tolypothrix. Kredit:Wikipedia / CC BY-SA 3.0 Vor tids store globale udfordringer, herunder klimaforandringer, energisikkerhed og knaphed på naturressourcer, fremme en
Kunstig cyanobakteriel biofilm kan opretholde produktionen af grøn ethylen i over en månedEt billede af cyanobakterier, Tolypothrix. Kredit:Wikipedia / CC BY-SA 3.0 Vor tids store globale udfordringer, herunder klimaforandringer, energisikkerhed og knaphed på naturressourcer, fremme en
- Direkte nedslag eller atomvåben? Sådan redder du Jorden fra en asteroide
- Binær stjerne sammensat af to brune dværge opdaget ved mikrolinsing
- Undersøgelse finder, at virtual reality -træning kan forbedre medarbejdernes sikkerhed
- Lava fra vulkanen Kilauea kommer ind i havet, skaber giftig sky
- Dybhavskoraller afslører, hvorfor atmosfærisk kulstof blev reduceret i koldere perioder
- Muliggør hurtig screening af poly(2-oxazolin)-baseret nanomedicin gennem divergerende syntese


