Ny højhastighedstest viser, hvordan antibiotika kombineres for at dræbe bakterier
På disse ultrahurtige tidsskalaer observerede holdet, at stofferne skabte mikroskopiske porer i bakteriens beskyttende ydre lag, hvilket fik indholdet til at lække ud og cellen til at dø.
Eksperimenterne er nogle af de første af deres slags, og resultaterne kan bane vejen for at designe mere effektive antibiotika, der målretter mod bakteriemembranen mere specifikt.
Forskningen er publiceret i tidsskriftet ACS Central Science.
Hvordan virker antibiotika?
En måde, hvorpå antibiotika dræber bakterier, er ved at målrette og beskadige integriteten af den bakterielle ydre membran, der består af et fosfolipid-dobbeltlag.
Det er to lag af fedtmolekyler (phospholipider), der danner en barriere omkring alle bakterieceller. Dobbeltlaget er en dynamisk og kompleks struktur, der har unikke fysiske egenskaber, såsom dets flydendehed, der afhænger af typen og antallet af lipider i membranen.
Membranafbrydelse er en førende årsag til bakteriel død, men hvordan det præcist sker, er ikke blevet fuldt ud forstået, hovedsagelig fordi disse hændelser sker på usædvanligt korte tidsskalaer.
Den nuværende undersøgelse adresserer dette vidensgab ved at kombinere eksperimenter med beregningssimuleringer for at undersøge de indledende processer involveret i membranskader.
At fange det usete
Et hold ledet af forskere fra Oxford University og University of California, San Diego, brugte high-speed atomic force microscopy (HS-AFM) til at se et membranforstyrrende antibiotikum interagere med en bakteriel membran i næsten realtid.
Højhastighedsinstrumentet registrerer interaktionerne mellem en oscillerende nanoskalaspids og et blødt materiale med en hastighed på næsten 770.000 billeder i sekundet, hvilket afslører detaljer, der ikke kan ses ved hjælp af konventionelle billeddannelsesmetoder.
Holdet brugte instrumentets unikke egenskaber til at fange de begivenheder, der sker i mikrosekunder til millisekunders tidsskalaer, efter at et antibiotikum kommer i kontakt med bakteriemembranen, hvilket giver dem mulighed for at observere selve begyndelsen af celledødsprocessen.
Professor Aleksander Bublitz fra Oxfords Institut for Kemi sagde:'Det er utroligt svært at afbilde hurtige processer i så små længdeskalaer, men ved at kombinere dette værktøj med beregningssimuleringer kan vi begynde at forstå, hvordan antibiotika får membraner til at nedbrydes. Vi kan så bruge den information til at designe bedre lægemidler, der specifikt retter sig mod bakteriemembranerne og forstyrrer dem mere effektivt.'
Ny indsigt
Forskningen afslører for første gang den afgørende rolle, som den bakterielle membranfluiditet og den antibiotiske molekylebindingsdynamik spiller i den poredannende proces.
Ved at efterligne systemet med computersimuleringer var forskerne i stand til at se, hvordan antibiotikaen virker på atomniveau.
Simuleringerne gjorde det muligt for dem at identificere bestemte membranlipider og specifikke antibiotika-membran-interaktioner, der er kritiske for poredannelsesprocessen.
Denne information kan bruges til at udvikle mere effektive lægemidler ved at udvikle specifikke molekyler, der målretter mod de identificerede lipider eller antibiotikabindingssteder.
 Varme artikler
Varme artikler
-
 Sporing af atombevægelse i realtid mellem krystalkorn i metallerTing Zhu, professor i maskinteknik ved Georgia Tech, foran sine TEM-billeder af polykrystallinske metaller og en grafisk simulerende atomstruktur. Kredit:Georgia Tech Metalliske materialer, der bru
Sporing af atombevægelse i realtid mellem krystalkorn i metallerTing Zhu, professor i maskinteknik ved Georgia Tech, foran sine TEM-billeder af polykrystallinske metaller og en grafisk simulerende atomstruktur. Kredit:Georgia Tech Metalliske materialer, der bru -
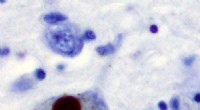 Ubrugeligt Parkinsons-molekyle spilder sine hemmelighederImmunhistokemi for alfa-synuclein, der viser positiv farvning (brun) af et intraneuralt Lewy-legeme i Substantia nigra ved Parkinsons sygdom. Kredit:Wikipedia Forskere fra UC San Francisco har for
Ubrugeligt Parkinsons-molekyle spilder sine hemmelighederImmunhistokemi for alfa-synuclein, der viser positiv farvning (brun) af et intraneuralt Lewy-legeme i Substantia nigra ved Parkinsons sygdom. Kredit:Wikipedia Forskere fra UC San Francisco har for -
 Ultrahurtige metalionbatterier baseret på nyt organisk katodemateriale er blevet udvikletKredit:CC0 Public Domain Forskere fra Skoltech Center for Energy Science and Technology, IPCP RAS og D.I. Mendeleev University of Chemical Technology har designet et nyt polymerkatodemateriale til
Ultrahurtige metalionbatterier baseret på nyt organisk katodemateriale er blevet udvikletKredit:CC0 Public Domain Forskere fra Skoltech Center for Energy Science and Technology, IPCP RAS og D.I. Mendeleev University of Chemical Technology har designet et nyt polymerkatodemateriale til -
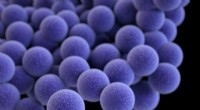 Forskere opdager gener, der hjælper skadelige bakterier til at modarbejde behandlingMethicillinresistent Staphylococcus aureus (MRSA). Kredit:Amerikanske centre for sygdomsbekæmpelse og forebyggelse Et Rutgers-ledet team har opdaget to gener, der gør nogle stammer af skadelige
Forskere opdager gener, der hjælper skadelige bakterier til at modarbejde behandlingMethicillinresistent Staphylococcus aureus (MRSA). Kredit:Amerikanske centre for sygdomsbekæmpelse og forebyggelse Et Rutgers-ledet team har opdaget to gener, der gør nogle stammer af skadelige
- Toyota hybrider kører over 60 % af tiden i nul-emissionstilstand, undersøgelse finder
- Nyt kompleks, der reagerer med nitril - en nøgle til at muliggøre nedregulering af kræftenzymer
- Nanozymterapi forhindrer opbygning af skadelig tandplak
- Sådan konverteres trefaset strøm til Amps
- Ingeniører skaber den mest slidstærke metallegering i verden
- Grafen kvanteprikker kan føre til billige solceller og OLED'er


