Hvilken effekt har temperaturen på reaktionshastigheden?
1. Øget temperatur:
- Højere temperaturer fører generelt til hurtigere reaktionshastigheder.
- Når temperaturen stiger, stiger den gennemsnitlige kinetiske energi af reaktantmolekylerne også.
- Denne øgede energi gør det muligt for molekyler at bevæge sig hurtigere, kollidere hyppigere og have en større chance for at nå den aktiveringsenergi, der kræves for, at reaktionen kan finde sted.
- Med flere molekyler, der besidder den nødvendige energi, forløber reaktionen i et hurtigere tempo.
2. Nedsat temperatur:
- Lavere temperaturer resulterer i langsommere reaktionshastigheder.
- Når temperaturen falder, falder den kinetiske energi af reaktantmolekylerne også.
- Molekyler bevæger sig langsommere, støder sjældnere sammen og har en lavere sandsynlighed for at overvinde aktiveringsenergibarrieren.
- Som følge heraf aftager reaktionshastigheden.
3. Aktiveringsenergi:
- Temperaturen påvirker direkte den aktiveringsenergi, der kræves til en kemisk reaktion.
- Aktiveringsenergi er den mindste mængde energi, reaktanter skal have for at omdanne til produkter.
- Højere temperaturer reducerer den effektive aktiveringsenergi, hvilket gør det lettere for molekyler at nå dette energiniveau og gennemgå reaktionen.
- Lavere temperaturer øger derimod den effektive aktiveringsenergi, hvilket gør reaktionen mindre sandsynlig.
4. Kollisionsfrekvens:
- Temperatur påvirker hyppigheden af kollisioner mellem reaktantmolekyler.
- Ved højere temperaturer får den øgede kinetiske energi molekyler til at bevæge sig hurtigere og kollidere hyppigere.
- Denne højere kollisionsfrekvens øger chancerne for, at molekyler støder på hinanden i den korrekte orientering, for at en reaktion kan finde sted.
- Omvendt reducerer lavere temperaturer kollisionsfrekvensen, hvilket mindsker sandsynligheden for vellykkede kollisioner.
5. Reaktionshastighedskonstant:
- Reaktionshastighedskonstanten (k) er et kvantitativt mål for reaktionshastigheden.
- Det repræsenterer hastigheden af ændring i koncentrationen af reaktanter eller produkter over tid.
- Temperaturen påvirker direkte værdien af reaktionshastighedskonstanten.
- Når temperaturen stiger, stiger reaktionshastighedskonstanten generelt, hvilket indikerer en hurtigere reaktion.
- På samme måde fører et fald i temperaturen til et fald i reaktionshastighedskonstanten, hvilket indikerer en langsommere reaktion.
Det er vigtigt at bemærke, at temperaturens effekt på reaktionshastigheden kan variere afhængigt af den specifikke kemiske reaktion og arten af de involverede reaktanter. Nogle reaktioner kan udvise mere følsomhed over for temperaturændringer end andre.
Sidste artikelHvordan dannes en kovalent binding mellem to atomer?
Næste artikelHvad er PH-værdien af KHCO3?
 Varme artikler
Varme artikler
-
 Fluorescerende sonde kunne lyse op kræftVed at belyse enzymet beta-galactosidase i en cellekultur, Michigan Tech kemikere håber at gøre det lettere at efterlade mere sundt væv i kræftkirurgi. En fluorescerende sonde udviklet af Michigan
Fluorescerende sonde kunne lyse op kræftVed at belyse enzymet beta-galactosidase i en cellekultur, Michigan Tech kemikere håber at gøre det lettere at efterlade mere sundt væv i kræftkirurgi. En fluorescerende sonde udviklet af Michigan -
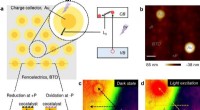 Forskere foreslår ny ladningsadskillelsesstrategi i ferroelektriske fotokatalysatorerLadningsadskillelse ved meta/ferroelektrisk grænseflade. et skematisk diagram af foreslået metal/ferroelektrisk fotokatalysator. b AFM-topografi af Au-partikler på en BaTiO3 enkelt krystal. Målestok,
Forskere foreslår ny ladningsadskillelsesstrategi i ferroelektriske fotokatalysatorerLadningsadskillelse ved meta/ferroelektrisk grænseflade. et skematisk diagram af foreslået metal/ferroelektrisk fotokatalysator. b AFM-topografi af Au-partikler på en BaTiO3 enkelt krystal. Målestok, -
 3-D-print af grønnere bygninger ved hjælp af lokal jordForskere har udviklet en metode til at 3D-printe strukturer ved hjælp af lokal jord. Kredit:Aayushi Bajpayee Byggebranchen står i øjeblikket over for to store udfordringer:efterspørgslen efter bær
3-D-print af grønnere bygninger ved hjælp af lokal jordForskere har udviklet en metode til at 3D-printe strukturer ved hjælp af lokal jord. Kredit:Aayushi Bajpayee Byggebranchen står i øjeblikket over for to store udfordringer:efterspørgslen efter bær -
 Batteriforskning:nye gennembrud inden for forskning i superbatterierDannelsen af singlet oxygen (1O2) forringer cyklusstabiliteten af mange alkalimetalkatoder, såsom Li-O2 katoden. I tidsskriftet præsenterer Angewandte Chemie Freunberger en effektiv og højspænding
Batteriforskning:nye gennembrud inden for forskning i superbatterierDannelsen af singlet oxygen (1O2) forringer cyklusstabiliteten af mange alkalimetalkatoder, såsom Li-O2 katoden. I tidsskriftet præsenterer Angewandte Chemie Freunberger en effektiv og højspænding
- Vil du annullere planer med en ven? Forskning siger, man ikke lyver
- Chesapeake Bay:Større end gennemsnittet sommer død zone prognose for 2018 efter vådt forår
- Molekylær nano-spioner gør det let at opdage sygdom
- Markerede en betydelig kølig besværgelse Megafaunas død?
- Et hurtigt kig på Nobelpriserne i 2022
- De unikke forhold for mennesker, der bor i deres køretøjer


