Der er 2 gram H2 gas i en beholder med fast volumen ved 273 C. 16 Han tilsættes til og temperaturen hæves 819 Så hvilket forhold sluttryk starttryk?
PV =nRT
hvor P er trykket, V er volumenet, n er antallet af mol gas, R er den ideelle gaskonstant, og T er temperaturen.
Hvis lydstyrken er fast, kan vi skrive:
P =nRT/V
Lad os beregne starttrykket ved hjælp af H2-gas:
n(H2) =2 g / 2 g/mol =1 mol
P1 =n(H2)RT1/V
P1 =(1 mol)(0,08206 L*atm/mol*K)(273 K)/V
P1 =22,4 atm
Lad os nu beregne det endelige tryk ved hjælp af H2 og He-gasser:
n(total) =n(H2) + n(He) =1 mol + 2 mol =3 mol
P2 =n(total)RT2/V
P2 =(3 mol)(0,08206 L*atm/mol*K)(1092 K)/V
P2 =86 atm
Derfor er forholdet mellem sluttryk og starttryk:
P2/P1 =86 atm/22,4 atm =3,8
Så trykket steg 3,8 gange.
 Varme artikler
Varme artikler
-
 Ny tilgang letter spektroskopi på individuelle molekylerProfessor Dr. Juergen Hauer (tv) og førsteforfatter Erling Thyrhaug med deres måleinstrument. I baggrunden, spektre taget med. Kredit:Andreas Battenberg Mens spektroskopiske målinger normalt bereg
Ny tilgang letter spektroskopi på individuelle molekylerProfessor Dr. Juergen Hauer (tv) og førsteforfatter Erling Thyrhaug med deres måleinstrument. I baggrunden, spektre taget med. Kredit:Andreas Battenberg Mens spektroskopiske målinger normalt bereg -
 Innovativ kombination af hårde og bløde materialer forbedrer vedhæftningen til ru overfladerVedhæftning til ru overflader forbedres væsentligt ved kombinationen af to materialer. Den store model viser det grundlæggende princip og strukturen af de nye klæbemidler, hvor bløde materialer (g
Innovativ kombination af hårde og bløde materialer forbedrer vedhæftningen til ru overfladerVedhæftning til ru overflader forbedres væsentligt ved kombinationen af to materialer. Den store model viser det grundlæggende princip og strukturen af de nye klæbemidler, hvor bløde materialer (g -
 Team opdager dobbelt helixstruktur i syntetisk makromolekyleLou Madsen (tv.) er lektor i Kemisk Institut og har ledet et internationalt tværfagligt samarbejde om opdagelsen af den dobbelte helixstruktur af en polymer kaldet PBDT. Ying Wang (th.) er en tidlig
Team opdager dobbelt helixstruktur i syntetisk makromolekyleLou Madsen (tv.) er lektor i Kemisk Institut og har ledet et internationalt tværfagligt samarbejde om opdagelsen af den dobbelte helixstruktur af en polymer kaldet PBDT. Ying Wang (th.) er en tidlig -
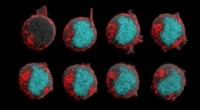 Forskere viser, at en kræftforsvarsmekanisme kan vendes tilbage for at angribe tumorerI disse time-lapse billeder, kimære antigenreceptorer reagerer på et opløseligt cytokin, udløser T-celleaktivering. Kredit:ZeNan Chang og Michael Lorenzini UCLA ingeniører og videnskabsmænd har ko
Forskere viser, at en kræftforsvarsmekanisme kan vendes tilbage for at angribe tumorerI disse time-lapse billeder, kimære antigenreceptorer reagerer på et opløseligt cytokin, udløser T-celleaktivering. Kredit:ZeNan Chang og Michael Lorenzini UCLA ingeniører og videnskabsmænd har ko
- Cigaretter tegner sig for halvdelen af det affald, der genvindes på kystlinierne i Vancouver og V…
- Kuratorer og huler:Hvordan et tip fra borgerforsker førte til dybe opdagelser i Utahs huler
- Bimetallisk legering nanokatalysator øger effektiv ammoniakproduktion med potentiale for kulstoffri…
- Ny analyse afslører, hvor marine hedebølger vil intensivere hurtigst
- Dens levested er decimeret, denne karismatiske Minnesota-fugl danser på kanten af glemsel
- Kontroversiel flydende strand afsløret ud for den franske riviera


