Beregn den nødvendige mængde oxalsyredihydrat til fremstilling af 200 ml 0,50 M syreopløsning?
Oxalsyredihydrat har den kemiske formel H2C2O4·2H2O. Dens molære masse beregnes ved at lægge molmasserne af alle dets atomer sammen:
$$2\gange 12,01 \text{ g/mol C} + 2\gange 1,01 \text{ g/mol H} + 4\gange 16,00 \text{ g/mol O} + 2\gange 18,02 \text{ g/ mol H2O}$$
Den molære masse af oxalsyredihydrat er 126,07 g/mol.
Trin 2:Beregn antallet af nødvendige mol oxalsyredihydrat
Vi kan bruge følgende formel til at beregne antallet af mol opløst stof, der er nødvendigt for at fremstille en opløsning af en given koncentration:
Molaritet (M) =mol opløst stof / volumen af opløsning (L)
Ved at omarrangere formlen får vi:
Mol opløst stof =Molaritet (M) × Opløsningsvolumen (L)
I dette tilfælde er den ønskede molaritet af oxalsyredihydratopløsningen 0,50 M, og volumenet af opløsning, vi ønsker at fremstille, er 200 ml, hvilket svarer til 0,2 L.
Nødvendigt antal mol oxalsyredihydrat =0,50 M × 0,2 L =0,1 mol
Trin 3:Beregn den nødvendige masse af oxalsyredihydrat
Nu hvor vi kender antallet af nødvendige mol oxalsyredihydrat, kan vi beregne den tilsvarende masse ved hjælp af dens molære masse:
Masse oxalsyredihydrat nødvendig =mol oxalsyredihydrat × molær masse oxalsyredihydrat
Vi erstatter de værdier, vi har:
Nødvendig masse af oxalsyredihydrat =0,1 mol × 126,07 g/mol =12,61 g
For at fremstille 200 ml 0,50 M oxalsyreopløsning skal vi derfor bruge 12,61 gram oxalsyredihydrat.
 Varme artikler
Varme artikler
-
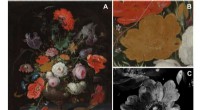 Kemisk og optisk billeddannelse forklarer, hvorfor en rose mistede sin farve i et berømt maleriPigmentnedbrydning i den gule rose i Abraham Mignons Stilleben med blomster og et ur. (A) Visuelt fotografi af stilleben med blomster og et ur af Abraham Mignon (1640-1679), olie på lærred, dateret ca
Kemisk og optisk billeddannelse forklarer, hvorfor en rose mistede sin farve i et berømt maleriPigmentnedbrydning i den gule rose i Abraham Mignons Stilleben med blomster og et ur. (A) Visuelt fotografi af stilleben med blomster og et ur af Abraham Mignon (1640-1679), olie på lærred, dateret ca -
 Undersøgelse kan hjælpe med at booste peptiddesignKredit:CC0 Public Domain Peptider, som er korte rækker af aminosyrer, spiller en afgørende rolle i sundhed og industri med en lang række medicinske anvendelser, herunder i antibiotika, anti-inflam
Undersøgelse kan hjælpe med at booste peptiddesignKredit:CC0 Public Domain Peptider, som er korte rækker af aminosyrer, spiller en afgørende rolle i sundhed og industri med en lang række medicinske anvendelser, herunder i antibiotika, anti-inflam -
 At gøre katalytiske overflader mere aktive for at hjælpe med at dekarbonisere brændstoffer og kem…Kredit:Massachusetts Institute of Technology Elektrokemiske reaktioner, der accelereres ved hjælp af katalysatorer, er kernen i mange processer til fremstilling og brug af brændstoffer, kemikalier
At gøre katalytiske overflader mere aktive for at hjælpe med at dekarbonisere brændstoffer og kem…Kredit:Massachusetts Institute of Technology Elektrokemiske reaktioner, der accelereres ved hjælp af katalysatorer, er kernen i mange processer til fremstilling og brug af brændstoffer, kemikalier -
 Ny tilgang kan føre til designet plast med specifikke egenskaberKredit:CC0 Public Domain Forestil dig en plastikpose, der kan bære dine dagligvarer hjem, nedbrydes derefter hurtigt, uden at skade miljøet. Eller en superstærk, letvægtsplastik til fly, raketter,
Ny tilgang kan føre til designet plast med specifikke egenskaberKredit:CC0 Public Domain Forestil dig en plastikpose, der kan bære dine dagligvarer hjem, nedbrydes derefter hurtigt, uden at skade miljøet. Eller en superstærk, letvægtsplastik til fly, raketter,
- Miljøvolds frontlinje
- COVID øgede Latinas ansvar derhjemme, mens de begrænsede deres evne til at arbejde:Rapporter
- Opladet ilt i ionosfæren kan tilbyde biomarkør for eksoplaneter
- Om Motion & Force for Kids
- Atmosfæriske beacons guider NASA-forskere i deres søgen efter liv
- Mars beboelighed begrænset af dens lille størrelse, isotopundersøgelse tyder på


