Hvor mange individuelle oxygenatomer er indeholdt i et mol Li2C2O4?
1. Start med den kemiske formel for lithiumoxalat:Li2C2O4.
2. Beregn molmassen af Li2C2O4 ved at tilføje atommasserne af dets bestanddele.
- Li:2 x 6,941 g/mol =13,882 g/mol
- C:2 x 12,011 g/mol =24,022 g/mol
- O:4 x 15,999 g/mol =63,996 g/mol
Total molær masse af Li2C2O4 =13,882 g/mol + 24,022 g/mol + 63,996 g/mol =101,900 g/mol.
3. Avogadros tal er cirka 6.022 x 10^23, hvilket repræsenterer antallet af partikler (atomer, molekyler eller ioner), der er til stede i et mol af et stof.
4. For at bestemme antallet af individuelle oxygenatomer i et mol Li2C2O4 skal du gange Avogadros tal med antallet af oxygenatomer i formlen.
Der er fire oxygenatomer i et molekyle Li2C2O4. Derfor er der i et mol Li2C2O4:
4 oxygenatomer/molekyle * 6,022 x 10^23 molekyler/mol =2,4088 x 10^24 oxygenatomer.
Som konklusion indeholder et mol Li2C2O4 2,4088 x 10^24 individuelle oxygenatomer.
Sidste artikelHvad står CH4 for i det periodiske system?
Næste artikelHvorfor er mgcl2 bedre koagulerende end kcl for As2S3?
 Varme artikler
Varme artikler
-
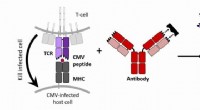 Udstyrelse af T -celleceptorer til bekæmpelse af en udbredt og undertiden dødelig virusT-celler er dygtige til at dræbe cytomegalovirus (CMV)-inficerede celler i kraft af en T-cellereceptor (TCR), der genkender intracellulære CMV-associerede proteiner, der bliver præsenteret på celleove
Udstyrelse af T -celleceptorer til bekæmpelse af en udbredt og undertiden dødelig virusT-celler er dygtige til at dræbe cytomegalovirus (CMV)-inficerede celler i kraft af en T-cellereceptor (TCR), der genkender intracellulære CMV-associerede proteiner, der bliver præsenteret på celleove -
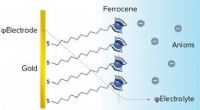 Kombineret tilgang til sondering af grænsefladeelektrokemi mere detaljeretFigur 1:Skematisk af et elektrokemisk aktivt ferrocen-termineret selvsamlet monolag på guld, som blev brugt som en model elektrokemisk grænseflade. Det elektrokemiske miljø illustreres af den potentie
Kombineret tilgang til sondering af grænsefladeelektrokemi mere detaljeretFigur 1:Skematisk af et elektrokemisk aktivt ferrocen-termineret selvsamlet monolag på guld, som blev brugt som en model elektrokemisk grænseflade. Det elektrokemiske miljø illustreres af den potentie -
 En visuel database over humane plasmaforbindelserDatabasen er i stand til at kortlægge sammenhængen mellem de forskellige metabolitter, at tilbyde besøgende yderligere forskningsmuligheder. Kredit:Tohoku Medical Megabank Organization Forskere i
En visuel database over humane plasmaforbindelserDatabasen er i stand til at kortlægge sammenhængen mellem de forskellige metabolitter, at tilbyde besøgende yderligere forskningsmuligheder. Kredit:Tohoku Medical Megabank Organization Forskere i -
 Silke kunne forbedre følsomheden, fleksibilitet af bærbare kropssensorerSilke kan snart bruges til at producere mere følsomme og fleksible kropssensorer som denne. Kredit:Yingying Zhang Fra smarte sokker til træningstøj, der måler anstrengelse, Bærbare kropssensorer e
Silke kunne forbedre følsomheden, fleksibilitet af bærbare kropssensorerSilke kan snart bruges til at producere mere følsomme og fleksible kropssensorer som denne. Kredit:Yingying Zhang Fra smarte sokker til træningstøj, der måler anstrengelse, Bærbare kropssensorer e
- Model viser, hvordan plankton overlever i en turbulent verden
- Sådan konverteres flydende propan til Gas
- Chiral Faraday effekt gennembrud, takket være spiraler lavet af nikkel
- Hvordan det er at være en flagermus
- Kombineret datatilgang kan fremskynde udviklingen af nye materialer
- NASA måler nedbør fra rester af Tropical Cyclone Owens ved Queensland -kysten


