Hvad ville det overordnede potentiale for 3Ag2S 2Al(s) -- Al2S3 6Ag(s)?
- Ag2S + 2 e- -> 2 Ag(s) + S2- (E° =-0,79 V)
- Al3+ + 3 e- -> Al(s) (E° =-1,66 V)
- Al2S3 + 6 e- -> 2 Al(s) + 3 S2- (E° =-1,04 V)
Den overordnede reaktion er:
3Ag2S + 2Al(s) -> Al2S3 + 6Ag(s)
Det samlede potentiale for reaktionen er summen af standardreduktionspotentialerne for halvreaktionerne:
E° =E°(katode) - E°(anode)
E° =0,79 V - (-1,66 V) =2,45 V
Derfor er det samlede potentiale for reaktionen 2,45 V, hvilket indikerer, at reaktionen er spontan og vil fortsætte i retning af dannelse af Al2S3 og Ag.
Sidste artikelHvorfor opløsningsmedie 900ml?
Næste artikelEr mineralolie opløselig i en opløsning af vand og tetrahydrofuran?
 Varme artikler
Varme artikler
-
 Hybride indium-lithium anoder giver hurtig grænsefladeiontransportNye lithiumelektroder belagt med indium kunne være grundlaget for mere kraftfulde, længerevarende, genopladelige batterier. Belægningen forhindrer uønskede side-reaktioner mellem elektroden og elektro
Hybride indium-lithium anoder giver hurtig grænsefladeiontransportNye lithiumelektroder belagt med indium kunne være grundlaget for mere kraftfulde, længerevarende, genopladelige batterier. Belægningen forhindrer uønskede side-reaktioner mellem elektroden og elektro -
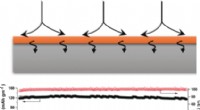
 Almindelig brugt kemisk fiksering forårsager aggregeringsartefakterFigur 1. En ny teknik til at observere levende cellemembraner for AFM ved hjælp af porøs siliciumnitridmembran (MPM). (a) Udseendet af MPM. (b) MPM-hullerne observeret af AFM. (c) MPM, når den er sat
Almindelig brugt kemisk fiksering forårsager aggregeringsartefakterFigur 1. En ny teknik til at observere levende cellemembraner for AFM ved hjælp af porøs siliciumnitridmembran (MPM). (a) Udseendet af MPM. (b) MPM-hullerne observeret af AFM. (c) MPM, når den er sat -
 Miniaturiseret massespektrometer til Mars-udforskning har et enormt potentialeKredit:Brigham Young University BYU-forskere har skabt en miniaturiseret, bærbar version af et værktøj, der nu er i stand til at analysere Mars atmosfære - og det er blot en af dets utallige anv
Miniaturiseret massespektrometer til Mars-udforskning har et enormt potentialeKredit:Brigham Young University BYU-forskere har skabt en miniaturiseret, bærbar version af et værktøj, der nu er i stand til at analysere Mars atmosfære - og det er blot en af dets utallige anv -
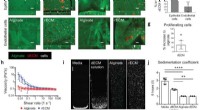 Ny bioink bringer 3D-print af menneskelige organer tættere på virkelighedenKarakterisering af rECM hybrid hydrogeler. a) Billede af alginat og mus rECM hydrogeler. Målestænger:1 mm. b) Alginat – fluorescein- og ECM – rhodamin -modificeret rECM -hydrogel, der viser fordelinge
Ny bioink bringer 3D-print af menneskelige organer tættere på virkelighedenKarakterisering af rECM hybrid hydrogeler. a) Billede af alginat og mus rECM hydrogeler. Målestænger:1 mm. b) Alginat – fluorescein- og ECM – rhodamin -modificeret rECM -hydrogel, der viser fordelinge
- Hvordan ligner Ceres på jorden?
- Hvordan magtafstandstro påvirker forbrugernes prisfølsomhed
- Mikrobenes rolle i industrien
- 'Her kommer solen':Har popmusik en 'regnrytme?'
- Hurtig transport i kulstof nanorørmembraner kan fremme menneskers sundhed
- Fysikere foreslår reversibel justering af nanopartiklers emissionsfarve


