Hvad er oxidationstallet for C i glukose?
1. Oxidationstallet for oxygen (O) er normalt -2.
2. Oxidationstallet for hydrogen (H) er normalt +1.
3. Summen af oxidationstallene for alle atomer i en neutral forbindelse er nul.
I betragtning af glucose (C6H12O6) kan vi tildele oxidationsnumrene som følger:
- Lad oxidationstallet for kulstof (C) være "x".
- Der er seks kulstofatomer, så det samlede oxidationstal fra kulstof er 6x.
- Der er tolv brintatomer, hver med et oxidationstal på +1, så det samlede oxidationstal fra brint er +12.
- Der er seks iltatomer, hver med et oxidationstal på -2, så det samlede oxidationstal fra ilt er -12.
Ifølge den tredje regel skal summen af oxidationstallene være nul:
6x + 12(+1) + 6(-2) =0
Forenkling af ligningen:
6x + 12 - 12 =0
6x =0
Ved at løse for x finder vi:
x =0
Derfor er oxidationstallet for kulstof (C) i glucose 0.
Sidste artikelHvad er betingelserne, når man tilføjer grus til is, og det virker?
Næste artikelHvad er ammoniak en væske eller gas?
 Varme artikler
Varme artikler
-
 Kemikere udvikler metode til hurtigt at screene, nøjagtigt identificere fentanyl og en bred vifte a…Kredit:McMaster University Forskere ved McMaster University har udviklet en ny lægemiddelscreeningsteknik, der kan føre til hurtig og nøjagtig identifikation af fentanyl, samt et stort antal andre
Kemikere udvikler metode til hurtigt at screene, nøjagtigt identificere fentanyl og en bred vifte a…Kredit:McMaster University Forskere ved McMaster University har udviklet en ny lægemiddelscreeningsteknik, der kan føre til hurtig og nøjagtig identifikation af fentanyl, samt et stort antal andre -
 Kulstoffangstprocessen producerer brint og byggematerialerKredit:CC0 Public Domain Ph.D. forsker Olawale Oloye og professor Anthony OMullane fra QUT Center for Clean Energy Technologies and Practices udviklede den elektrokemiske opsamling og omdannelse a
Kulstoffangstprocessen producerer brint og byggematerialerKredit:CC0 Public Domain Ph.D. forsker Olawale Oloye og professor Anthony OMullane fra QUT Center for Clean Energy Technologies and Practices udviklede den elektrokemiske opsamling og omdannelse a -
 Nyt katalysatormateriale producerer rigeligt billigt brintKredit:CC0 Public Domain QUT-kemiforskere har opdaget billigere og mere effektive materialer til fremstilling af brint til lagring af vedvarende energi, der kan erstatte nuværende vandspaltningska
Nyt katalysatormateriale producerer rigeligt billigt brintKredit:CC0 Public Domain QUT-kemiforskere har opdaget billigere og mere effektive materialer til fremstilling af brint til lagring af vedvarende energi, der kan erstatte nuværende vandspaltningska -
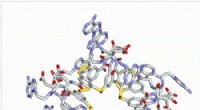 Forskere laver komplekst molekyle, der spontant folder som et proteinSet ovenfra af det centrale hulrum af det foldede molekyle. Kredit:Bin Liu, Universitetet i Groningen I biologi, foldede proteiner er ansvarlige for de fleste avancerede funktioner. Disse kompleks
Forskere laver komplekst molekyle, der spontant folder som et proteinSet ovenfra af det centrale hulrum af det foldede molekyle. Kredit:Bin Liu, Universitetet i Groningen I biologi, foldede proteiner er ansvarlige for de fleste avancerede funktioner. Disse kompleks


