Hvad er hybridiseringen af centralt atom i NOBr?
I betragtning af elektrongrupperne kan vi bruge teorien om valensskalelektronparrepulsion (VSEPR) til at forudsige den molekylære geometri. Tilstedeværelsen af et ensomt par og to bundne atomer skaber en trigonal pyramideformet elektronpargeometri omkring nitrogen.
For at imødekomme denne geometri gennemgår nitrogen sp3-hybridisering. Ved sp3-hybridisering dannes fire ækvivalente hybridorbitaler ved at blande en s orbitaler og tre p-orbitaler. Disse fire sp3 hybrid orbitaler har et tetraedrisk arrangement, hvor det enlige par indtager en af de tetraedriske positioner.
Derfor er hybridiseringen af det centrale atom (nitrogen) i NOBr sp3.
 Varme artikler
Varme artikler
-
 Enheden simulerer filtrering og iontransportfunktioner af menneskelige nyrerKredit:CC0 Public Domain Kemitekniske forskere ved University of Arkansas har udviklet en enhed, der simulerer blodfiltrering og iontransportfunktioner i den menneskelige nyre. Teknologien kan omd
Enheden simulerer filtrering og iontransportfunktioner af menneskelige nyrerKredit:CC0 Public Domain Kemitekniske forskere ved University of Arkansas har udviklet en enhed, der simulerer blodfiltrering og iontransportfunktioner i den menneskelige nyre. Teknologien kan omd -
 Forskningsteam afdækker ekstraordinære egenskaber ved strontiumniobatForskere ledet af professor T Venky Venkatesan (første række, centrum), Direktør for NUSNNI, afdækkede ekstraordinære egenskaber ved halvledermateriale strontiumniobat. Kredit:National University of S
Forskningsteam afdækker ekstraordinære egenskaber ved strontiumniobatForskere ledet af professor T Venky Venkatesan (første række, centrum), Direktør for NUSNNI, afdækkede ekstraordinære egenskaber ved halvledermateriale strontiumniobat. Kredit:National University of S -
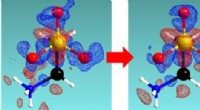 Statistisk inferens for at efterligne den meget erfarne krystallografs driftsmådePræcision af krystallografisk observation blev forbedret fra venstre mod højre ved hjælp af måledesign baseret på den foreslåede metode. Forskelle fra faktiske til sfæriske elektrontætheder er beskrev
Statistisk inferens for at efterligne den meget erfarne krystallografs driftsmådePræcision af krystallografisk observation blev forbedret fra venstre mod højre ved hjælp af måledesign baseret på den foreslåede metode. Forskelle fra faktiske til sfæriske elektrontætheder er beskrev -
 Kampen mod svære at behandle svampeinfektionerKonidioforer med konidier af de mikroskopiske svampe Aspergillus oryzae under lysmikroskop. Kredit:Yulianna.x / Wikimedia / CC BY-SA 4.0 Systemiske svampeinfektioner er meget sjældnere end andre s
Kampen mod svære at behandle svampeinfektionerKonidioforer med konidier af de mikroskopiske svampe Aspergillus oryzae under lysmikroskop. Kredit:Yulianna.x / Wikimedia / CC BY-SA 4.0 Systemiske svampeinfektioner er meget sjældnere end andre s
- Er et kviksølv i termometeret skinnende?
- Ny undersøgelse finder sammenhæng mellem fejlruhed og størrelsen af jordskælv
- Nu begynder vi:Ti enkle måder at gøre Australiens klimaspil til virkelig næste niveau
- Schweizisk til at holde vågne i stor højde for tabt gletsjer
- Dronebaseret termisk billeddannelse og analyse for energieffektivitet
- Alle systemer går, mens Parker Solar Probe begynder sin anden solbane


