Hvad er pH på 4,3x10-8 M H3O?
```
pH =-log[H3O+]
```
hvor [H3O+] repræsenterer koncentrationen af hydroniumioner i mol pr. liter (M).
I dette tilfælde får vi koncentrationen af H3O+ som 4,3 x 10-8 M. Ved at sætte denne værdi ind i formlen får vi:
```
pH =-log(4,3 x 10-8)
```
```
pH ≈ 7,37
```
Derfor er pH-værdien af en opløsning med en H3O+-koncentration på 4,3 x 10-8 M cirka 7,37. Dette indikerer, at opløsningen er let basisk, da en neutral opløsning har en pH-værdi på 7, og enhver værdi over 7 betragtes som basisk.
Sidste artikelHvad kaldes det den temperatur, hvor en væske koger?
Næste artikelHvad er molekylerne i pap?
 Varme artikler
Varme artikler
-
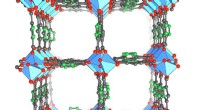 I ørkenforsøg, næste generations vandopsamler leverer frisk vand fra luftenKrystalstrukturen af de nyeste, aluminiumsbaseret metal-organisk ramme, MOF-303, som fanger dobbelt så meget vand som den tidligere MOF, der blev brugt i vandhøsteren. Kredit:Yaghi lab, UC Berkeley
I ørkenforsøg, næste generations vandopsamler leverer frisk vand fra luftenKrystalstrukturen af de nyeste, aluminiumsbaseret metal-organisk ramme, MOF-303, som fanger dobbelt så meget vand som den tidligere MOF, der blev brugt i vandhøsteren. Kredit:Yaghi lab, UC Berkeley -
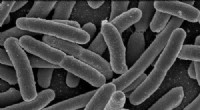 Virus skelner, ødelægge E. coli i drikkevandEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH For hurtigt at opdage tilstedeværelsen af E coli i drikkevand, Fødevareforskere fra Cornell University kan nu bruge en bakteriofa
Virus skelner, ødelægge E. coli i drikkevandEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH For hurtigt at opdage tilstedeværelsen af E coli i drikkevand, Fødevareforskere fra Cornell University kan nu bruge en bakteriofa -
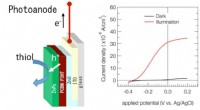 Miljøvenlige elektrokemiske katalysatorer, der bruger solceller til at høste energi fra solenStrukturen af den foreslåede enhed, viser, hvordan de genererede huller (h+) bruges til at lette thioloxidation. Den målte strøm stiger dramatisk under belysning og anvendelse af et lille potentiale
Miljøvenlige elektrokemiske katalysatorer, der bruger solceller til at høste energi fra solenStrukturen af den foreslåede enhed, viser, hvordan de genererede huller (h+) bruges til at lette thioloxidation. Den målte strøm stiger dramatisk under belysning og anvendelse af et lille potentiale -
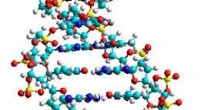 En præbiotisk vej til DNAKredit:Ludwig Maximilian Universitetet i München DNA kan være dukket op på Jorden tidligere, end man hidtil har antaget. LMU-kemikere ledet af Oliver Trapp viser, at en simpel reaktionsvej kunne h
En præbiotisk vej til DNAKredit:Ludwig Maximilian Universitetet i München DNA kan være dukket op på Jorden tidligere, end man hidtil har antaget. LMU-kemikere ledet af Oliver Trapp viser, at en simpel reaktionsvej kunne h
- Australske brande øgede CO2-men også kulstoffangende alger:undersøgelser
- Drone bruges til at hjælpe med 3-D-genindspilning af japansk interneringslejr
- Kunne laboratoriedyrket kød bane vejen for mere etisk, miljøvenlig mad?
- Smartphones kan forbedre den akademiske præstation, når det bruges rigtigt
- Moskva giver grønt lys til Yamal gas superprojekt
- Erdogan siger, at Uber sluttede i Tyrkiet


