Hvordan finder man iltprocenten i masse i en forbindelse?
1. Bestem den molære masse af forbindelsen.
- Læg atommasserne sammen for alle atomerne i forbindelsen.
2. Bestem massen af ilt i forbindelsen.
- Gang iltens atommasse (15,999 g/mol) med antallet af oxygenatomer i forbindelsen.
3. Beregn iltprocenten i masse.
- Divider massen af oxygen i forbindelsen med molmassen af forbindelsen, gang derefter med 100%.
Formel:
% oxygen efter masse =(iltmasse i forbindelse / molær masse af forbindelse) * 100 %
Eksempel:
For glucose (C6H12O6) er den molære masse:
(6 x 12,011 g/mol) + (12 x 1,008 g/mol) + (6 x 15,999 g/mol) =180,156 g/mol
Massen af oxygen i glukose er:
6 x 15,999 g/mol =95,994 g/mol
Den procentvise ilt i masse er:
% oxygen efter masse =(95,994 g/mol / 180,156 g/mol) * 100 % =53,29 %
Derfor udgør oxygen cirka 53,29% af massen af glukose.
Sidste artikelHvilket udtryk bruges til at repræsentere massen af 1 molekyle af et stof?
Næste artikelHvordan laver man tøris?
 Varme artikler
Varme artikler
-
 Ny teknik kan strømline lægemiddeldesignKredit:CC0 Public Domain Forskere har udviklet en proces, der kraftigt kan reducere arbejdet involveret i computerproteindesign, ifølge en undersøgelse i Proceedings of the National Academy of Sc
Ny teknik kan strømline lægemiddeldesignKredit:CC0 Public Domain Forskere har udviklet en proces, der kraftigt kan reducere arbejdet involveret i computerproteindesign, ifølge en undersøgelse i Proceedings of the National Academy of Sc -
 Forskere øger varmen på smeltede metaller for at skabe fremtidige teknologierBryan Owens-Baird, en kandidatstuderende forsker fra Iowa State University, forbereder sig på at studere en af sine prøver, en pulveriseret forbindelse af fosfor, silicium, og tin, med NOMAD -instru
Forskere øger varmen på smeltede metaller for at skabe fremtidige teknologierBryan Owens-Baird, en kandidatstuderende forsker fra Iowa State University, forbereder sig på at studere en af sine prøver, en pulveriseret forbindelse af fosfor, silicium, og tin, med NOMAD -instru -
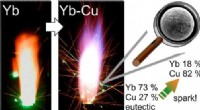 Forskere bruger sjældne jordarters metaller i legeringspulvere til at producere grønne, iøjnefald…Grafisk abstrakt. Kredit:ACS Omega (2022). DOI:10.1021/acsomega.2c03081 Stjernekastere kan være meget sjove - glimtende, brusende og spyttede lysbuer ud fra håndholdte pinde eller rør på jorden. Me
Forskere bruger sjældne jordarters metaller i legeringspulvere til at producere grønne, iøjnefald…Grafisk abstrakt. Kredit:ACS Omega (2022). DOI:10.1021/acsomega.2c03081 Stjernekastere kan være meget sjove - glimtende, brusende og spyttede lysbuer ud fra håndholdte pinde eller rør på jorden. Me -
 Elektronmikroskopi giver et nyt syn på lille virus med terapeutisk potentialeElektronmikroskopi giver et nyt syn på lille virus med terapeutisk potentiale. Indsat viser den cryo-EM-afledte struktur af en AAV2. Det fulde billede viser den eksperimentelt bestemte tæthed (grå) og
Elektronmikroskopi giver et nyt syn på lille virus med terapeutisk potentialeElektronmikroskopi giver et nyt syn på lille virus med terapeutisk potentiale. Indsat viser den cryo-EM-afledte struktur af en AAV2. Det fulde billede viser den eksperimentelt bestemte tæthed (grå) og
- AC Vs. DC-solenoider og hvordan de fungerer
- 5 reddet fra oversvømmelser, da orkanen oversvømmer Hawaii med regn
- Ny analytisk tilgang forbedrer kernemagnetisk resonanssignaldetektion i tidligere usynlige områder
- Sådan laver du en 3D-model af åndedrætssystemet
- I katastrofer vågner, nye computerteknikker understøtter beredskabspersonale
- DNA-reparation efter CRISPR-skæring slet ikke, hvad folk troede


