Hvad er de generelle fem typer reaktioner?
1. Kombinationsreaktioner (også kaldet syntesereaktioner): To eller flere stoffer kombineres og danner et enkelt produkt. For eksempel kombineres brint og ilt for at danne vand:
$$2H_2 + O_2 → 2H_2O$$
2. Dekomponeringsreaktioner: En enkelt forbindelse nedbrydes i to eller flere produkter. For eksempel nedbrydes vand til brint og ilt:
$$2H_2O → 2H_2 + O_2$$
3. Forbrændingsreaktioner: Et stof reagerer med ilt for at frigive varme og lys. For eksempel brænder metan i ilt for at producere kuldioxid og vand:
$$CH_4 + 2O_2 → CO_2 + 2H_2O$$
4. Enkelt-erstatningsreaktioner: Et grundstof erstatter et andet grundstof i en forbindelse. For eksempel reagerer jern med kobbersulfat for at producere jernsulfat og kobber:
$$Fe + CuSO_4 → FeSO_4 + Cu$$
5. Dobbelt-erstatningsreaktioner: To forbindelser udveksler ioner for at danne to nye forbindelser. For eksempel reagerer natriumchlorid og sølvnitrat for at producere natriumnitrat og sølvchlorid:
$$NaCl + AgNO_3 → NaNO_3 + AgCl$$
Sidste artikelHvordan smelter man grundstoffet kviksølv?
Næste artikelHvad er forskellen mellem korrosion af jernholdige og ikke-metaller?
 Varme artikler
Varme artikler
-
 Ammoniak:Et trumfkort til energiomstillingsprocessenKevin Rouwenhorst. Kredit:University of Twente Under sit praktikophold som Kemiteknologistuderende hos Haldor Topsøe, UT Ph.D. forsker Kevin Rouwenhorst indså de mange muligheder, som ammoniak give
Ammoniak:Et trumfkort til energiomstillingsprocessenKevin Rouwenhorst. Kredit:University of Twente Under sit praktikophold som Kemiteknologistuderende hos Haldor Topsøe, UT Ph.D. forsker Kevin Rouwenhorst indså de mange muligheder, som ammoniak give -
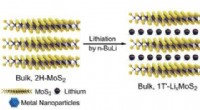 Brintproduktion i et begrænset rumFigur 1:Indkapslingen af ædelmetal nanopartikler i MoS2 ved en in-situ reduktion strategi. National University of Singapore kemikere har udviklet en metode til at begrænse ædelmetal -nanopartikl
Brintproduktion i et begrænset rumFigur 1:Indkapslingen af ædelmetal nanopartikler i MoS2 ved en in-situ reduktion strategi. National University of Singapore kemikere har udviklet en metode til at begrænse ædelmetal -nanopartikl -
 Kemiske ingeniører udgiver papir udfordrende teorier om glasovergangTermiske signaturer for en ultrastabil amorf teflon. (A) Varmestrøm versus temperatur for en 675 nm tyk VPD amorf teflonfilm ved forskellige afkølingshastigheder. (B) Logaritme af afkølingshastighed v
Kemiske ingeniører udgiver papir udfordrende teorier om glasovergangTermiske signaturer for en ultrastabil amorf teflon. (A) Varmestrøm versus temperatur for en 675 nm tyk VPD amorf teflonfilm ved forskellige afkølingshastigheder. (B) Logaritme af afkølingshastighed v -
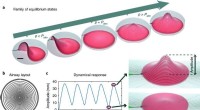 Ved at kombinere pneumatik med en hydrogel for at skabe en baromorf - til blød robotteknologien, Kontinuerlig familie af ligevægtstilstande opnået for en baromorf under forskellige tryk. b, Tilsvarende netværk af kanaler indlejret i pladen. Kanaler er mere koncentrerede i den centrale region
Ved at kombinere pneumatik med en hydrogel for at skabe en baromorf - til blød robotteknologien, Kontinuerlig familie af ligevægtstilstande opnået for en baromorf under forskellige tryk. b, Tilsvarende netværk af kanaler indlejret i pladen. Kanaler er mere koncentrerede i den centrale region
- Reducering af fosforafstrømning
- Hvordan man forklarer polaritet
- Forskere finder, at virkningerne af klimaændringer kan accelerere i midten af århundredet
- Kongressen stopper militær brug af giftigt skum, der forurener drikkevand
- Hvad sker der med dyrene i regnskoven, når det skæres ned?
- Forskere udvikler perovskit røntgendetektor til medicinsk billeddannelse


