Hvorfor indeholder affaldsgasserne CO2 og Ni-metan, når de brændes?
```
CH4 + 2O2 → CO2 + 2H2O
```
I denne reaktion oxideres carbonatomet i metan til CO2, mens hydrogenatomerne oxideres til H2O. Reaktionen er meget eksoterm, hvilket betyder, at den frigiver en stor mængde varmeenergi. Det er derfor, metan bruges som brændsel til opvarmning og madlavning.
Tilstedeværelsen af Ni i affaldsgasserne ville være usædvanlig og kunne indikere, at en nikkel-baseret katalysator blev brugt i forbrændingsprocessen. Det er dog usandsynligt, at der ville være betydelige mængder Ni til stede i affaldsgasserne. Tilstedeværelsen af metan i røggasserne tyder på, at forbrændingsprocessen var ufuldstændig, og at noget af metanen ikke blev omdannet til CO2 og H2O. Dette kan skyldes mangel på ilt i forbrændingsprocessen, eller det kan skyldes brugen af et brændstof af dårlig kvalitet.
Sidste artikelHvordan er Bohrs atommodel forskellig fra blommebudding-modellen?
Næste artikelHvad er fysisk-kemisk analyse?
 Varme artikler
Varme artikler
-
 Forskere laver verdens hurtigste molekylære skytteSkematisk fremstilling af en rotaxan, den type molekyle, der var genstand for undersøgelsen. Kredit:Wikimedia Commons Takket være et smart kemisk design, Det er lykkedes forskere ved universitetet
Forskere laver verdens hurtigste molekylære skytteSkematisk fremstilling af en rotaxan, den type molekyle, der var genstand for undersøgelsen. Kredit:Wikimedia Commons Takket være et smart kemisk design, Det er lykkedes forskere ved universitetet -
 3-D-print og månestøv:Et astronautsæt til fremtidig rumudforskning?(a) Foreløbige test for 3-D-printning af måneregolit-simulator NU-LHT-2M på en grundplade af kulstofstål og (b) SEM-billede af samme. Kredit:Politecnico di Milano En af de store udfordringer relat
3-D-print og månestøv:Et astronautsæt til fremtidig rumudforskning?(a) Foreløbige test for 3-D-printning af måneregolit-simulator NU-LHT-2M på en grundplade af kulstofstål og (b) SEM-billede af samme. Kredit:Politecnico di Milano En af de store udfordringer relat -
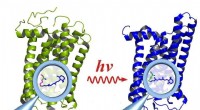 Ser komplekse molekyler på arbejdeRhodopsin før (venstre) og efter aktivering af lys (højre):Aktiveringen forårsager ændringer i funktionelle grupper inde i molekylet (forstørrelsesglas), som påvirker hele molekylet. Kredit:E. Ritter/
Ser komplekse molekyler på arbejdeRhodopsin før (venstre) og efter aktivering af lys (højre):Aktiveringen forårsager ændringer i funktionelle grupper inde i molekylet (forstørrelsesglas), som påvirker hele molekylet. Kredit:E. Ritter/ -
 Hurtige tests til tidlig diagnose af hjerteanfald og identifikation af sepsisHøjpræcisionsautomatisk dispenser til præcis påføring af specifikke reagenser. Kredit:©NUST MISIS NUST MISIS-forskere har udviklet en ny type membranteststrimmel til en kvantitativ immunokromatogr
Hurtige tests til tidlig diagnose af hjerteanfald og identifikation af sepsisHøjpræcisionsautomatisk dispenser til præcis påføring af specifikke reagenser. Kredit:©NUST MISIS NUST MISIS-forskere har udviklet en ny type membranteststrimmel til en kvantitativ immunokromatogr
- Hvad indikerer en vedvarende opblomstring af alger om planetens sundhed?
- Ny rejse til universet fra DESHIMA
- Ris, Penn State åbent center for 2-D belægninger
- Forskere foretager den første globale vurdering af drivhusgasemissioner fra plastik i livscyklussen
- Skiløbere såret af flyvende sten på japansk vulkan
- Fysikere siger, at samling af nanopartikler er som at bygge med LEGO'er


