Hvilke tiltrækningskræfter holder metanmolekyler sammen?
Metan er et ikke-polært molekyle, så det har ingen permanente dipol-dipol-attraktioner. Elektronerne i metanmolekylerne bevæger sig dog konstant, hvilket skaber midlertidige dipoler. Disse midlertidige dipoler kan inducere dipoler i nabomolekyler, hvilket resulterer i van der Waals-kræfter. Van der Waals kræfter er relativt svage, men de er de eneste tiltrækningskræfter mellem metanmolekyler.
Sidste artikelVands reaktion med andre stoffer er kendt som?
Næste artikelHvordan er blyant bly et mineral?
 Varme artikler
Varme artikler
-
 Laser spor terapi, næringsstoffer, toksinerI biologiske systemer, kulstof-14 kan bruges som et biokemisk sporstof til at spore mikrodoser af næringsstoffer, toksiner og terapeutika hos mennesker og dyr. Kredit:Lawrence Livermore National Labor
Laser spor terapi, næringsstoffer, toksinerI biologiske systemer, kulstof-14 kan bruges som et biokemisk sporstof til at spore mikrodoser af næringsstoffer, toksiner og terapeutika hos mennesker og dyr. Kredit:Lawrence Livermore National Labor -
 Forskere har opdaget, hvordan blodorme fremstiller deres unikke kobbertænderVenstre:Billede af den udbøjede snabel af Glycera dibranchiata med dens fire fritlagte kæber, højre:Scanningselektronmikroskopbillede af en Glycera-kæbe (Skalastang, 0,5 mm). Kredit:Matter/Wonderly et
Forskere har opdaget, hvordan blodorme fremstiller deres unikke kobbertænderVenstre:Billede af den udbøjede snabel af Glycera dibranchiata med dens fire fritlagte kæber, højre:Scanningselektronmikroskopbillede af en Glycera-kæbe (Skalastang, 0,5 mm). Kredit:Matter/Wonderly et -
 Forskere fremmer bedre billeddannelsesværktøj til at studere sygdomSpectrally encoded enhanced representations (SEER) teknologi fra USC virker op til 67 gange hurtigere med 2,7 gange større definition end andre teknikker. Kredit:Francesco Cutrale, USC USC-forsker
Forskere fremmer bedre billeddannelsesværktøj til at studere sygdomSpectrally encoded enhanced representations (SEER) teknologi fra USC virker op til 67 gange hurtigere med 2,7 gange større definition end andre teknikker. Kredit:Francesco Cutrale, USC USC-forsker -
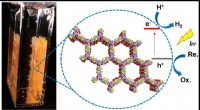 Forskere opdager meget aktiv organisk fotokatalysatorOrganisk katalysatormateriale til fotokatalytisk brintudvikling. Kredit:University of Liverpool Forskere fra University of Liverpool, University College London og East China University of Science
Forskere opdager meget aktiv organisk fotokatalysatorOrganisk katalysatormateriale til fotokatalytisk brintudvikling. Kredit:University of Liverpool Forskere fra University of Liverpool, University College London og East China University of Science
- Sikkerhedsteam diskuterede svaghed i bare metal-tjenester
- Hemmeligheden bag Australiens vulkaner afsløret i ny undersøgelse
- Kulstof nanorør kan billigt høste sollys
- Ny forskning i Kenya finder et sødt sted til at høste revfisk
- Mont Ventoux-skoven – et naturligt laboratorium til at studere virkningerne af klimaændringer
- Forskere opnår 51,5 dB ikke-gensidig isolation


