Reklamer for antacida hævder ofte, at disse produkter neutraliserer mavesyre. Antacida er baser. Hvad ville være en analogi til måden på hvilke syrer?
1. Syre-Base-reaktion :Når et antacida, som er en base, blandes med mavesyre, som er en syre, sker der en kemisk reaktion. Denne reaktion er en syre-base neutraliseringsreaktion.
2. Danning af salt og vand :Under reaktionen kombineres hydrogenionerne (H+) fra mavesyren med hydroxidionerne (OH-) fra antacidaen og danner vand (H2O). De resterende positivt ladede ioner fra antacidet (såsom natrium, calcium eller magnesium) kombineres med de negativt ladede ioner fra mavesyren og danner et salt.
3. Neutralisering :Saltet og vandet, der dannes som produkter af reaktionen, er neutrale forbindelser, hvilket betyder, at de ikke har sure eller basiske egenskaber. Som et resultat neutraliseres det sure miljø i maven, og pH-værdien af maveindholdet stiger.
4. Midlertidig nødhjælp :Antacida giver midlertidig lindring af halsbrand, fordøjelsesbesvær eller sure opstød ved at neutralisere mavesyre. Det er dog vigtigt at bemærke, at de ikke behandler den underliggende årsag til tilstanden. For langsigtet behandling af disse problemer anbefales det at konsultere en sundhedsperson.
5. Eksempler :Nogle almindelige antacida omfatter bagepulver (natriumbicarbonat), calciumcarbonat, magnesiumhydroxid og aluminiumhydroxid. Ligesom bagepulver neutraliserer eddike ved at reagere og danne vand og natriumacetat, reagerer antacida med mavesyre og danner vand og det tilsvarende salt.
 Varme artikler
Varme artikler
-
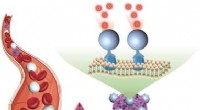 Direkte påvisning af cirkulerende tumorceller i blodprøverKredit:Wiley-VCH Tumorceller, der cirkulerer i blodet, er markører for tidlig opdagelse og prognose af kræft. Imidlertid, påvisning af disse celler er udfordrende på grund af deres knaphed. I jour
Direkte påvisning af cirkulerende tumorceller i blodprøverKredit:Wiley-VCH Tumorceller, der cirkulerer i blodet, er markører for tidlig opdagelse og prognose af kræft. Imidlertid, påvisning af disse celler er udfordrende på grund af deres knaphed. I jour -
 Ioniske faser af ammoniakrig hydrat opdaget ved høje densiteterDet foreslåede fasediagram for AHH baseret på dette brev og lavtryksdata fra Wilson et al. For de eksperimentelle data, forskellige farver skildrer forskellige faser, og forskellige fyldte symboler re
Ioniske faser af ammoniakrig hydrat opdaget ved høje densiteterDet foreslåede fasediagram for AHH baseret på dette brev og lavtryksdata fra Wilson et al. For de eksperimentelle data, forskellige farver skildrer forskellige faser, og forskellige fyldte symboler re -
 En hydrogel, der kan stoppe blødning fra en arterieKredit:CC0 Public Domain Et team af forskere tilknyttet flere institutioner i Kina har udviklet en hydrogel, der kan stoppe blødninger fra en punkteret arterie. I deres papir offentliggjort i tids
En hydrogel, der kan stoppe blødning fra en arterieKredit:CC0 Public Domain Et team af forskere tilknyttet flere institutioner i Kina har udviklet en hydrogel, der kan stoppe blødninger fra en punkteret arterie. I deres papir offentliggjort i tids -
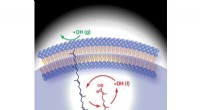 Forskere opdager et nyt spor bag aldersrelaterede sygdomme og madfordærvelseIllustration af Criegee-mellemmekanismen. Berkeley Lab-forskere har fundet en fælles sammenhæng mellem Criegee-mellemprodukter og nedbrydningen af de umættede lipider i fødevarer og cellerne i vores
Forskere opdager et nyt spor bag aldersrelaterede sygdomme og madfordærvelseIllustration af Criegee-mellemmekanismen. Berkeley Lab-forskere har fundet en fælles sammenhæng mellem Criegee-mellemprodukter og nedbrydningen af de umættede lipider i fødevarer og cellerne i vores
- Hvad får glas til at gå i stykker?
- Folk i højere social klasse har en overdrevet tro på, at de er bedre end andre
- Du kører som en pige:Undersøgelse viser kønsbias i opfattelsen af samkørsel
- Forskere rapporterer om mulige løsninger til svært genanvendelig plast
- Sådan identificerer du Baby Rattlesnakes
- Cambridge Analytica-skandale - legitime forskere, der bruger Facebook-data, kan være sideløbende s…


