Hvad er forskellen mellem en svag og stærk syre involverer syrer evne til at gøre hvad?
Dissocierer kun lidt i vand, og kun en lille brøkdel af syremolekyler producerer hydrogenioner.
En svag syre har en svag donerende kraft.
Fx:eddikesyre (CH3COOH)
Stærk syre: Dissocierer fuldstændigt i vand for at danne hydrogenioner og konjugeret base.
Producerer en meget høj koncentration af hydrogenioner.
En stærk syre har høj donationsevne.
Fx:saltsyre (Hcl), salpetersyre (HNO3)
Forskellen:
- Grad af dissociation:Svage syrer dissocierer kun delvist, mens stærke syrer dissocierer fuldstændigt.
- Ligevægt:Svage syrer når en ligevægtstilstand, hvor både dissocierede og udissocierede molekyler sameksisterer, mens stærke syrer dissocierer fuldstændigt, og ingen udissocierede molekyler forbliver.
- Brintionkoncentration:Svage syrer producerer en lavere koncentration af hydrogenioner sammenlignet med stærke syrer i samme koncentration.
- pH-værdi:Opløsninger af svage syrer har en højere pH-værdi end opløsninger af stærke syrer i samme koncentration.
- Ætsende:Stærke syrer er generelt mere ætsende end svage syrer på grund af deres høje hydrogenionkoncentration.
- Reaktivitet:Stærke syrer er mere reaktive og deltager lettere i kemiske reaktioner på grund af deres højere koncentration af brintioner.
 Varme artikler
Varme artikler
-
 Enkeltmolekyle påvisning af kræftmarkører bringer flydende biopsi tættere på klinikkenHver prik, der ses på dette PRAM-billede, repræsenterer ét mikroRNA, der er bundet til sensoren. Kredit:Nantao Li En hurtig, billig, men følsom teknik til at opdage kræftmarkører bringer forskere
Enkeltmolekyle påvisning af kræftmarkører bringer flydende biopsi tættere på klinikkenHver prik, der ses på dette PRAM-billede, repræsenterer ét mikroRNA, der er bundet til sensoren. Kredit:Nantao Li En hurtig, billig, men følsom teknik til at opdage kræftmarkører bringer forskere -
 Forskere kontrollerer de elektriske egenskaber af optiske hukommelsesenhederKredit: Journal of Materials Chemistry C (2019). DOI:10.1039/c9tc01273g En gruppe forskere fra Skoltech, Instituttet for problemer med kemisk fysik i RAS, og N.D. Zelinsky Institute of Organic Ch
Forskere kontrollerer de elektriske egenskaber af optiske hukommelsesenhederKredit: Journal of Materials Chemistry C (2019). DOI:10.1039/c9tc01273g En gruppe forskere fra Skoltech, Instituttet for problemer med kemisk fysik i RAS, og N.D. Zelinsky Institute of Organic Ch -
 Forskere foreslår at bruge maskinlæring til at forudsige materialers egenskaberForskere foreslog at bruge maskinlæringsmetoder til at forudsige egenskaberne af kunstige safirkrystaller. Det er et unikt materiale, der er meget udbredt i mikroelektronik, optik og elektronik. Kredi
Forskere foreslår at bruge maskinlæring til at forudsige materialers egenskaberForskere foreslog at bruge maskinlæringsmetoder til at forudsige egenskaberne af kunstige safirkrystaller. Det er et unikt materiale, der er meget udbredt i mikroelektronik, optik og elektronik. Kredi -
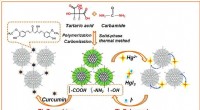 Hvordan nitrogen-doterede fluorescerende kulstofprikker hjælper kampen mod sygdomSkematisk diagram af forberedelses- og responsmekanismen for NCDer. Kredit:Wei Chen Evnen til pålideligt og præcist at detektere niveauer af iodidion og curcumin er afgørende inden for fødevare- o
Hvordan nitrogen-doterede fluorescerende kulstofprikker hjælper kampen mod sygdomSkematisk diagram af forberedelses- og responsmekanismen for NCDer. Kredit:Wei Chen Evnen til pålideligt og præcist at detektere niveauer af iodidion og curcumin er afgørende inden for fødevare- o
- Stor enkelt-krystal grafen er mulig
- NASAs Lucy på himlen med … asteroider?
- Hvilke funktionelle grupper findes i cellulose?
- Ny kompositteknologi til forbedret elektrisk og termisk ledningsevne af konventionelle kompositmater…
- Hvordan man dyrker ametystkrystal
- De sidste 12.000 år viser en mere kompleks klimahistorie end hidtil antaget


