Hvad er betingelserne for dannelse af oxider?
* Høj temperatur: Mange oxider dannes ved høje temperaturer. Det skyldes, at de høje temperaturer giver den nødvendige energi til at nedbryde bindingerne mellem iltatomerne og de andre atomer i forbindelsen.
* Tilstedeværelse af ilt: Det er klart, at der kræves oxygen for at danne oxider. Ilten kan være til stede i luften, eller den kan tilsættes til reaktionsblandingen.
* Et reduktionsmiddel: Et reduktionsmiddel er et stof, der donerer elektroner til et andet stof. I tilfælde af oxiddannelse donerer reduktionsmidlet elektroner til oxygenatomerne, hvilket gør det muligt for dem at binde sig til de andre atomer i forbindelsen.
* En katalysator: En katalysator er et stof, der fremskynder en kemisk reaktion uden at blive forbrugt i reaktionen. Nogle oxider kræver en katalysator for at dannes.
Følgende er nogle specifikke eksempler på de betingelser, der kræves for at danne oxider:
* Jernoxid: Jernoxid dannes, når jern opvarmes i nærvær af ilt. Den høje temperatur giver den energi, der skal til for at nedbryde bindingerne mellem jernatomerne og iltatomerne, og ilten i luften reagerer med jernet og danner jernoxid.
* Kuldioxid: Kuldioxid dannes, når kulstof forbrændes i nærvær af ilt. Den høje temperatur af det brændende kulstof giver den energi, der skal til for at nedbryde bindingerne mellem kulstofatomerne og oxygenatomerne, og ilten i luften reagerer med kulstoffet og danner kuldioxid.
* Vand: Vand dannes, når brint og ilt kombineres under de rigtige forhold. En flammes høje temperatur giver den energi, der skal til for at nedbryde bindingerne mellem brintatomerne og oxygenatomerne, og ilten i luften reagerer med brinten og danner vand.
Oxider findes overalt omkring os, og de spiller en vigtig rolle i mange kemiske processer. Ved at forstå de betingelser, der kræves for at oxider kan dannes, kan vi bedre forstå disse processer og bruge dem til vores fordel.
Sidste artikelHvad er kendetegnende elektron?
Næste artikelHvad er det kemiske navn på stensalt?
 Varme artikler
Varme artikler
-
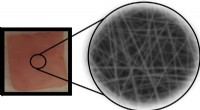 Implanterbar piezoelektrisk polymer forbedrer kontrolleret frigivelse af lægemidlerEn implanterbar piezoelektrisk polymer nanofiber -enhed, der frigiver kontrollerede mængder af et lægemiddel under mekanisk kraft. Kredit:Jin Nam/UCR En membran lavet af tråde af en polymer, der a
Implanterbar piezoelektrisk polymer forbedrer kontrolleret frigivelse af lægemidlerEn implanterbar piezoelektrisk polymer nanofiber -enhed, der frigiver kontrollerede mængder af et lægemiddel under mekanisk kraft. Kredit:Jin Nam/UCR En membran lavet af tråde af en polymer, der a -
 Nyt open source-websted indeholder tegninger til lab-on-a-chip-enhederMetafludics.org, et nyt MIT open source-websted, leverer tegninger til mikrofluidiske dele. På billedet er et par billeder fra hjemmesiden. Kredit:Metafludics.org Et nyt MIT-designet open source-w
Nyt open source-websted indeholder tegninger til lab-on-a-chip-enhederMetafludics.org, et nyt MIT open source-websted, leverer tegninger til mikrofluidiske dele. På billedet er et par billeder fra hjemmesiden. Kredit:Metafludics.org Et nyt MIT-designet open source-w -
 Forskere kan forudsige og designe enkeltatomkatalysatorer til vigtige kemiske reaktionerKredit:CC0 Public Domain Forskere ved Tufts University, University College London (UCL), Cambridge University og University of California i Santa Barbara har vist, at en katalysator faktisk kan væ
Forskere kan forudsige og designe enkeltatomkatalysatorer til vigtige kemiske reaktionerKredit:CC0 Public Domain Forskere ved Tufts University, University College London (UCL), Cambridge University og University of California i Santa Barbara har vist, at en katalysator faktisk kan væ -
 AI-drevet mikroskop kunne kontrollere kræftmargener på få minutterEt nyt mikroskop kaldet DeepDOF bruger kunstig intelligens til hurtigt og billigt at afbilde alle cellerne i store vævssnit (til venstre) i høj opløsning med minimal forberedelse, eliminerer den dyre
AI-drevet mikroskop kunne kontrollere kræftmargener på få minutterEt nyt mikroskop kaldet DeepDOF bruger kunstig intelligens til hurtigt og billigt at afbilde alle cellerne i store vævssnit (til venstre) i høj opløsning med minimal forberedelse, eliminerer den dyre
- Natriumbaserede batterier kan gøre din smartphone billigere og renere
- Et system til at påvirke hypnagogiske mikrodrømme
- Lyskontrollerede Higgs-tilstande findes i superledere; potentiale sensor, computerbrug
- Hvad sker der med kinetisk energi, når stoffet bliver varmere?
- Forskere udvikler metode til at teste seismisk sårbarhed af vandrørledningssystemer
- Sådan bruger du din telefon til at maksimere juleindkøb


