Hvor mange atomer er der i 63,5 g kulilte?
Den molære masse af carbonmonoxid (CO) er 28,01 g/mol. Det betyder, at et mol kulilte vejer 28,01 gram.
Avogadros tal er 6.022 x 10^23. Dette betyder, at et mol af ethvert stof indeholder 6,022 x 10^23 atomer (eller molekyler).
Så for at beregne antallet af atomer i 63,5 g carbonmonoxid kan vi bruge følgende formel:
Antal atomer =(masse i gram) / (molær masse i g/mol) * Avogadros tal
Ved at erstatte de givne værdier i formlen får vi:
Antal atomer =(63,5 g) / (28,01 g/mol) * (6,022 x 10^23 atomer/mol)
Antal atomer =1,43 x 10^24 atomer
Derfor er der 1,43 x 10^24 atomer i 63,5 g carbonmonoxid.
Sidste artikelEr chloroform blandbar med petroleumsether?
Næste artikelAntallet af valenselektroner for 1s22s22p4 er?
 Varme artikler
Varme artikler
-
 Perovskite solceller:Perfektion kræves ikkeForenklet tværsnit af en perovskit solcelle:perovskitlaget dækker ikke hele overfladen, men udviser i stedet huller. Forskerne kunne vise, at der opbygges et beskyttende lag, som forhindrer kortslutni
Perovskite solceller:Perfektion kræves ikkeForenklet tværsnit af en perovskit solcelle:perovskitlaget dækker ikke hele overfladen, men udviser i stedet huller. Forskerne kunne vise, at der opbygges et beskyttende lag, som forhindrer kortslutni -
 Kemikere skaber en ny vej i søgen efter antibiotikaForskere ved Yale University arbejder på en kemisk proces, der kan føre til skabelsen af en ny klasse af antibiotika. Kredit:Michael S. Helfenbein Yale University forskere har udviklet en ny kem
Kemikere skaber en ny vej i søgen efter antibiotikaForskere ved Yale University arbejder på en kemisk proces, der kan føre til skabelsen af en ny klasse af antibiotika. Kredit:Michael S. Helfenbein Yale University forskere har udviklet en ny kem -
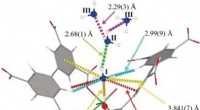 Et robust materiale til optagelse og opbevaring af ammoniak ved tætheder, der kommer tæt på den f…Kredit:Wiley Håndtering, opbevaring, og forsendelse af ammoniak kræver dyrt udstyr og særlige forholdsregler på grund af dets iboende ætsende og toksiske egenskaber. Forskere i Manchester, Storbri
Et robust materiale til optagelse og opbevaring af ammoniak ved tætheder, der kommer tæt på den f…Kredit:Wiley Håndtering, opbevaring, og forsendelse af ammoniak kræver dyrt udstyr og særlige forholdsregler på grund af dets iboende ætsende og toksiske egenskaber. Forskere i Manchester, Storbri -
 Ny teknik til bestemmelse af afstand i cellerIn-celleafstandsbestemmelse ved EPR afslører væsentlig strukturel information om biomakromolekyler under native betingelser. For første gang, den pulserede EPR -teknik RIDME (relaxation induced dipola
Ny teknik til bestemmelse af afstand i cellerIn-celleafstandsbestemmelse ved EPR afslører væsentlig strukturel information om biomakromolekyler under native betingelser. For første gang, den pulserede EPR -teknik RIDME (relaxation induced dipola
- Elektronisk stemmeafgivning kan øge valgdeltagelsen blandt unge ved kommunalvalg
- Nanopartikler påvirker deres flydende miljø:Undersøgelse præsenterer atomindsigt
- Sådan beregnes Kovats-indeks
- Australien godkender nyt kulprojekt, efterhånden som klimaadvarslerne vokser
- Udvinding af spildevand til gødning og energi for at forhindre vandmangel


