Er sio2 mere sur end so2?
SiO2 er surt, fordi det kan reagere med vand og danne kiselsyre (H4SiO4). Reaktionen mellem SiO2 og vand kan repræsenteres som følger:
SiO2(s) + 2H2O(l) → H4SiO4(vandig)
I denne reaktion donerer SiO2 to protoner til vandmolekyler og danner kiselsyre- og hydroniumioner (H3O+). Hydroniumionerne er ansvarlige for kiselsyrens sure egenskaber.
På den anden side er SO2 også surt, men det er mindre surt end SiO2. Dette skyldes, at SO2 kun har et surt hydrogenatom, hvorimod SiO2 har fire. Reaktionen mellem SO2 og vand kan repræsenteres som følger:
SO2(g) + H2O(l) → H2SO3(vandig)
I denne reaktion donerer SO2 en proton til et vandmolekyle og danner svovlsyre (H2SO3) og hydroniumioner. Hydroniumionerne er ansvarlige for svovlsyrlingens sure egenskaber.
Fordi SiO2 kan donere flere protoner end SO2, er det mere surt end SO2.
Sidste artikelForskellen mellem sure pellets og basiske pellets?
Næste artikelCalamine er en base eller syre?
 Varme artikler
Varme artikler
-
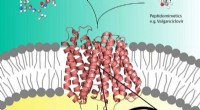 Røntgenbilleder afslører layout af lastet lægemiddeltransportørPro-lægemidler som Valganciclovir (øverst til højre) kan bruge peptidtransportøren (i midten) i cellemembranen, der normalt transporterer næringsstofpeptider (øverst til venstre) ind i cellen. Kredit:
Røntgenbilleder afslører layout af lastet lægemiddeltransportørPro-lægemidler som Valganciclovir (øverst til højre) kan bruge peptidtransportøren (i midten) i cellemembranen, der normalt transporterer næringsstofpeptider (øverst til venstre) ind i cellen. Kredit: -
 Hvordan enzymer producerer brintMartin Winkler (højre) og Thomas Happe (venstre) har fanget et enzyms forbigående mellemliggende tilstand. Kredit:Ruhr-Universitaet-Bochum Forskere ved Ruhr-Universität Bochum og Freie Universität
Hvordan enzymer producerer brintMartin Winkler (højre) og Thomas Happe (venstre) har fanget et enzyms forbigående mellemliggende tilstand. Kredit:Ruhr-Universitaet-Bochum Forskere ved Ruhr-Universität Bochum og Freie Universität -
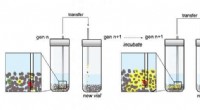 Livlig kemi skabt i laboratoriesøgning efter måder at studere livets oprindelse påForskerne udsatte deres kemiske supper for en form for selektion ved at tage en lille mængde materiale fra et hætteglas og placere det i et nyt hætteglas med frisk pyrit og kemikalier. Efter flere gen
Livlig kemi skabt i laboratoriesøgning efter måder at studere livets oprindelse påForskerne udsatte deres kemiske supper for en form for selektion ved at tage en lille mængde materiale fra et hætteglas og placere det i et nyt hætteglas med frisk pyrit og kemikalier. Efter flere gen -
 Selvdrevne papirspåner kunne hjælpe med at slå en tidlig alarm for skovbrandeEn sensor (hvid strimmel) på en stueplante aktiverer en alarm, når ilden er tæt på. Kredit:Tilpasset fra ACS anvendte materialer og grænseflader 2020 De seneste ødelæggende brande i Amazonas reg
Selvdrevne papirspåner kunne hjælpe med at slå en tidlig alarm for skovbrandeEn sensor (hvid strimmel) på en stueplante aktiverer en alarm, når ilden er tæt på. Kredit:Tilpasset fra ACS anvendte materialer og grænseflader 2020 De seneste ødelæggende brande i Amazonas reg
- Kabelførte islændinge søger at holde fjerntliggende halvø digital-fri
- Hvorfor forbrugere giver afkald på sæder på forreste række:Ofrer oplevelseskvalitet for sammenho…
- Hurtig og præcis flerfarvebilleddannelse af biomolekyler nu mulig
- Frysetørrede jordbær og is giver et meget stabilt forhold
- Menneskeheden står over for et afgørende spørgsmål:Hvordan vil AI ændre os?
- Soliton-molekyler fik til at vibrere som rigtige molekyler


