Hvordan enzymer producerer brint

Martin Winkler (højre) og Thomas Happe (venstre) har fanget et enzyms forbigående mellemliggende tilstand. Kredit:Ruhr-Universitaet-Bochum
Forskere ved Ruhr-Universität Bochum og Freie Universität Berlin har præciseret det afgørende katalytiske trin i produktionen af brint med enzymer. Enzymerne, kaldet [FeFe] -hydrogenaser, effektivt omdanne elektroner og protoner til brint. De er således en kandidat til den bioteknologiske produktion af den potentielle energikilde. "For at producere brint i industriel skala ved hjælp af enzymer, vi skal præcist forstå, hvordan de fungerer, "siger prof. Thomas Happe, en af forfatterne til undersøgelsen.
Teamet ledet af Happe og Dr. Martin Winkler fra den Bochum-baserede fotobioteknologiske arbejdsgruppe rapporterer om resultaterne med Berlin-baserede kolleger ledet af Dr. Sven Stripp i tidsskriftet Naturkommunikation .
Enzym virker i to retninger
Hydrogenaser kan arbejde i to retninger:de gør protoner og elektroner til brint, og også opdele hydrogen i protoner og elektroner. Disse reaktioner finder sted i det aktive centrum af hydrogenasen, som er en kompleks struktur omfattende seks jern- og seks svovlatomer, kaldet H-klyngen. Under den katalytiske proces, denne klynge passerer gennem talrige mellemstater.
Når molekylært brint (H2) deles, brintmolekylet binder i første omgang til H-klyngen. "Hydrogenase -forskere var altid overbeviste om, at H2 måtte dele sig ujævnt i reaktionens første trin, "forklarer Martin Winkler. Ideen:En positivt ladet proton (H+) og en negativt ladet hydridion (H-) skabes, som derefter fortsætter med at reagere hurtigt for at danne to protoner og to elektroner. "Hydridtilstanden i det aktive enzym, hvor hydridionen således er bundet til det aktive center, er meget ustabil - indtil videre har ingen været i stand til at verificere dette, "siger Winkler. Det er netop det, forskerne nu har opnået.
Trick gør ustabil tilstand synlig
Ved hjælp af et trick, de forstærkede H-klyngetilstanden med hydridionen, så det kunne verificeres spektroskopisk. Når brint deles, der opnås en kemisk ligevægt mellem de involverede reaktionspartnere - protoner, hydridioner og brintmolekyler. Koncentrationerne af de tre brinttilstande bestemmes af en dynamisk ligevægt af katalytiske H-klyngetilstande. Da forskerne tilføjede store mængder protoner og brint til blandingen udefra, de tippede balancen - til fordel for hydridtilstanden. Det aktive center med den negativt ladede hydridion akkumuleret i en større mængde; nok til at være målbar.
Holdet demonstrerede også hydrid mellemliggende tilstand, som også forekommer under brintproduktion, i yderligere forsøg med hydrogenaser, der var blevet ændret på en bestemt måde.
"Vi var således i stand til at demonstrere det katalytiske princip for disse hydrogenaser i et forsøg for første gang, "opsummerer Thomas Happe." Dette giver et afgørende grundlag for at gengive H-klyngens meget effektive katalytiske mekanisme til industriel produktion af brint. "Enzymerne kan omdanne op til 10, 000 brintmolekyler pr. Sekund.
Sidste artikelUndersøgelse af porerne i membranvesikler
Næste artikelHvordan forskere opfinder nye farver
 Varme artikler
Varme artikler
-
 Forskergruppen opdager gummimateriale, der kan føre til ridsefri lak til bilenQueens University Belfast -forskning kan betyde ridsefast maling til biler. Kredit:Queens University Belfast Anført af Dr Elton Santos fra Universitys School of Mathematics and Physics, et interna
Forskergruppen opdager gummimateriale, der kan føre til ridsefri lak til bilenQueens University Belfast -forskning kan betyde ridsefast maling til biler. Kredit:Queens University Belfast Anført af Dr Elton Santos fra Universitys School of Mathematics and Physics, et interna -
 Kemikere opdager måder at lave nye nitrogenprodukter ud af luftenKredit:CC0 Public Domain Et smart træk med nitrogen har bragt verden et skridt tættere på at skabe en række nyttige produkter – fra farvestoffer til lægemidler – ud af den blå luft. Opdagelsen ko
Kemikere opdager måder at lave nye nitrogenprodukter ud af luftenKredit:CC0 Public Domain Et smart træk med nitrogen har bragt verden et skridt tættere på at skabe en række nyttige produkter – fra farvestoffer til lægemidler – ud af den blå luft. Opdagelsen ko -
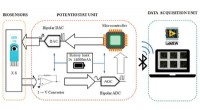 Bluetooth-aktiveret enhed registrerer gæringsprocessen over dageBlokdiagram over multikanalpotentiostaten med seks 3-elektrode biosensorer, der producerer data, der strømmer gennem et printkort og transmitterer trådløst til et LabVIEW-interface ved hjælp af Blueto
Bluetooth-aktiveret enhed registrerer gæringsprocessen over dageBlokdiagram over multikanalpotentiostaten med seks 3-elektrode biosensorer, der producerer data, der strømmer gennem et printkort og transmitterer trådløst til et LabVIEW-interface ved hjælp af Blueto -
 Video:Surfside-lejlighedskollaps og videnskaben om betonBetonbygninger falder ikke bare sammen ud af det blå. Selv jordskælv er ikke meningen at bringe dem ned. Så hvorfor byggede Champlain Towers South-bygningen i Surfside, Florida - en moderne struktur b
Video:Surfside-lejlighedskollaps og videnskaben om betonBetonbygninger falder ikke bare sammen ud af det blå. Selv jordskælv er ikke meningen at bringe dem ned. Så hvorfor byggede Champlain Towers South-bygningen i Surfside, Florida - en moderne struktur b
- Systemet tildeler bedre tidfølsom databehandling på tværs af kerner for at opretholde hurtige bru…
- Hvordan tackling af voldtægtsmyter blandt nævninge kan bidrage til at øge dommene under retssagen
- Myter og risici i app, der giver dig et kig ind i ældre selv
- Fremmedsprogsundervisningen bliver mere og mere sparsom
- Antallet af børnefattigdom kan halveres i det næste årti efter forslag i en ny ekspertrapport
- Superledning og ferromagnetisme bekæmper en jævn match


