Hvordan bestemmer man en molekyleformel ud fra den empiriske formel?
Forstå molær masse:Find ud af molmassen af den empiriske formel ved at summere atommasserne af alle de tilstedeværende grundstoffer.
Analyser grundstofsammensætning:Bestem den empiriske formels grundstofsammensætning i procent.
Beregn molekylvægt:Indhent information om molekylvægten (eller den molære masse) af forbindelsen. Dette leveres normalt eksperimentelt gennem teknikker såsom massespektrometri.
Beregn multiplikator:Divider molekylvægten med den empiriske formels molære masse. Resultatet er et helt tal, som er multiplikatoren (n).
Multiplicer subscripts:Multiplicer alle subscripts i den empiriske formel med n for at opnå den molekylære formel.
Bekræft molekylvægten:Bekræft, at molekylvægten af molekylformlen svarer til den eksperimentelt opnåede molekylvægt.
Her er et eksempel, hvor du bruger ethylenglycol til at illustrere disse trin:
Empirisk formel:CH2O
Molær masse med empirisk formel (CH2O):
(1 x 12,01 g/mol C) + (2 x 1,01 g/mol H) + (1 x 16,00 g/mol O) =30,03 g/mol
Eksperimentel molekylvægt af ethylenglycol:62,07 g/mol
Multiplikator (n):
62,07 g/mol / 30,03 g/mol =2
Molekylformel:
C2H4O2
Molekylvægt af molekylformel (C₂H4O₂):
(2 x 12,01 g/mol C) + (4 x 1,01 g/mol H) + (2 x 16,00 g/mol O) =62,07 g/mol
Molekylformlen for ethylenglycol er således C2H4O2, hvilket svarer til den eksperimentelle molekylvægt.
Sidste artikelHar C6H12 og C6h14 den samme emoiriske formel?
Næste artikelHvad er den empiriske formel for c12h12?
 Varme artikler
Varme artikler
-
 Massespektrometriteknik hjælper med at identificere forfalskede Robert Burns-manuskripterRobert Burns af Alexander Nasmyth (1758-1840). Kredit:Public Domain Et team af forskere ved University of Glasgow har udviklet en massespektrometriteknik til at identificere forfalskede manuskript
Massespektrometriteknik hjælper med at identificere forfalskede Robert Burns-manuskripterRobert Burns af Alexander Nasmyth (1758-1840). Kredit:Public Domain Et team af forskere ved University of Glasgow har udviklet en massespektrometriteknik til at identificere forfalskede manuskript -
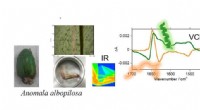 Mikroskopisk vibrationel cirkulær dikroisme muliggør kortlægning af supramolekylær chiralitetIR-intensitetskortlægning og VCD-spektre af Anomala albopilosa. Kredit:Hisako Sato, Ehime Universitet Insektvinger er interessante og attraktive som unikke eksempler på bioinspirerede og biomimeti
Mikroskopisk vibrationel cirkulær dikroisme muliggør kortlægning af supramolekylær chiralitetIR-intensitetskortlægning og VCD-spektre af Anomala albopilosa. Kredit:Hisako Sato, Ehime Universitet Insektvinger er interessante og attraktive som unikke eksempler på bioinspirerede og biomimeti -
 Ultralet materiale modstår supersoniske mikropartikelpåvirkningerIngeniører ved MIT, Caltech, og ETH Zürich finder nanoarkitekterede materialer designet ud fra præcist mønstrede nanoskalastrukturer (billedet) kan være en lovende vej til letvægtsrustning, beskyttend
Ultralet materiale modstår supersoniske mikropartikelpåvirkningerIngeniører ved MIT, Caltech, og ETH Zürich finder nanoarkitekterede materialer designet ud fra præcist mønstrede nanoskalastrukturer (billedet) kan være en lovende vej til letvægtsrustning, beskyttend -
 Skin et lys:Ny forskning viser, hvordan lavenergilys kan bøje plastikForskere afslørede en måde at bruge lavenergilys til at manipulere fotopolymerer eller plastfilm. Kredit:Florida State University Et hold af Florida State University-forskere har afsløret en måde a
Skin et lys:Ny forskning viser, hvordan lavenergilys kan bøje plastikForskere afslørede en måde at bruge lavenergilys til at manipulere fotopolymerer eller plastfilm. Kredit:Florida State University Et hold af Florida State University-forskere har afsløret en måde a
- I den fjerne fremtid, stjernernes forbiflyvninger vil fuldstændig demontere solsystemet
- Vævsintegreret følsom glucose nanosenor bruger inaktivt glucoseoxidase enzym til kontinuerlig over…
- Hvordan Google fik stater til at legalisere førerløse biler (Opdatering)
- Forskere afslører det molekylære grundlag for syn
- NASA ser kraftige tordenvejr i centrum af Tropical Storm Lidias
- Hot topic:Hvordan varmestrøm påvirker Jordens magnetfelt


