Forklar forskellen i reaktionshastigheder for et givet metal med to forskellige syrer?
1. Metallets reaktivitet: Forskellige metaller har varierende reaktivitet med syrer. Nogle metaller, såsom natrium eller kalium, er meget reaktive og reagerer kraftigt med syrer, mens andre, såsom guld eller platin, er relativt inerte og reagerer langsomt eller slet ikke. Et metals reaktivitet bestemmes af dets placering i det periodiske system og dets elektroniske konfiguration.
2. Syrens styrke: Styrken af en syre spiller også en afgørende rolle for at bestemme reaktionshastigheden. Stærke syrer, såsom saltsyre (HCl) eller svovlsyre (H2SO4), dissocieres fuldstændigt i vand og frigiver en høj koncentration af hydrogenioner (H+). Dette fører til en hurtigere reaktionshastighed med metaller sammenlignet med svage syrer, såsom eddikesyre (CH3COOH), som delvist dissocierer og frigiver færre H+-ioner.
3. Koncentration af syren: Koncentrationen af syren påvirker reaktionshastigheden. Når koncentrationen af syren stiger, er flere H+ ioner tilgængelige til at reagere med metallet, hvilket fører til en hurtigere reaktionshastighed. For eksempel vil en højere koncentration af HCl reagere hurtigere med et metal end en lavere koncentration af HCl.
4. Temperatur: Forøgelse af temperaturen øger generelt reaktionshastigheden. Højere temperaturer giver mere energi til reaktanterne, så de lettere kan overvinde aktiveringsenergibarrieren og reagere hurtigere. Nogle metaller kan dog reagere langsommere ved højere temperaturer på grund af dannelsen af et beskyttende oxidlag på deres overflader.
5. Inhibitorer og katalysatorer: Tilstedeværelsen af visse stoffer kan enten hæmme eller katalysere reaktionen mellem et metal og en syre. Inhibitorer sænker reaktionshastigheden, mens katalysatorer fremskynder den. For eksempel kan tilsætning af et stof som natriumthiosulfat (Na2S2O3) hæmme reaktionen mellem jern og saltsyre ved at danne et beskyttende lag af jernsulfid på metallets overflade.
Ved at overveje disse faktorer er det muligt at forstå og forudsige forskellene i reaktionshastigheder mellem et givet metal og to forskellige syrer. Metallets reaktivitet, syrernes styrke og koncentration, temperaturen og tilstedeværelsen af inhibitorer eller katalysatorer bidrager alle til den samlede reaktionshastighed.
Sidste artikelEr argonatomer og en calciumion isoelektroniske?
Næste artikelEr H2O en væske eller gas?
 Varme artikler
Varme artikler
-
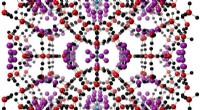 CO2 clathrate hydrat egenskaberFigur 1:Krystalstruktur af et CO2-klatrathydrat. Burstrukturen er dannet ud fra interaktionen af CO2-gas med vandmolekyler i is (rød og sort:ilt- og brintatomer, henholdsvis). CO2-molekyler (blå og
CO2 clathrate hydrat egenskaberFigur 1:Krystalstruktur af et CO2-klatrathydrat. Burstrukturen er dannet ud fra interaktionen af CO2-gas med vandmolekyler i is (rød og sort:ilt- og brintatomer, henholdsvis). CO2-molekyler (blå og -
 Evergreen idé gør biomasse-DNA til nedbrydelige materialerKredit:CC0 Public Domain DNA har mange praktiske anvendelser. Det gemmer blueprintet af genetisk kode. Det hjælper med at indlede arternes udvikling. Det kan også potentielt gøre en stærkere, mer
Evergreen idé gør biomasse-DNA til nedbrydelige materialerKredit:CC0 Public Domain DNA har mange praktiske anvendelser. Det gemmer blueprintet af genetisk kode. Det hjælper med at indlede arternes udvikling. Det kan også potentielt gøre en stærkere, mer -
 Forskere genopdager hurtigtvirkende tysk insekticid tabt i kølvandet på Anden VerdenskrigEn monofluoranalog af DDT, set gennem et optisk mikroskop. Faste fluorerede former for DDT dræbte insekter hurtigere end DDT. Kredit:Xiaolong Zhu og Jingxiang Yang, NYU Institut for Kemi En ny und
Forskere genopdager hurtigtvirkende tysk insekticid tabt i kølvandet på Anden VerdenskrigEn monofluoranalog af DDT, set gennem et optisk mikroskop. Faste fluorerede former for DDT dræbte insekter hurtigere end DDT. Kredit:Xiaolong Zhu og Jingxiang Yang, NYU Institut for Kemi En ny und -
 Nedbrydelige elektroniske komponenter fremstillet af majsstivelseKredit:American Chemical Society Efterhånden som forbrugerne opgraderer deres gadgets i et stigende tempo, mængden af elektronisk affald, vi genererer, fortsætter med at stige. For at hjælpe med
Nedbrydelige elektroniske komponenter fremstillet af majsstivelseKredit:American Chemical Society Efterhånden som forbrugerne opgraderer deres gadgets i et stigende tempo, mængden af elektronisk affald, vi genererer, fortsætter med at stige. For at hjælpe med
- Omkostningerne til COVID-19-svindel vil sandsynligvis stige betydeligt, rapporten afsluttes
- NASA ser tropisk cyklon Berguitta gennemblødning af Mauritius og øen Reunion
- Hvorfor virksomheder undervurderer behovet for at tilpasse ekstreme klimahændelser
- Minimering af virkningen af restaurantlukninger, restriktioner i Kina midt i COVID-19-krisen
- Vejret end vådt:Global opvarmning betyder mere regn for asiatiske monsunregioner
- Chip-baserede enheder forbedrer anvendeligheden af kvantesikret kommunikation


