Hvilken saltbro bruges i en elektrokemisk celle af kobberzink?
Kaliumnitrat opløses i vand til positivt ladede kaliumioner (K+) og negativt ladede nitrationer (NO3-). Når cellen er i drift, sker migrationen af ioner for at opretholde ladningsneutralitet i elektrolytten. Kaliumionerne bevæger sig mod katoden (zinkelektrode), mens nitrationerne vandrer mod anoden (kobberelektroden).
Saltbroen har flere vigtige funktioner:
1. Ladningsbærer:Saltbroen tillader bevægelse af ioner for at fuldende det elektriske kredsløb. Det giver en vej til overførsel af ladning mellem de to halvceller, hvilket sikrer strømmen af elektrisk strøm.
2. Forhindrer direkte blanding:Saltbroen adskiller de to halvceller og forhindrer direkte kontakt og blanding af deres opløsninger. Denne adskillelse er væsentlig for at opretholde de distinkte elektrodereaktioner og for at undgå uønskede sidereaktioner.
3. Opretholder ladningsneutralitet:Når ioner migrerer gennem saltbroen, opretholder de ladningsneutralitet i elektrolytrummene. Dette hjælper med at stabilisere cellens potentiale og sikrer en kontinuerlig strøm af strøm.
4. Minimerer koncentrationsændringer:Saltbroen minimerer koncentrationsændringer i halvcellerummene. Ved at tillade bevægelser af ioner sikrer det, at opløsningernes sammensætning forbliver relativt konstant over tid.
Det er værd at bemærke, at valget af saltbro (såsom kaliumnitrat eller andre egnede salte) afhænger af forskellige faktorer, herunder de specifikke elektrodematerialer og ønskede eksperimentelle forhold.
Sidste artikelHvad er hybridiseringen af centralt atom i H3O?
Næste artikelHvor mange repræsentative partikler er der i 2,5 mol?
 Varme artikler
Varme artikler
-
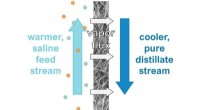 Hvordan gør man et bedre stykke arbejde med at rense saltvand? Ved at holde afsaltningsværktøj tø…Den varme vandstrøm med høj saltholdighed er på den ene side af membranen og en kølig ren vandstrøm på den anden. det opvarmede vand fordamper, efterlader saltet og danner en damp, som omdannes til en
Hvordan gør man et bedre stykke arbejde med at rense saltvand? Ved at holde afsaltningsværktøj tø…Den varme vandstrøm med høj saltholdighed er på den ene side af membranen og en kølig ren vandstrøm på den anden. det opvarmede vand fordamper, efterlader saltet og danner en damp, som omdannes til en -
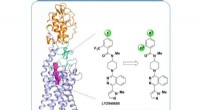 Forskere dechifrerer multi-domænet, struktur i fuld længde af den menneskelige glattede receptorStruktur af multi-domæne human Smoothened receptor, et vigtigt lægemiddelmål for kræftsygdomme. Kredit:ShanghaiTech University Et team af forskere ledet af iHuman Institute of ShanghaiTech Univers
Forskere dechifrerer multi-domænet, struktur i fuld længde af den menneskelige glattede receptorStruktur af multi-domæne human Smoothened receptor, et vigtigt lægemiddelmål for kræftsygdomme. Kredit:ShanghaiTech University Et team af forskere ledet af iHuman Institute of ShanghaiTech Univers -
 AI identificerer ændringer i mikrostruktur i aldrende materialerTopologisk analyse af røntgen-CT-data til genkendelse og trending af ændringer i mikrostruktur under materialeældning. Kredit:Lawrence Livermore National Laboratory Lawrence Livermore National Lab
AI identificerer ændringer i mikrostruktur i aldrende materialerTopologisk analyse af røntgen-CT-data til genkendelse og trending af ændringer i mikrostruktur under materialeældning. Kredit:Lawrence Livermore National Laboratory Lawrence Livermore National Lab -
 Forskere opdager en bedre måde at lave plast af svovl påKredit:CC0 Public Domain Forskere ved University of Liverpool har opdaget en ny proces til fremstilling af polymerer af svovl, som kan være en måde at fremstille plast på, der er mindre skadeligt
Forskere opdager en bedre måde at lave plast af svovl påKredit:CC0 Public Domain Forskere ved University of Liverpool har opdaget en ny proces til fremstilling af polymerer af svovl, som kan være en måde at fremstille plast på, der er mindre skadeligt
- Hvilken af følgende Bronstead-Lowry-syrer opfører sig ikke som en stærk syre, når den er oplø…
- NASAs Perseverance rover begynder sin første videnskabskampagne på Mars
- Washington omfavner kontantfrit liv-men til hvilken pris?
- Den eksperimentelle observation af ekkoer i et enkelt molekyle
- Ny indsigt i Jordens kulstofkredsløb
- Eksperter måler de økonomiske konsekvenser af COVID-19-pandemien


